Эта статья может быть слишком технической для понимания большинством читателей . ( Июль 2013 г. ) ( Узнайте, как и когда удалить этот шаблон сообщения ) |
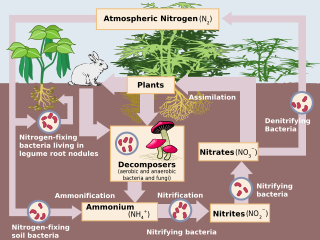
Влияние человека на круговорот азота разнообразно. В настоящее время поступления азота (N) в окружающую среду в сельском хозяйстве и промышленности превышают поступления в результате естественной фиксации азота . [1] Вследствие антропогенного воздействия глобальный цикл азота (рис. 1) значительно изменился за последнее столетие. Глобальные мольные доли закиси азота (N 2 O) в атмосфере увеличились с доиндустриального значения ~ 270 нмоль / моль до ~ 319 нмоль / моль в 2005 году. [2] На деятельность человека приходится более одной трети выбросов N 2 O. , большая часть которых приходится на аграрный сектор. [2]Эта статья предназначена для того, чтобы дать краткий обзор истории антропогенного поступления азота и описанных воздействий азота на отдельные наземные и водные экосистемы .
История антропогенного поступления азота [ править ]
| Типы еды | Подкисляющие выбросы (г экв. SO 2 на 100 г белка) |
|---|---|
| Говядина | 343,6 |
| Сыр | 165,5 |
| Свинина | 142,7 |
| Баранина и баранина | 139,0 |
| Фермерские ракообразные | 133,1 |
| Домашняя птица | 102,4 |
| Выращенная рыба | 65,9 |
| Яйца | 53,7 |
| Арахис | 22,6 |
| Горох | 8,5 |
| Тофу | 6,7 |
Примерно 78% атмосферы Земли составляет газообразный азот (N 2 ), который является инертным соединением и биологически недоступен для большинства организмов. Для использования в большинстве биологических процессов N 2 должен быть преобразован в реактивный N (Nr), который включает неорганические восстановленные формы (NH 3 и NH 4 + ), неорганические окисленные формы (NO, NO 2 , HNO 3 , N 2 O и NO 3 - ) и органических соединений ( мочевина , амины и белки ). [1] N 2 имеет прочную тройную связь и поэтому имеет значительное количество энергии (226 ккал моль−1 ) требуется для преобразования N 2 в Nr. [1] До промышленных процессов единственными источниками такой энергии были солнечное излучение и электрические разряды. [1] Используя большое количество метаболической энергии и фермент нитрогеназу , некоторые бактерии и цианобактерии превращают атмосферный N 2 в NH 3 , процесс, известный как биологическая азотфиксация (BNF). [4] Антропогенным аналогом BNF является процесс Габера-Боша , в котором H 2 реагирует с атмосферным N 2.при высоких температурах и давлениях с образованием NH 3 . [5] Наконец, N 2 превращается в NO под действием энергии молнии , которой можно пренебречь в нынешних умеренных экосистемах, или при сжигании ископаемого топлива . [1]
До 1850 года природный BNF, BNF, вызванный выращиванием (например, посев зернобобовых культур), и включенное органическое вещество были единственными источниками азота для сельскохозяйственного производства. [5] На рубеже веков Nr из залежей гуано и нитрата натрия собирали и экспортировали с засушливых островов Тихого океана и пустынь Южной Америки. [5] К концу 1920-х годов первые промышленные процессы, хотя и неэффективные, широко использовались для производства NH 3 . [1] Благодаря усилиям Фрица Габера и Карла Боша, процесс Габера-Боша стал крупнейшим источником азотных удобрений после 1950-х годов и заменил BNF в качестве основного источника производства NH 3 . [5] С 1890 по 1990 год антропогенно созданный Nr увеличился почти в девять раз. [1] За это время человеческое население увеличилось более чем в три раза, отчасти из-за увеличения производства продуктов питания.
После промышленной революции дополнительным источником антропогенного поступления азота стало сжигание ископаемого топлива , которое используется для высвобождения энергии (например, для питания автомобилей). При сжигании ископаемого топлива высокие температуры и давление обеспечивают энергию для производства NO в результате окисления N 2 . [1] Кроме того, при добыче и сжигании ископаемого топлива ископаемый азот может стать реактивным (т.е. выбросы NO x ). [1] В 1970-х годах ученые начали осознавать, что поступления азота накапливаются в окружающей среде и влияют на экосистемы. [1]
Воздействие антропогенных факторов на азотный цикл [ править ]
Между 1600 и 1990 годами глобальное производство химически активного азота (Nr) увеличилось почти на 50%. [6] В течение этого периода атмосферные выбросы видов Nr, по сообщениям, увеличились на 250%, а их осаждение в морских и наземных экосистемах увеличилось более чем на 200%. [6] Кроме того, сообщалось о четырехкратном увеличении притока растворенного неорганического азота в прибрежные районы. [6] Азот является важным ограничивающим питательным веществом во многих системах, включая леса, водно-болотные угодья, прибрежные и морские экосистемы; следовательно, это изменение в выбросах и распределении Nr привело к значительным последствиям для водных и наземных экосистем. [7] [8]
Атмосфера [ править ]
| Типы еды | Выбросы парниковых газов (г экв. CO 2 -C на грамм белка) |
|---|---|
| Мясо жвачных животных | 62 |
| Рециркуляционная аквакультура | 30 |
| Траловое рыболовство | 26 |
| Аквакультура без рециркуляции | 12 |
| Свинина | 10 |
| Домашняя птица | 10 |
| Молочный | 9.1 |
| Нетраловый промысел | 8,6 |
| Яйца | 6,8 |
| Крахмалистые корни | 1,7 |
| Пшеница | 1.2 |
| Кукуруза | 1.2 |
| Бобовые | 0,25 |
Поступающие в атмосферу N в основном включают оксиды N (NO x ), аммиака (NH 3 ) и закиси азота (N 2 O) из водных и наземных экосистем [4] и NO x в результате сжигания ископаемого топлива и биомассы. [1]
В агроэкосистемах внесение удобрений привело к усилению микробной нитрификации (аэробный процесс, при котором микроорганизмы окисляют аммоний [NH 4 + ] до нитрата [NO 3 - ]) и денитрификации (анаэробный процесс, при котором микроорганизмы восстанавливают NO 3 - до атмосферного азота [N 2 ]). ). Оба процесса естественным образом приводят к утечке оксида азота (NO) и закиси азота (N 2 O) в атмосферу. [4] Особое беспокойство вызывает N 2 O, который имеет средний срок службы в атмосфере 114–120 лет [10] и в 300 раз более эффективен, чем CO 2.как парниковый газ . [4] NO x, образующийся в промышленных процессах, автомобилях и сельскохозяйственных удобрениях, и NH 3, выбрасываемый из почв (т.е. как дополнительный побочный продукт нитрификации) [4] и животноводство, переносятся в подветренные экосистемы, влияя на круговорот азота и потери питательных веществ. Были названы шесть основных эффектов выбросов NO x и NH 3 : [1] 1) снижение видимости атмосферы из-за аэрозолей аммония (мелкодисперсные твердые частицы [PM]); 2) повышенная концентрация озона ; 3) озон и ТЧ влияют на здоровье человека (например,респираторные заболевания , рак ); 4) усиление радиационного воздействия и глобального изменения климата ; 5) снижение продуктивности сельского хозяйства из-за осаждения озона ; и 6) закисление экосистем [11] и эвтрофикация .
Биосфера [ править ]
Наземные и водные экосистемы получают Nr из атмосферы в результате влажного и сухого осаждения. [1] Атмосферные виды Nr могут откладываться в экосистемах в виде осадков (например, NO 3 - , NH 4 + , органические соединения азота), в виде газов (например, NH 3 и газообразная азотная кислота [HNO 3 ]) или в виде аэрозолей ( например, нитрат аммония [NH 4 NO 3 ]). [1] Водные экосистемы получают дополнительный азот из поверхностных и речных стоков . [8]
Повышенное осаждение N может подкислять почвы, ручьи и озера и изменять продуктивность лесов и пастбищ. В экосистемах пастбищ внесение азота привело к первоначальному увеличению продуктивности, а затем к ее снижению по мере превышения критических пороговых значений. [1] Также было продемонстрировано влияние азота на биоразнообразие , круговорот углерода и изменения в видовом составе. В высокоразвитых районах прибрежных прибрежных океанических и устьевых систем реки доставляют прямые (например, поверхностный сток ) и косвенные (например, загрязнение грунтовых вод) поступления азота от агроэкосистем. [8] Увеличение поступления азота может привести к закислению пресной воды и эвтрофикации морских вод.
Наземные экосистемы [ править ]
Влияние на продуктивность и круговорот питательных веществ [ править ]
Большая часть земного роста в системах с умеренным климатом ограничена N; поэтому поступление азота (например, посредством осаждения и удобрения) может увеличить доступность азота, что временно увеличивает поглощение азота, рост растений и микробов, а также накопление азота в биомассе растений и органическом веществе почвы . [12] Включение большего количества азота в органическое вещество снижает соотношение C: N, увеличивая выделение минерального азота (NH 4 + ) во время разложения органического вещества гетеротрофными микробами (например, аммонификации ). [13] По мере увеличения аммонификации увеличивается и нитрификация минерализованного азота. Поскольку микробная нитрификация и денитрификацияявляются "негерметичными", ожидается, что осаждение N приведет к увеличению выбросов газовых примесей. [14] Кроме того, с увеличением накопления NH 4 + в почве в процессе нитрификации высвобождаются ионы водорода, которые подкисляют почву. NO 3 - , продукт нитрификации, очень подвижен и может вымываться из почвы вместе с положительно заряженными щелочными минералами, такими как кальций и магний. [4] В кислых почвах мобилизованные ионы алюминия могут достигать токсичных концентраций, отрицательно влияя как на наземные, так и на прилегающие водные экосистемы.
Антропогенные источники азота обычно попадают в горные леса в результате осаждения . [15] Потенциальной проблемой увеличения осаждения N в результате деятельности человека является изменение круговорота питательных веществ в лесных экосистемах. Многочисленные исследования продемонстрировали как положительное, так и отрицательное воздействие атмосферного осаждения N на продуктивность лесов и накопление углерода. Добавлено N часто быстро обездвижены микробами , [16] и эффект от остального доступного N зависит от способности сообщества завода для поглощения N. [17] В системах с высоким поглощением N ассимилируется биомассой растений, что приводит к увеличению чистой первичной продуктивности (NPP) и, возможно, к увеличениюсвязывание углерода за счет большей фотосинтетической способности. Однако реакция экосистемы на добавление азота зависит от многих факторов, характерных для конкретного участка, включая климат, историю землепользования и количество добавок азота. Например, на северо-востоке США древостои лиственных пород, получающие постоянное поступление азота, продемонстрировали большую способность удерживать азот и увеличивать годовую чистую первичную продуктивность (НППП), чем древостоя хвойных пород. [18] Когда ввод N превышает потребность системы, N может быть потерян из-за выщелачивания и газовых потоков. Когда доступный азот превышает поглощающую способность экосистемы (например, растительность, почва, микробы и т. Д.), Происходит насыщение азотом и избыток азота теряется в поверхностных водах, грунтовых водах и атмосфере. [12] [17] [18]Насыщение азотом может привести к дисбалансу питательных веществ (например, потере кальция из-за вымывания нитратов) и возможному упадку леса. [13]
15-летнее исследование хронических добавок азота в программе Гарвардских лесных долгосрочных экологических исследований ( LTER ) пролило свет на многие последствия увеличения осаждения азота на круговорот питательных веществ в лесах умеренного пояса. Было обнаружено, что постоянное добавление азота приводит к большим потерям от выщелачивания, повышенной смертности сосны и прекращению накопления биомассы. [18] В другом исследовании сообщалось, что хроническое добавление азота приводит к накоплению нефотосинтетического азота и, следовательно, к снижению фотосинтетической способности, что предположительно приводит к серьезному углеродному стрессу и смертности. [17] Эти результаты опровергают предыдущие гипотезы о том, что увеличение поступления азота приведет к увеличению АЭС и секвестрации углерода .
Воздействие на разнообразие видов растений [ править ]
Многие растительные сообщества развивались в условиях низкого содержания питательных веществ; следовательно, увеличение поступления азота может изменить биотические и абиотические взаимодействия, что приведет к изменениям в составе сообщества. Несколько исследований по добавлению питательных веществ показали, что увеличение поступления азота приводит к доминированию быстрорастущих видов растений, что приводит к снижению видового богатства. [19] [20] [21] Быстрорастущие виды имеют большее сродство к поглощению азота и вытесняют медленнорастущие виды растений, блокируя доступ солнечному свету своей более высокой надземной биомассой. [22] Другие исследования показали, что вторичные реакции системы на обогащение N, включая закисление почвы и изменения микоризСообщества позволили стрессоустойчивым видам вытеснить чувствительные виды. [11] [23] Деревья с арбускулярными микоризными ассоциациями с большей вероятностью выиграют от увеличения почвенного азота, поскольку эти грибы не могут расщеплять органический азот почвы. [24] Два других исследования обнаружили доказательства того, что увеличение доступности азота привело к сокращению численности вересковых пустошей с разнообразием видов . Вересковые пустоши характеризуются бедными азотом почв, что исключает азотные травы; однако по мере увеличения осаждения N и подкисления почвы вторжение пастбищ заменяет низинные пустоши. [25] [26]
В более позднем экспериментальном исследовании внесения азотных удобрений и нарушения (т.е. обработки почвы) в старой сукцессии полей было обнаружено, что видовое богатство снижалось с увеличением азота, независимо от уровня нарушения. Эксперименты по конкуренции показали, что конкурентные доминанты исключают конкурентоспособно низшие виды между событиями нарушения. При увеличении поступления азота конкуренция сместилась с подземной на надземную (т. Е. К конкуренции за свет), и темпы заселения участков значительно снизились. Эти внутренние изменения могут кардинально повлиять на сообщество, сдвигая баланс между конкуренцией и колонизацией между видами. [21] В системах, основанных на патчах, региональное сосуществование может происходить за счет компромиссов в конкурентных и колонизаторских способностях при достаточно высоких уровнях нарушений. [27]Таким образом, при обратном ранжировании конкурентных и колонизирующих способностей растения могут сосуществовать в пространстве и времени, поскольку нарушение удаляет более сильных конкурентов из участков, что позволяет создать высших колонизаторов. Однако, как продемонстрировали Уилсон и Тилман, увеличение поступления питательных веществ может свести на нет компромиссы, что приведет к конкурентному исключению этих превосходных колонизаторов / бедных конкурентов. [21]
Водные экосистемы [ править ]
Водные экосистемы также по-разному реагируют на обогащение азотом. NO 3 - нагрузка из насыщенных азотом наземных экосистем может привести к закислению пресноводных систем ниже по течению и эвтрофикации морских систем ниже по течению. Подкисление пресной воды может вызвать отравление алюминием и гибель чувствительных к pH видов рыб. Поскольку морские системы, как правило, ограничены азотом, чрезмерное поступление азота может привести к ухудшению качества воды из-за токсичного цветения водорослей, недостатка кислорода, потери среды обитания, сокращения биоразнообразия и потерь рыболовства. [8]
Подкисление пресных вод [ править ]
Отложения азота из атмосферы в наземных ландшафтах могут быть преобразованы в результате микробных процессов в почве в биологически доступный азот, что может привести к подкислению поверхностных вод и утрате биоразнообразия . Поступление NO 3 - и NH 4 + из наземных систем и атмосферы может подкислять пресноводные системы, когда буферная емкость мала из-за подкисления почвы . [8] Загрязнение азотом в Европе, северо-востоке США и Азии является актуальной проблемой для подкисления пресной воды . [28]Исследования подкисления озер в экспериментальной зоне озер (ELA) на северо-западе Онтарио четко продемонстрировали негативное влияние повышенной кислотности на местные виды рыб: пополнение и рост озерной форели (Salvelinus namaycush) резко сократились из-за истребления ее основных видов добычи во время подкисления. [29]Реактивный азот из сельского хозяйства, животноводства, удобрений, септических систем и других источников повысил концентрацию нитратов в водных путях большинства промышленно развитых стран. Концентрация нитратов в 1000 норвежских озер увеличилась вдвое менее чем за десятилетие. Количество рек на северо-востоке Соединенных Штатов и большей части Европы за последнее столетие увеличилось в 10-15 раз. Реактивный азот может загрязнять питьевую воду через сток в ручьи, озера, реки и грунтовые воды. Только в Соединенных Штатах целых 20% источников подземных вод превышают установленный Всемирной организацией здравоохранения предел концентрации нитратов в питьевой воде. Эти высокие концентрации могут вызвать «болезнь голубого ребенка», когда ионы нитрата ослабляют способность крови переносить кислород.Исследования также связывают высокие концентрации нитратов с репродуктивными проблемами и склонностью к некоторым видам рака, таким как рак мочевого пузыря и яичников.[30]
Эвтрофикация морских систем [ править ]
Урбанизация, обезлесение и сельскохозяйственная деятельность в значительной степени способствуют попаданию наносов и питательных веществ в прибрежные воды через реки. [8] Увеличение поступления биогенных веществ в морские системы продемонстрировало как краткосрочное повышение продуктивности и улова, так и долгосрочные пагубные последствия эвтрофикации . Утроение NO 3 - нагрузки в реке Миссисипи во второй половине 20 века коррелировало с увеличением вылова рыбы в водах, окружающих дельту Миссисипи; [31] Однако, эти питательные входы произвели сезонную гипоксию (концентрации кислорода менее 2-3 мг L -1 , « мертвые зоны ») в Мексиканском заливе. [1] [8] В эстуарных и прибрежных системах высокие поступления питательных веществ увеличивают первичную продукцию (например, фитопланктон , морские травы, макроводоросли), что увеличивает мутностьчто приводит к уменьшению проникновения света через толщу воды. Следовательно, рост подводной растительности снижается, что снижает сложность среды обитания и снижает выработку кислорода. Повышенная первичная продукция (например, фитопланктон, макроводоросли и т. Д.) Приводит к потоку углерода в придонные воды, когда разлагающееся органическое вещество (т. Е. Стареющая первичная продукция) опускается и потребляется аэробными бактериями, находящимися ниже в толще воды. В результате потребление кислорода в придонных водах больше, чем его диффузия из поверхностных вод. Кроме того, при цветении определенных водорослей, называемом вредоносным цветением водорослей (ВЦВ), образуются токсины, которые могут действовать как нервно-мышечные соединения или соединения, повреждающие органы. Цветение водорослей может быть вредным как для других морских обитателей, так и для людей. [32] [33]
Интеграция [ править ]
Вышеупомянутые реакции системы на поступление реактивного азота (Nr) почти полностью изучаются отдельно; однако исследования все чаще указывают на то, что проблемы загрузки азота связаны множеством путей транспортировки питательных веществ через границы системы. [1] Этот последовательный переход между экосистемами называется каскадом азота. [6] ( см. Иллюстрацию из Программы Организации Объединенных Наций по окружающей среде ). Во время каскада некоторые системы накапливают Nr, что приводит к временной задержке в каскаде и усилению воздействия Nr на среду, в которой он накапливается. В конечном итоге антропогенные поступления Nr либо накапливаются, либо денитрифицированы; Однако в определении относительной важности накопления Nr иденитрификация , которая произошла в основном из-за отсутствия интеграции между научными дисциплинами. [1] [34]
Большая часть Nr поступает в глобальные агроэкосистемы, каскадом проходит через атмосферу, водные и наземные экосистемы до тех пор, пока он не преобразуется в N 2 , в основном за счет денитрификации . [1] Хотя земная денитрификация производит газообразные промежуточные соединения (оксид азота [NO] и закись азота [N 2 O]), последний этап - микробное производство N 2 - имеет решающее значение, поскольку атмосферный N 2 является стоком для Nr. [34] Многие исследования ясно продемонстрировали, что управляемые буферные полосы и заболоченные земли могут удалять значительные количества нитратов (NO 3 - ) из сельскохозяйственных систем посредствомденитрификация . [35] Такое управление может помочь ослабить нежелательные каскадные эффекты и устранить накопление Nr в окружающей среде. [1]
Человеческая деятельность доминирует в глобальных и большинстве региональных N-циклов. [36] Поступления азота показали негативные последствия как для круговорота питательных веществ, так и для разнообразия местных видов в наземных и водных системах. Фактически, из-за долгосрочного воздействия на пищевые сети поступления Nr широко считаются наиболее серьезной проблемой загрязнения в морских системах. [8] Как в наземных, так и в водных экосистемах реакция на обогащение N различается; однако общая повторяющаяся тема - важность пороговых значений (например, насыщения азота ) в способности системы удерживать питательные вещества. Для того чтобы контролировать каскад N, необходимо интегрировать научные дисциплины и продолжить работу по хранению Nr и скорости денитрификации . [34]
См. Также [ править ]
- Планетарные границы
Ссылки [ править ]
- ^ a b c d e f g h i j k l m n o p q r s t Галлоуэй, Дж. Нью-Йорк; Aber, JD; Эрисман, JNW; Зейтцингер, ИП; Ховарт, RW; Обтекатель EB; Косби, Би Джей (2003). «Азотный каскад». Бионаука . 53 (4): 341. DOI : 10,1641 / 0006-3568 (2003) 053 [0341: УЧПУ] 2.0.CO; 2 .
- ^ а б Аллей и др. 2007. Изменение климата МГЭИК 2007: основы физических наук. Вклад Рабочей группы I в Третий оценочный доклад Межправительственной группы экспертов по изменению климата. Сводный отчет для политиков (SPM). Архивировано 16 июля 2011 г. в Wayback Machine .
- ^ Nemecek, T .; Пур, Дж. (2018-06-01). «Снижение воздействия продуктов питания на окружающую среду за счет производителей и потребителей». Наука . 360 (6392): 987–992. Bibcode : 2018Sci ... 360..987P . DOI : 10.1126 / science.aaq0216 . ISSN 0036-8075 . PMID 29853680 . S2CID 206664954 .
- ^ a b c d e f Schlesinger, WH 1997. Биогеохимия: анализ глобальных изменений , Сан-Диего, Калифорния.
- ^ a b c d Смил, В. 2001. Обогащение земли: Фриц Габер, Карл Бош и трансформация мирового производства продуктов питания . MIT Press, Кембридж, Массачусетс.
- ^ a b c d Галлоуэй, Джеймс Н .; Коулинг, Эллис Б. (2002). «Реактивный азот и мир: 200 лет перемен». AMBIO: журнал окружающей человека среды . 31 (2): 64–71. DOI : 10.1579 / 0044-7447-31.2.64 . PMID 12078011 . S2CID 8104525 .
- ^ Vitousek, P .; Ховарт, Р. (1991). «Ограничение азота на суше и в море: как это может произойти?». Биогеохимия . 13 (2). DOI : 10.1007 / BF00002772 . S2CID 93106377 .
- ^ a b c d e f g h Rabalais, Nancy N. (2002). «Азот в водных экосистемах». AMBIO: журнал окружающей человека среды . 31 (2): 102–12. DOI : 10,1639 / 0044-7447 (2002) 031 [0102: NIAE] 2.0.CO; 2 . PMID 12077998 .
- ^ Майкл Кларк; Тилман, Дэвид (ноябрь 2014 г.). «Глобальные диеты связывают экологическую устойчивость и здоровье человека». Природа . 515 (7528): 518–522. Bibcode : 2014Natur.515..518T . DOI : 10,1038 / природа13959 . ISSN 1476-4687 . PMID 25383533 . S2CID 4453972 .
- ^ Джон Т. Хотон , Ю. Дин, диджей Григс, М. Ногер, П. ван дер Линдена, Х. Даи, К. Maskell, и СА Джонсон. 2001. IPCC Climate Change 2001: The Scientific Basis. Вклад Рабочей группы I в Третий оценочный доклад Межправительственной группы экспертов по изменению климата . Cambridge University Press]
- ^ а б Houdijk, ALFM; Verbeek, PJM; Дейк, HFG; Рулофс, JGM (1993). «Распространение и уменьшение исчезающих видов травянистых пустошей в зависимости от химического состава почвы». Растение и почва . 148 : 137–143. DOI : 10.1007 / BF02185393 . S2CID 22600629 .
- ^ a b Aber, JD, KJ Nadelhoffer, P. Steudler и JM Melillo. 1989. «Насыщение азотом в северных лесных экосистемах». Биология 39: 378–386
- ^ a b Aber, JD (1992). «Круговорот азота и насыщение азотом в лесных экосистемах умеренного пояса». Тенденции в экологии и эволюции . 7 (7): 220–224. DOI : 10.1016 / 0169-5347 (92) 90048-G . PMID 21236013 .
- ^ Matson, P; Lohse, KA; Холл, SJ (2002). «Глобализация осаждения азота: последствия для наземных экосистем». Амбио . 31 (2): 113–9. DOI : 10,1639 / 0044-7447 (2002) 031 [0113: tgondc] 2.0.co; 2 . JSTOR 4315223 . PMID 12077999 .
- ^ Абер, Джон Д .; Goodale, Christine L .; Ollinger, Scott V .; Смит, Мария-Луиза; Мэджилл, Элисон Х .; Мартин, Мэри Э .; Hallett, Ричард А .; Стоддард, Джон Л. (2003). «Меняет ли отложение азота на азотный статус северо-восточных лесов?». Бионаука . 53 (4): 375. DOI : 10,1641 / 0006-3568 (2003) 053 [0375: INDATN] 2.0.CO; 2 . JSTOR 1314369 .
- ^ Nadelhoffer, KJ; Даунс, MR; Фрай, Б. (1999). «Мойки для обогащения 15N в дубовом лесу и на плантациях красной сосны». Экологические приложения . 9 : 72–86. DOI : 10,1890 / 1051-0761 (1999) 009 [0072: SFNEAT] 2.0.CO; 2 .
- ^ а б в Бауэр, Джорджия; Bazzaz, FA; Minocha, R .; Long, S .; Magill, A .; Aber, J .; Бернсон, GM (2004). «Влияние хронических добавок азота на химию тканей, фотосинтетическую способность и потенциал секвестрации углерода красной сосны (Pinus Resinosa Ait.) На северо-востоке Соединенных Штатов». Экология и управление лесами . 196 : 173–186. DOI : 10.1016 / j.foreco.2004.03.032 .
- ^ a b c Мэджилл, AH; Aber, JD; Карри, WS; Надельхоффер, KJ; Мартин, ME; Макдауэлл, WH; Melillo, JM; Steudler, P. (2004). «Ответ экосистемы на 15 лет хронических добавок азота в Harvard Forest LTER, Массачусетс, США». Экология и управление лесами . 196 : 7–28. DOI : 10.1016 / j.foreco.2004.03.033 .
- ^ Лора Фостер Huenneke; Стивен П. Гамбург; Роджер Койде; Гарольд А. Муни; Питер М. Витаусек (1990). «Влияние почвенных ресурсов на инвазию растений и структуру сообщества в калифорнийских серпентиновых пастбищах». Экология . 71 (2): 478–491. DOI : 10.2307 / 1940302 . JSTOR 1940302 .
- Перейти ↑ Tilman, D. (1997). «Инвазивность сообщества, ограничение набора и биоразнообразие пастбищ». Экология . 78 : 81–83. DOI : 10,1890 / 0012-9658 (1997) 078 [0081: CIRLAG] 2.0.CO; 2 .
- ^ а б в Уилсон, SD; Тильман, Д. (2002). «Квадратичная вариация видового богатства старых полей по градиентам возмущения и азота». Экология . 83 (2): 492. DOI : 10,1890 / 0012-9658 (2002) 083 [0492: QVIOFS] 2.0.CO; 2 .
- ^ Wamelink, GWW; ван Доббен, HF; Мол-Дейкстра, JP; Шувенберг, EPAG; Kros, J .; de Vries, W .; Берендсе, Ф. (сентябрь 2009 г.). «Влияние сокращения осаждения азота на биоразнообразие и связывание углерода». Экология и управление лесами . 258 (8): 1774–1779. DOI : 10.1016 / j.foreco.2008.10.024 .
- ^ Эгертон-Уорбертон, LM; Аллен, Е.Б. (2000). «Сдвиги в сообществах Arbuscular Mycorrhizal по градиенту антропогенного отложения азота». Экологические приложения . 10 (2): 484. DOI : 10,1890 / 1051-0761 (2000) 010 [0484: SIAMCA] 2.0.CO; 2 .
- ^ Куинн Томас, R .; Canham, Charles D .; Уэзерс, Кэтлин С .; Гудейл, Кристин Л. (22 декабря 2009 г.). «Увеличение накопления углерода в деревьях в ответ на осаждение азота в США». Природа Геонауки . 3 (1): 13–17. DOI : 10.1038 / ngeo721 . ISSN 1752-0908 .
- ^ Aerts, Риен; Берендсе, Франк (август 1988). «Влияние увеличения доступности питательных веществ на динамику растительности на влажных вересковых пустошах» . Vegetatio . 76 (1–2): 63–69. DOI : 10.1007 / BF00047389 (неактивный 2021-01-16). ISSN 0042-3106 . CS1 maint: DOI неактивен с января 2021 г. ( ссылка )
- ^ Bobbink, R .; Heil, GW; Raessen, МБ (1992). «Атмосферное осаждение и процессы обмена растительного покрова в экосистемах пустоши». Загрязнение окружающей среды (Баркинг, Эссекс: 1987) . 75 (1): 29–37. DOI : 10.1016 / 0269-7491 (92) 90053-D . PMID 15092046 .
- Перейти ↑ Hastings, A. (1980). «Нарушение, сосуществование, история и конкуренция за космос». Теоретическая популяционная биология . 18 (3): 363–373. DOI : 10.1016 / 0040-5809 (80) 90059-3 .
- Перейти ↑ Driscoll, CT, GB Lawrence, AJ Bulger, TJ Butler, CS Cronan, C. Eagar, KF Lambert, GE Likens, JL Stoddard и KC Weathers. 2001. Кислотные отложения на северо-востоке Соединенных Штатов: источники и входы, экосистемные эффекты и стратегии управления . С. 180-198
- ^ Миллс, KH; Чаланчук С.М.; Аллан, ди-джей (2000). «Восстановление популяций рыб в озере 223 после экспериментального подкисления». Канадский журнал рыболовства и водных наук . 57 : 192–204. DOI : 10.1139 / f99-186 .
- ^ Филдс, Скотт (июль 2004 г.). «Глобальный азот: бесконтрольный цикл» . Перспективы гигиены окружающей среды . 112 (10): A556 – A563. DOI : 10.1289 / ehp.112-a556 . PMC 1247398 . PMID 15238298 .
- ^ Граймс, Черчилль Б. (2001). «Рыболовство и сброс реки Миссисипи». Рыболовство . 26 (8): 17–26. DOI : 10,1577 / 1548-8446 (2001) 026 <0017: FPATMR> 2.0.CO; 2 .
- ^ Skulberg, Olav M .; Кодд, Джеффри А .; Кармайкл, Уэйн В. (1984-01-01). «Токсичные сине-зеленые водоросли в Европе: растущая проблема». Амбио . 13 (4): 244–247. JSTOR 4313034 .
- ^ Смит, VH; Tilman, GD; Некола, JC (1999). «Эвтрофикация: воздействие избыточного поступления питательных веществ на пресноводные, морские и наземные экосистемы». Загрязнение окружающей среды . 100 (1–3): 179–196. DOI : 10.1016 / s0269-7491 (99) 00091-3 . PMID 15093117 .
- ^ a b c Дэвидсон, EA; Зейтцингер, С. (2006). «Загадка прогресса в исследованиях денитрификации». Экологические приложения . 16 (6): 2057–2063. DOI : 10,1890 / 1051-0761 (2006) 016 [2057: TEOPID] 2.0.CO; 2 . PMID 17205889 .
- ^ Джексон, RD; Allen-Diaz, B .; Оутс, LG; Тейт, KW (2006). «Нитрат родниковой воды увеличился с прекращением выпаса скота в калифорнийской дубовой саванне». Экосистемы . 9 (2): 254. DOI : 10.1007 / s10021-005-0166-7 . S2CID 24450808 .
- ↑ Galloway, JN; Dentener, FJ; Capone, DG; Бойер, EW; Ховарт, RW; Зейтцингер, ИП; Аснер, ГП; Кливленд, CC; Зеленый, Пенсильвания; Голландия, EA; Карл, DM; Майклс, AF; Портер, JH; Таунсенд, штат Арканзас; Vöosmarty, CJ (2004). «Циклы азота: прошлое, настоящее и будущее» (PDF) . Биогеохимия . 70 (2): 153. DOI : 10.1007 / s10533-004-0370-0 . JSTOR 4151466 . S2CID 98109580 . Архивировано из оригинального (PDF) 11 ноября 2005 г.
Дальнейшее чтение [ править ]
- Хорошо, AG; Битти, PH (2011). «Удобряющая природа: трагедия излишеств в обществе» . PLOS Биология . 9 (8): e1001124. DOI : 10.1371 / journal.pbio.1001124 . PMC 3156687 . PMID 21857803 ..
- Scarsbrook M .; Barquin J .; Грей Д. (2007). Холодноводные источники Новой Зеландии и их биоразнообразие (PDF) . Наука для сохранения . ISBN 978-0-478-14289-1. ISSN 1173-2946 .
- Olde Venterink, H .; Вассен, MJ; Verkroost, AWM; Де Руйтер, ПК (2003). «Видовое богатство – модели продуктивности различаются между N-, P- и K-ограниченными водно-болотными угодьями» (PDF) . Экология . 84 (8): 2191–2199. DOI : 10.1890 / 01-0639 . JSTOR 3450042 . Архивировано из оригинального (PDF) 03 марта 2016 года . Проверено 3 сентября 2009 .