 | |
| Имена | |
|---|---|
| Название ИЮПАК Бромид железа (II) | |
| Другие имена Бромид железа | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.029.244 |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| 2 февраля | |
| Молярная масса | 215,65 г моль -1 |
| Внешность | желто-коричневое твердое вещество |
| Плотность | 4,63 г см −3 , твердое вещество |
| Температура плавления | 684 ° C (1263 ° F, 957 K) (безводный) 27 ° C (гексагидрат) |
| Точка кипения | 934 ° С (1713 ° F, 1207 К) |
| 117 г / 100 мл | |
| Растворимость в других растворителях | ТГФ , метанол , этанол |
| + 13,600 · 10 −6 см 3 / моль | |
| Структура | |
| Ромбоэдрический , hP3 , SpaceGroup = P-3m1, No. 164 | |
| восьмигранный | |
| Опасности | |
| Основные опасности | никто |
| R-фразы (устаревшие) | R20 R36 / 37/38 |
| S-фразы (устаревшие) | S26 S36 |
| Родственные соединения | |
Другие анионы | Хлорид железа (II) |
Другие катионы | бромид железа (III) |
Родственные соединения | VBr 2 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Бромид железа (II) представляет собой неорганическое соединение с химической формулой FeBr 2 . Безводное соединение представляет собой парамагнитное твердое вещество желтого или коричневатого цвета. Известно также несколько гидратов FeBr 2 , все они представляют собой твердые вещества бледного цвета. Это обычный предшественник других соединений железа в исследовательских лабораториях, но для этого соединения не существует приложений.
Структура [ править ]
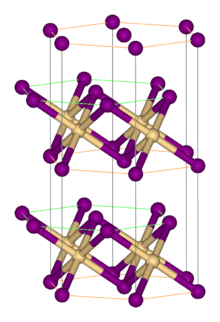
Как и большинство галогенидов металлов, FeBr 2 имеет полимерную структуру, состоящую из изолированных металлических центров, сшитых галогенидами. Он кристаллизуется со структурой CdI 2 , состоящей из плотноупакованных слоев бромид-ионов, между которыми расположены ионы Fe (II) в октаэдрических отверстиях. [1] Упаковка галогенидов немного отличается от упаковки FeCl 2 , в которой используется мотив CdCl 2 .
Синтез и реакции [ править ]
FeBr 2 синтезируется с использованием метанольного раствора концентрированной бромистоводородной кислоты и порошка железа. Он добавляет сольват метанола [Fe (MeOH) 6 ] Br 2 вместе с газообразным водородом. Нагревание метанольного комплекса в вакууме дает чистый FeBr 2 . [2]
FeBr 2 реагирует с двумя эквивалентами бромида тетраэтиламмония с образованием [(C 2 H 5 ) 4 N] 2 FeBr 4 . [3] FeBr 2 реагирует с бромидом и бромом с образованием сильно окрашенных частиц смешанной валентности [FeBr 3 Br 9 ] - . [4]
Магнетизм [ править ]
FeBr 2 обладает сильным метамагнетизмом при 4,2 К и долгое время изучался как прототип метамагнитного соединения. [5] [6]
Ссылки [ править ]
- ^ Haberecht, J .; Borrmann, Η .; Книп, Р. (2001). «Уточнение кристаллической структуры дибромида железа FeBr2» . Zeitschrift für Kristallographie - Новые кристаллические структуры . 216 (1–4). DOI : 10.1524 / ncrs.2001.216.14.544 .
- Перейти ↑ Winter, G. (1973). «Галогениды железа (II)». Неорганические синтезы . Неорганические синтезы. 14 . С. 99–104. DOI : 10.1002 / 9780470132456.ch20 . ISBN 9780470132456.
- ^ NS Gill, F .. B. Taylor Inorganic Syntheses 1967, том 9, стр. 136-142. DOI : 10.1002 / 9780470132401.ch37
- ^ Holleman, AF; Виберг, Э. "Неорганическая химия" Academic Press: Сан-Диего, 2001. ISBN 0-12-352651-5
- ^ Уилкинсон, МК; Кабель, JW; Wollan, EO; Келер, WC (15 января 1959 г.). "Нейтронографические исследования магнитного упорядочения в FeBr 2 , CoBr 2 , FeCl 2 и CoCl 2 ". Физический обзор . 113 (2): 497–507. Bibcode : 1959PhRv..113..497W . DOI : 10.1103 / PhysRev.113.497 .
- ^ Джейкобс, IS; Лоуренс, ЧП (10 декабря 1967 г.). «Метамагнитные фазовые переходы и гистерезис в FeCl 2 ». Физический обзор . 164 (2): 866–878. Bibcode : 1967PhRv..164..866J . DOI : 10.1103 / PhysRev.164.866 .