| Имена | |||
|---|---|---|---|
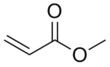
| Название ИЮПАК Метилпроп-2-еноат [1] | |||
| Другие имена | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.002.274 | ||
| КЕГГ | |||
PubChem CID | |||
| UNII | |||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 4 Н 6 О 2 | |||
| Молярная масса | 86,090 г · моль -1 | ||
| Внешность | Бесцветная жидкость | ||
| Запах | Едкий [2] | ||
| Плотность | 0,95 г / см 3 [3] | ||
| Температура плавления | -74 ° С (-101 ° F, 199 К) [3] | ||
| Точка кипения | 80 ° C (176 ° F, 353 K) [3] | ||
| 5 г / 100 мл | |||
| Давление газа | 65 мм рт. Ст. (20 ° C) [2] | ||
| Опасности | |||
| Основные опасности | Вреден (Xn); Легковоспламеняющийся (F +) | ||
| Паспорт безопасности | Оксфордский паспорт безопасности материалов | ||
| точка возгорания | -3 ° С (27 ° F, 270 К) [3] | ||
| Пределы взрываемости | 2,8–25% [2] | ||
| Смертельная доза или концентрация (LD, LC): | |||
ЛК 50 ( средняя концентрация ) | 3575 частей на миллион (мышь) 1350 частей на миллион (крыса, 4 часа) 1000 частей на миллион (крыса, 4 часа) 2522 частей на миллион (кролик, 1 час) [4] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 10 частей на миллион (35 мг / м 3 ) [кожа] [2] | ||
REL (рекомендуется) | TWA 10 частей на миллион (35 мг / м 3 ) [кожа] [2] | ||
IDLH (Непосредственная опасность) | 250 частей на миллион [2] | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Метилакрилат представляет собой органическое соединение , более точно метиловый эфир из акриловой кислоты . Это бесцветная жидкость с характерным едким запахом. В основном он производится для производства акрилатного волокна, из которого ткут синтетические ковры. [5] Это также реагент в синтезе различных фармацевтических промежуточных продуктов.
Производство [ править ]
Промышленный стандарт реакции для получения метилакрилат этерификации с метанолом в услови х кислотного катализа ( серной кислоты , п-толуолсульфоновой кислоты или кислых ионообменников. [6] ). Переэтерификация облегчается, поскольку метанол и метилакрилат образуют низкокипящий азеотроп ( точка кипения 62–63 ° C). [7]
В патентной литературе [8] описан однореакторный способ, включающий парофазное окисление пропена или 2-пропеналя кислородом в присутствии метанола.
Другие методы [ править ]
Метилакрилат можно получить дебромированием метил-2,3-дибромпропаноата цинком . [9] метилакрилат формируется в хорошем выходе на пиролиз из метила лактата в присутствии кетно (кетена). [10] Метиллакат - это возобновляемый « зеленый химикат ». Другой патент [11] описывает дегидратацию метиллактата над цеолитами .
Катализируемое тетракарбонилом никеля гидрокарбоксилирование ацетилена монооксидом углерода в присутствии метанола также дает метилакрилат. [12] Реакция метилформиата с ацетиленом в присутствии катализаторов переходных металлов также приводит к метилакрилату. [13] И алкоголиз пропиолактона метанолом, и метанолиз акрилонитрила через промежуточно образованный сульфат акриламида [14] также являются доказанными, но устаревшими процессами.
Используйте [ редактировать ]
Метилакрилат после бутилакрилата и этилакрилата является третьим по важности сложным эфиром акриловой кислоты с мировым годовым объемом производства около 200 000 тонн в год. [15]
Метилакрилат реагирует, катализируемая основаниями Льюиса в присоединении Михаэля, с аминами с высокими выходами до производных β-аланина, которые дают амфотерные поверхностно-активные вещества, когда используются длинноцепочечные амины и впоследствии гидролизуется сложноэфирная функция.
Метилакрилат используется для получения 2-диметиламиноэтилакрилата путем переэтерификации диметиламиноэтанолом в значительных количествах, превышающих 50 000 тонн / год. [16]
Метилакрилат используется в качестве сомономера при полимеризации с различными акриловыми и виниловыми мономерами . При этом он имеет такой же диапазон применения, как и этилакрилат. [17] При использовании метилакрилата в качестве сомономера получаемые акриловые краски тверже и более хрупкие, чем краски с гомологичными акрилатами. Сополимеризация метилакрилата с акрилонитрилом улучшает их способность к переработке в расплаве с получением волокон, которые могут использоваться в качестве предшественников углеродных волокон. [18]
Акрилаты также используются при получении дендримеров поли (амидоамина) (ПАМАМ), обычно путем присоединения по Михаэлю с первичным амином .
Метилакрилат является предшественником волокон, из которых ткут ковры.
Из-за тенденции к полимеризации образцы обычно содержат ингибитор, такой как гидрохинон.
Реакции [ править ]
Метилакрилат является классическим акцептором Михаэля, что означает, что он добавляет нуклеофилы на своем конце. Например, в присутствии основного катализатора он добавляет сероводород, чтобы получить тиоэфир: [19]
- 2 CH 2 CHCO 2 CH 3 + H 2 S → S (CH 2 CH 2 CO 2 CH 3 ) 2
Еще это хороший диенофил .
Безопасность [ править ]
Это острый токсин с LD 50 (крысы, перорально) 300 мг / кг и TLV 10 ppm.
Ссылки [ править ]
- ^ a b «Метилакрилат - Резюме Соединения» . PubChem . Проверено 30 июня 2012 года .
- ^ a b c d e f Карманный справочник NIOSH по химической опасности. «# 0394» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ a b c d Запись в базе данных веществ GESTIS Института безопасности и гигиены труда
- ^ "Метилакрилат" . Немедленно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ↑ Такаши Охара, Такахиса Сато, Нобору Симидзу, Гюнтер Прешер, Гельмут Швинд, Отто Вайберг, Клаус Мартен, Гельмут Грейм (2003). «Акриловая кислота и производные». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a01_161.pub2 . ISBN 3527306730.CS1 maint: использует параметр авторов ( ссылка )
- ^ «Этерификация: эфиры акрилата (MA, EA, BA, MMA, 2-EHA)» . amberlyst.com . Проверено 21 февраля 2013 .
- ^ Чесси Е. Rehberg (1955). «н-Бутилакрилат» . Органический синтез . 26:18 .; Сборник , 3 , с. 146
- ^ США 3925463 , Natale Ferlazzo, и Буцци Gian Фаусто, Ghirga Марчелло, "Способ производства метилакрилата", опубликованной 1975-12-09, назначен Societa Italiana RESINE SIR, SpA
- ^ F. Beilstein: Handbuch der organischen Chemie , 3. Auflage, 1. Band. Verlag Leopold Voss, 1893, S. 501. Volltext .
- ^ США 2417748 , Хью Дж Hagemeyer, "Получение метилакрилата", опубликованной 1947-03-18, назначен Eastman Kodak Company
- ^ США 5250729 , Takafumi Abe, Шиничи Hieda, «Способ получения ненасыщенной карбоновой кислоты или сложный эфир», переуступленном компании Mitsubishi Gas Chemical Company
- ^ W. Reppe, J. Liebigs Ann. Chem., 582 (1), 116-132 (1953)
- ^ США 6022990 , Чжао-Tie Лю Цзя Ци Чжан Сянь-Гуй Ян, «Метод синтеза метилакрилат», опубликованной 2000-02-08, назначен Чэнду Институт органической химии
- ^ Х.-Дж. Арпе, Industrielle Organische Chemie , 6. Aufl., Wiley-VCH Verlag, Weinheim, 2007, ISBN 978-3-527-31540-6 .
- ^ Отчет о маркетинговых исследованиях CEH Акриловая кислота и сложные эфиры, SRI Consulting, июль 2007 г.
- ^ 2010136696 , Жан-Мишель Поль, Борис Тоннелье, Фрэнсис Огюстен, «Состав, включающий оксид диалкилолова и его использование в качестве катализатора переэтерификации для синтеза (мет) акриловых эфиров», опубликовано 02 декабря 2010 г., передано Arkema France
- ^ DOW Метилакрилат, Оценка безопасности продукта
- ↑ VA Bhanu; и другие. (2002), "Синтез и характеристика акрилонитрила и метилакрилат статистических сополимеров в качестве предшественников в расплаве перерабатываемых углеродного волокна" (PDF) , полимерный (на немецком языке ), 43 (18), стр 4841-4850,. DOI : 10.1016 / S0032-3861 ( 02) 00330-0
- ^ Эдвард А. Fehnel и Марвин Кармак (1950). «Метил-β-дипропионат» . Органический синтез . 30 : 65.; Сборник , 4 , с. 669