 | |
| Имена | |
|---|---|
| Название ИЮПАК Сульфид никеля (II) | |
| Другие имена сульфид никеля, моносульфид никеля, сульфид никеля | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.037.113 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
Панель управления CompTox ( EPA ) | |
| |
| Характеристики | |
| NiS | |
| Молярная масса | 90,7584 г моль -1 |
| Внешность | черный твердый |
| Запах | Без запаха |
| Плотность | 5,87 г / см 3 |
| Температура плавления | 797 ° С (1467 ° F, 1070 К) |
| Точка кипения | 1388 ° С (2530 ° F, 1661 К) |
| нерастворимый | |
| Растворимость | растворим в азотной кислоте |
| + 190,0 · 10 −6 см 3 / моль | |
| Структура | |
| шестиугольный | |
| Опасности | |
| Основные опасности | может вызвать рак при вдыхании |
| Пиктограммы GHS |  |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Сульфид никеля - неорганическое соединение с формулой NiS. Это твердое вещество черного цвета, которое получают обработкой солей никеля (II) сероводородом . Известно много сульфидов никеля, в том числе минерал миллерит , который также имеет формулу NiS. Помимо полезных руд, сульфиды никеля являются продуктами реакций обессеривания и иногда используются в качестве катализаторов . Известны нестехиометрические формы сульфида никеля, например Ni 9 S 8 и Ni 3 S 2 .
Структура [ править ]
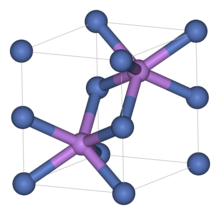
Как и многие другие родственные материалы, сульфид никеля имеет мотив арсенида никеля . В этой структуре никель октаэдрический, а сульфидные центры расположены в тригонально-призматических позициях. [1]
Сульфид никеля имеет два полиморфа . Α-фаза имеет гексагональную элементарную ячейку, а β-фаза - ромбоэдрическую ячейку. Α-фаза стабильна при температурах выше 379 ° C (714 ° F) и превращается в β-фазу при более низких температурах. Этот фазовый переход вызывает увеличение объема на 2-4%. [2] [3] [4]
Синтез [ править ]
Осаждение твердого черного сульфида никеля является основой традиционных схем качественного неорганического анализа , который начинается с разделения металлов на основе растворимости их сульфидов. Такие реакции записываются: [5]
- Ni 2+ (водн.) + H 2 S (водн.) → NiS (т.) + 2 H + (водн.)
Было разработано множество других более контролируемых методов, включая реакции метатезиса в твердом состоянии (из NiCl 2 и Na 2 S) и высокотемпературные реакции элементов. [6]
Происшествие [ править ]
Естественный [ править ]
Минерал миллерит также является сульфидом никеля с молекулярной формулой NiS, хотя его структура отличается от синтетического стехиометрического NiS из-за условий, в которых он образуется. Он встречается в естественных условиях в низкотемпературных гидротермальных системах, в полостях карбонатных пород и как побочный продукт других никелевых минералов. [7]
В производстве стекла [ править ]
Флоат-стекло содержит небольшое количество сульфида никеля, образующегося из серы в осветлителе Na.
2ТАК
4и никель, содержащийся в загрязнителях металлических сплавов. [8]
Включения сульфида никеля представляют собой проблему для закаленного стекла . После отпуска включения сульфида никеля находятся в метастабильной альфа-фазе. В конечном итоге включения переходят в бета-фазу (стабильную при низкой температуре), увеличиваясь в объеме и вызывая трещины в стекле. В середине закаленного стекла материал находится под напряжением , что вызывает распространение трещин и приводит к самопроизвольному разрушению стекла. [9] Самопроизвольное разрушение происходит спустя годы или десятилетия после производства стекла. [8]
Ссылки [ править ]
- ^ Уэллс, AF (1984) Структурная неорганическая химия, Оксфорд: Clarendon Press. ISBN 0-19-855370-6 .
- ^ Бишоп, DW; Thomas, PS; Рэй, А.С. (1998). «Рамановские спектры сульфида никеля (II)». Бюллетень материаловедения . 33 (9): 1303. DOI : 10.1016 / S0025-5408 (98) 00121-4 .
- ^ «NiS и самопроизвольный выход из строя» . Стекло в сети. Ноябрь 2012. Архивировано из оригинала на 2013-06-12.
- ^ Бонати, Антонио; Пизано, Габриэле; Ройер Карфаньи, Джанни (12 октября 2018 г.). «Статистическая модель разрушения стеклянных пластин из-за включений сульфида никеля». Журнал Американского керамического общества . DOI : 10.1111 / jace.16106 .
- ^ O.Glemser «Никель Сульфид» в Справочнике препаративной неорганической химии, 2й изд. Под редакцией Г. Брауэра, Academic Press, 1963, NY. Vol. 2. п. 1551.
- ^ основные ссылки можно найти в: Shabnam Virji, Richard B. Kaner, Bruce H. Weiller «Прямое электрическое измерение превращения ацетатов металлов в сульфиды металлов с помощью сероводорода» Inorg. Chem., 2006, 45 (26), pp 10467–10471. DOI : 10.1021 / ic0607585
- ^ Gamsjager HC, Bugajski J., Gajda T., Lemire RJ, Preis W. (2005) Химическая термодинамика никеля, Амстердам, Elsevier BV
- ^ a b Карлссон, Стефан (30 апреля 2017 г.). «Самопроизвольное разрушение термически упрочненного стекла - обзор и перспективы» . Керамика - Силикаты : 188–201. DOI : 10,13168 / cs.2017.0016 . Проверено 16 августа 2019 .
- ↑ Барри, Джон (12 января 2006 г.). "Ахиллова пята из прекрасного материала: закаленное стекло" . Стекло в сети . Проверено 16 августа 2019 .