 | |
 | |
| Имена | |
|---|---|
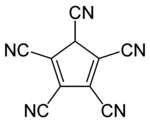
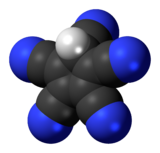
| Название ИЮПАК Циклопента-1,3-диен-1,2,3,4,5-пентакарбонитрил | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
PubChem CID | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| C 10 H N 5 | |
| Молярная масса | 191,153 г · моль -1 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Pentacyanocyclopentadiene является производным от циклопентадиена с пятью цианогрупп с молекулярной формулой С 5 Н (CN) 5 . Соответствующий анион , пентацианоциклопентадиенид , является лигандом с молекулярной формулой C
5(CN)-
5. В отличие от других анионов на основе кольцевого звена C 5, он связывается с металлами через боковые цианогруппы, а не через кольцо C 5 . Анион был впервые синтезирован Вебстером в 1960-х годах [1], а его сопряженная кислота - намного позже. [2] Совсем недавно Райт открыл его обширную координационную химию. [3] [4] В силе комбинации мезомерной и ароматической стабилизация его аниона, pentacyanocyclopentadiene является суперкислотным , с предполагаемым водным р K в -11. [5] Свободная кислота была получена Ридом в 2004 году, и ей была приписана полимерная структура с протонами, которые связывают плоский C5 (CN) 5 шт. [6]
Синтез [ править ]
Пентацианоциклопентадиен синтезируется путем сочетания дисульфида углерода и цианида натрия в диметилформамиде перед окислением с использованием персульфата аммония, а окончательная очистка дает соль пентацианоциклопентадиена аммония. Дальнейшая реакция с гидридом натрия приводит к образованию NaC 5 (CN) 5, который является отправной точкой для его координационной химии с переходными металлами.
Реакции и координационная химия [ править ]
Сочетание пентацианоциклопентадиена натрия (NaC 5 (CN) 5 ) с солями галогенидов переходных металлов приводит к образованию комплексов металлов, содержащих C
5(CN)-
5анион. [3] [4]
Поскольку анион связывается с металлами через цианидную группу, он может действовать как пентагональный узел. Таким образом, он может образовывать фуллереноподобные структуры с большими пустотами, содержащими растворитель. [7] [8] Это имеет важные последствия для хранения и разделения газа.
Ссылки [ править ]
- ^ Webster, OW (1966). «Диазотетрацианоциклопентадиен». Журнал Американского химического общества . 88 (17): 4055–4060. DOI : 10.1021 / ja00969a029 .
- Перейти ↑ Reed, C. (2004). «Исследование пентациано-циклопентадиенид-иона, C5(CN)- 5, как слабо координирующий анион и потенциальное основание конъюгата суперкислот » (PDF) . Chem. Commun .: 706. doi : 10.1039 / b316122f .
- ^ а б Райт, DS (2011). «Комплексы переходных металлов аниона пентацианоциклопентадиенида». Chem. Commun . 47 (36): 10007. DOI : 10.1039 / c1cc13021h . PMID 21833428 .
- ^ а б Райт, DS (2012). «Комплексы группы 11, содержащие лиганд [C 5 (CN) 5 ] - ;« координационные аналоги »молекулярных металлоорганических систем». Dalton Trans . 41 (19): 5919. DOI : 10.1039 / c2dt30274h . PMID 22473357 .
- ^ Джонатан, Клейден; Гривс, Ник; Уоррен, Стюарт Г. (2012). Органическая химия (2-е изд.). Оксфорд: Издательство Оксфордского университета. ISBN 9780199270293. OCLC 761379371 .
- ^ Ричардсон, Кристофер; Рид, Кристофер А. (2004). «Исследование пентациано-циклопентадиенид-иона, C5(CN)- 5, как слабо координирующий анион и потенциальное основание конъюгата суперкислотной кислоты. Силилирование и протонирование » . Chem. Commun. (6): 706–707. Doi : 10.1039 / B316122F . ISSN 1359-7345 .
- ^ Bacsa, J. (2011). «Сборка первых металлоорганических каркасов фуллеренового типа с использованием плоского пятиуровневого координационного узла». Энгью. Chem. Int. Эд . 50 (36): 8279–8282. DOI : 10.1002 / anie.201102783 .
- ^ Меньше, RJ (2013). "Растворитель направление молекулярной архитектуры в пентацианоциклопентадиенидах металлов группы 1". Евро. J. Inorg. Chem . 2013 (7): 1161–1169. DOI : 10.1002 / ejic.201201342 .