 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК рубидий (1 +); азид | |
| Другие имена Азид рубидия | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
PubChem CID | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| 3 руб. | |
| Молярная масса | 127,49 г · моль -1 |
| Внешность | Бесцветные иглы [1] |
| Плотность | 2,79 г / см 3 [1] [2] |
| Температура плавления | 317–321 ° C (603–610 ° F, 590–594 K) [2] [4] |
| Точка кипения | Разлагается |
| 107,1 г / 100 г (16 ° C) 114,1 г / 100 г (17 ° C) [3] | |
| Растворимость | 0,182 г / 100 г (16 ° C, этанол ) [3] |
| Термохимия | |
Std энтальпия формации (Δ F H ⦵ 298 ) | -0,1 ккал · моль -1 [2] |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Другие анионы | Нитрат рубидия |
Другие катионы | Азид лития Азид натрия Азид калия Азид серебра Азид аммония |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Азид рубидия представляет собой неорганическое соединение с формулой Rb N 3 . Это рубидий соль из азида иона ( Н-
3). Как и большинство азидов , он взрывоопасен. [4]
Подготовка [ править ]
Азид рубидия может быть получен в результате реакции между сульфатом рубидия и азидом бария, которая приводит к образованию легко отделяемого нерастворимого сульфата бария : [3]
По крайней мере, в одном исследовании азид рубидия был получен в результате реакции между бутилнитритом , моногидратом гидразина и гидроксидом рубидия :
Эта формула обычно используется для синтеза азида калия из едкого калия . [5]
Использует [ редактировать ]
Азид рубидия был исследован на предмет возможного использования в ячейках с паром щелочных металлов, которые являются компонентами атомных часов , атомных магнитометров и атомных гироскопов . Азиды являются желательными исходными материалами, потому что они разлагаются на металлический рубидий и газообразный азот под воздействием УФ-излучения . Согласно одной публикации:
Среди различных методов, используемых для заполнения микроизготовленных ячеек с паром щелочных металлов [sic] , УФ-разложение азида рубидия (RbN 3 ) на металлический Rb и азот в ячейках с покрытием Al 2 O 3 является очень многообещающим подходом для изготовления недорогих пластин. [6]
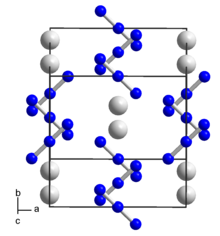
Структура [ править ]
При комнатной температуре азид рубидия имеет ту же структуру, что и фтористый водород калия ; искаженная структура хлорида цезия . При 315 ° C и 1 атм азид рубидия переходит в нормальную структуру хлорида цезия. Температура перехода II / I азида рубидия находится в пределах 2 ° C от его точки плавления. [4]
Азид рубидия имеет структурный переход под высоким давлением, который происходит при давлении около 4,8 килобар при 0 ° C. Границу перехода II / III перехода можно определить соотношением , где - давление в килобарах, а - температура в градусах Цельсия . [4]
Реакции [ править ]
Как и все азиды, он будет разлагаться и выделять газообразный азот при нагревании или сильном ударе :
Опасности [ править ]
При давлении 4,1 кбар и температуре около 460 ° C азид рубидия взрывоопасен. [4] В нормальных условиях он взрывается при температуре 395 ° C. [2] Он также разлагается под воздействием ультрафиолета . [6]
Азид рубидия очень чувствителен к механическому удару , его чувствительность к ударам сопоставима с таковой у тротила . [7]
Как и все азиды, азид рубидия токсичен.
Ссылки [ править ]
- ^ а б Перри, Дейл (1995-05-17). Справочник неорганических соединений . В сети. п. 333. ISBN 9780849386718. Проверено 31 января 2018 года .
- ^ a b c d Харт, Уильям; Beumel, OF; Уэйли, Томас (22 октября 2013 г.). Химия лития, натрия, калия, рубидия, цезия и франция: пергамские тексты по неорганической химии . Интернет: Pergamon Press. п. 438. ISBN 9781483187570. Проверено 31 января 2018 года .
- ^ a b c Хала, Иржи. «Серия данных по растворимости IUPAC-NIST. 79. Псевдогалогениды щелочных и щелочноземельных металлов» (PDF) . nist.gov . Проверено 31 января 2018 года .
- ^ a b c d e Писториус, Карл WFT (27 декабря 1968 г.). «Фазовые диаграммы для высоких давлений одновалентных азидов космической группы D 4hI8-14 / mcm» (PDF) . В сети. С. 1, 4–5 . Проверено 1 февраля 2018 .
- ^ Огден, Дж. Стивен; Дайк, Джон М .; Левасон, Уильям; Ферранте, Франческо; Гальярди, Лаура. "Характеристика молекулярных азидов щелочных металлов" (PDF) . PMID 16491492 . Проверено 2 февраля 2018 . Cite journal requires
|journal=(help) - ^ a b Карлен, Сильвен; Гобет, Жан; Оверстольц, Томас; Хеслер, Жак; Леконт, Стив (26 января 2017 г.). «Оценка срока службы заполненных RbN 3 атомно-паровых ячеек МЭМС с покрытием из Al 2 O 3 » (PDF) . Оптика Экспресс . 25 (3): 2187–2194. Bibcode : 2017OExpr..25.2187K . DOI : 10,1364 / OE.25.002187 . PMID 29519066 . Проверено 17 марта 2018 года .
- ^ Бабу, К. Рамеш; Вайтхесваран, Г. (2013). «Структура, упругие и динамические свойства KN3 и RbN3: исследование с использованием функционала плотности Ван-дер-Ваальса». Науки о твердом теле . Центр перспективных исследований высокоэнергетических материалов (ACRHEM), Хайдарабадский университет. 23 : 17–25. arXiv : 1311.0979 . Bibcode : 2013SSSci..23 ... 17R . CiteSeerX 10.1.1.768.1309 . DOI : 10.1016 / j.solidstatesciences.2013.05.017 .
| HN 3 | Он | ||||||||||||||||||
| LiN 3 | Быть (N 3 ) 2 | В (N 3 ) 3 | CH 3 N 3 , C (N 3 ) 4 | N (N 3 ) 3 , H 2 N — N 3 | О | FN 3 | Ne | ||||||||||||
| NaN 3 | Мг (N 3 ) 2 | Al (N 3 ) 3 | Si (N 3 ) 4 | п | SO 2 (N 3 ) 2 | ClN 3 | Ar | ||||||||||||
| Кн 3 | Ca (N 3 ) 2 | СБН (N 3 ) 3 | Ti (N 3 ) 4 | ВО (№ 3 ) 3 | Cr (N 3 ) 3 , CrO 2 (N 3 ) 2 | Mn (N 3 ) 2 | Fe (N 3 ) 2 , Fe (N 3 ) 3 | Co (N 3 ) 2 , Co (N 3 ) 3 | Ni (N 3 ) 2 | CuN 3 , Cu (N 3 ) 2 | Zn (N 3 ) 2 | Ga (N 3 ) 3 | Ge | В качестве | Se (N 3 ) 4 | 3 руб. | Kr | ||
| 3 руб. | Sr (N 3 ) 2 | Y | Zr (N 3 ) 4 | Nb | Пн | Tc | Ru (N 3 ) 6 3- | Rh (N 3 ) 6 3- | Pd (N 3 ) 2 | AgN 3 | Cd (N 3 ) 2 | В | Sn | Sb | Te | В 3 | Xe (N 3 ) 2 | ||
| ЦСН 3 | Ba (N 3 ) 2 | Hf | Та | W | Re | Операционные системы | Ir (N 3 ) 6 3- | Pt (N 3 ) 6 2− | Au (N 3 ) 4 - | Hg 2 (N 3 ) 2 , Hg (N 3 ) 2 | TlN 3 | Pb (N 3 ) 2 | Би (N 3 ) 3 | По | В | Rn | |||
| Пт | Ra (N 3 ) 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Ур. | Ц | Og | |||
| ↓ | |||||||||||||||||||
| Ла | Ce (N 3 ) 3 , Ce (N 3 ) 4 | Pr | Nd | Вечера | См | Европа | Gd (N 3 ) 3 | Tb | Dy | Хо | Э | Тм | Yb | Лу | |||||
| Ac | Чт | Па | UO 2 (N 3 ) 2 | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||||


![{\ displaystyle {\ ce {C4H9ONO + N2H4 * H2O + RbOH -> [{\ ce {C_2H_5OH}}] RbN3 + C4H9OH + 3H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b58511202f0feb09d210afff08dc3b6bff1bb951)



![{\ Displaystyle {\ ce {2RbN3 -> [\ Delta] 2Rb + 3N2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f46a53c26319bb5f2de53fdcc8f256ea03e6e339)