| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Толуол [1] | |||
| Систематическое название ИЮПАК Метилбензол | |||
| Другие названия Фенил метана Толуол Anisen | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| Сокращения | PhMe MePh BnH Tol | ||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.003.297 | ||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 7 Н 8 | |||
| Молярная масса | 92,141 г · моль -1 | ||
| Появление | Бесцветная жидкость [2] | ||
| Запах | сладкий, острый, бензол -как [3] | ||
| Плотность | 0,87 г / мл (20 ° C) [2] | ||
| Температура плавления | -95 ° С (-139 ° F, 178 К) [2] | ||
| Точка кипения | 111 ° С (232 ° F, 384 К) [2] | ||
| 0,52 г / л (20 ° C) [2] | |||
| журнал P | 2,68 [4] | ||
| Давление газа | 2,8 кПа (20 ° C) [3] | ||
Магнитная восприимчивость (χ) | −66,11 · 10 −6 см 3 / моль | ||
Показатель преломления ( n D ) | 1,497 (20 ° С) | ||
| Вязкость | 0,590 сП (20 ° C) | ||
| Состав | |||
Дипольный момент | 0,36 Д | ||
| Опасности | |||
| Основные опасности | легковоспламеняющиеся | ||
| Паспорт безопасности | См .: страницу данных SIRI.org | ||
| Пиктограммы GHS | |||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H225 , H361d , H304 , H373 , H315 , H336 | ||
Меры предосторожности GHS | Р210 , Р240 , Р301 + 310 , P302 + 352 , P308 + 313 , P314 , P403 + 233 | ||
| NFPA 704 (огненный алмаз) |  2 3 0 | ||
| точка возгорания | 4 ° С (39 ° F, 277 К) [2] | ||
| Пределы взрываемости | 1,1–7,1% [3] | ||
Пороговое предельное значение (ПДК) | 50 мл / м 3 , 190 мг / м 3 | ||
| Смертельная доза или концентрация (LD, LC): | |||
ЛК 50 ( средняя концентрация ) | > 26700 частей на миллион (крыса, 1 час ) 400 частей на миллион (мышь, 24 часа) [5] | ||
LC Lo ( самый низкий опубликованный ) | 55 000 частей на миллион (кролик, 40 мин) [5] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 200 ppm C 300 ppm 500 ppm (максимум 10 минут) [3] | ||
REL (рекомендуется) | TWA 100 частей на миллион (375 мг / м 3 ) ST 150 частей на миллион (560 мг / м 3 ) [3] | ||
IDLH (Непосредственная опасность) | 500 частей на миллион [3] | ||
| Родственные соединения | |||
Связанные ароматические углеводороды | бензол ксилол нафталин | ||
Родственные соединения | метилциклогексан | ||
| Страница дополнительных данных | |||
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. | ||
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ | ||
Спектральные данные | УФ , ИК , ЯМР , МС | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
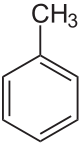
Толуол ( / т ɒ LJ у я н / ), также известный как толуол ( / т ɒ LJ U ɒ л / ), представляет собой ароматический углеводород . Это бесцветная нерастворимая в воде жидкость с запахом разбавителей для краски . Это монозамещенное производное бензола , состоящее из метильной группы (CH₃), присоединенной к фенильной группе . Таким образом, его систематическое название ИЮПАК - метилбензол.. Толуол преимущественно используется в качестве промышленного сырья и растворителя .
В качестве растворителя в некоторых типах разбавителей для красок , перманентных маркерах , контактном цементе и некоторых типах клея толуол иногда используется в качестве развлекательного ингалянта [7] и может нанести серьезный неврологический вред. [8] [9]
История [ править ]
Это соединение было впервые выделено в 1837 году путем перегонки соснового масла польским химиком Филипом Вальтером , который назвал его ретиннафтом . [10] В 1841 году французский химик Анри Этьен Сент-Клер Девиль выделил углеводород из бальзама Толу (ароматический экстракт тропического колумбийского дерева Myroxylon balsamum ), который Девиль признал похожим на ретиннафту Уолтера и бензол; отсюда он назвал новый углеводород бензоэном . [11] В 1843 году Йонс Якоб Берцелиус рекомендовал название толуин .[12] В 1850 году французский химик Огюст Каур выделил из древесного дистиллята углеводород, который он признал похожим на бензоен Девиляи который Каур назвал толуеном . [13]
Химические свойства [ править ]
Толуол реагирует как обычный ароматический углеводород при электрофильном ароматическом замещении . [14] [15] [16] Поскольку метильная группа имеет более высокие свойства высвобождения электронов, чем атом водорода в том же положении, толуол более активен по отношению к электрофилам, чем бензол . Она подвергается сульфирование с получением п - толуолсульфоновую кислоту , и хлорирование с помощью Cl 2 в присутствии FeCl 3 с получением орто- и пара - изомеров из хлортолуол .
Важно отметить, что боковая метильная цепь в толуоле подвержена окислению. Толуол реагирует с перманганатом калия с образованием бензойной кислоты и с хромилхлоридом с образованием бензальдегида ( реакция Этара ).
Метильная группа подвергается галогенированию в условиях свободных радикалов . Например, N- бромсукцинимид (NBS), нагретый с толуолом в присутствии AIBN, приводит к бензилбромиду . Такое же преобразование можно осуществить с элементарным бромом в присутствии УФ-света или даже солнечного света. Толуол также можно бромировать, обрабатывая его HBr и H 2 O 2 в присутствии света. [17]
- C 6 H 5 CH 3 + Br 2 → C 6 H 5 CH (Br) 2 + HBr
- C 6 H 5 CH 2 Br + Br 2 → C 6 H 5 CHBr 2 + HBr
Метильная группа в толуоле подвергается депротонированию только с очень сильными основаниями, ее pK a оценивается примерно в 41. [18] Полное гидрирование толуола дает метилциклогексан . Реакция требует высокого давления водорода и катализатора .
Производство [ править ]
Толуол в естественных условиях содержится в сырой нефти в небольших количествах и является побочным продуктом при производстве бензина на установке каталитического риформинга или установке крекинга этилена . Это также побочный продукт производства кокса из угля . Окончательное разделение и очистка выполняется любым из процессов дистилляции или экстракции растворителем, используемых для ароматических углеводородов БТК (бензол, толуол и изомеры ксилола).
Лабораторная подготовка [ править ]
Толуол дешево производится в промышленных масштабах. В принципе, его можно приготовить разными способами. Например, хотя бензол представляет только дидактический интерес, он реагирует с метилхлоридом в присутствии кислоты Льюиса, такой как хлорид алюминия, с образованием толуола:
- C 6 H 5 H + CH 3 Cl → C 6 H 5 CH 3 + HCl
Такие реакции осложняются полиметилированием, поскольку толуол более подвержен алкилированию, чем бензол.
Использует [ редактировать ]
Прекурсор бензола и ксилола [ править ]
Толуол в основном используется в качестве предшественника бензола путем гидродеалкилирования :
- С 6 Н 5 СН 3 + Н 2 → С 6 Н 6 + СН 4
Вторая по значению заявка связана с его диспропорционированием до смеси бензола и ксилола . [19]
Нитрация [ править ]
Нитрование толуола дает моно-, ди- и тринитротолуол, все из которых широко используются. Динитротолуол является предшественником толуолдиизоцианата , который используется при производстве пенополиуретана . Тринитротолуол - это взрывчатое вещество, обычно сокращенно ТНТ.
Окисление [ править ]
Бензойная кислота и бензальдегид производятся в промышленных масштабах путем частичного окисления толуола кислородом . Типичные катализаторы включают нафтенаты кобальта или марганца . [20]
Растворитель [ править ]
Толуол является обычным растворителем , например, для красок , разбавителей красок, силиконовых герметиков [21], многих химических реагентов , резины , типографской краски, клеев (клея), лаков , средств для кожевенной обработки и дезинфицирующих средств . [19]
Топливо [ править ]
Толуол может быть использован в качестве октанового числа в бензине топлива для двигателей внутреннего сгорания , а также топливо для реактивных двигателей . Толуол в количестве 86% по объему питал все двигатели с турбонаддувом в Формуле-1 в 1980-х годах, впервые разработанные командой Honda . Остальные 14% был «наполнитель» из н - гептана , чтобы уменьшить октановое число , чтобы удовлетворить Формулы Один ограничений на топливо. 100% толуол можно использовать в качестве топлива как для двухтактных, так и для четырехтактных двигателей ; однако из-за плотноститоплива и других факторов, топливо не испаряется легко, если оно не нагревается до 70 ° C (158 ° F). Honda решила эту проблему в своих автомобилях Формулы-1, пропустив топливопроводы через теплообменник , используя энергию воды в системе охлаждения для нагрева топлива. [22]
В Австралии в 2003 году было обнаружено, что толуол незаконно смешивался с бензином в топливных точках для продажи в качестве стандартного автомобильного топлива. Толуол не облагается акцизным налогом на топливо, в то время как другие виды топлива облагаются налогом более 40%, что обеспечивает более высокую норму прибыли для поставщиков топлива. Степень замещения толуола не определена. [23] [24]
Нишевые приложения [ править ]
В лаборатории толуол используется в качестве растворителя для углеродных наноматериалов, включая нанотрубки и фуллерены, а также его можно использовать в качестве индикатора фуллерена . Толуольный раствор C 60 имеет ярко-фиолетовый цвет. Толуол используется в качестве цемента для комплектов тонкого полистирола (путем растворения и последующего сплавления поверхностей), так как его можно очень точно наносить кистью и не содержит основной массы клея. Толуол можно использовать для разрушения красных кровяных телец с целью извлечения гемоглобина в биохимических экспериментах. Толуол также использовался в качестве хладагента из-за его хороших способностей к теплопередаче в натриевых холодных ловушках, используемых в контурах системы ядерных реакторов. Толуол также использовался в процессеудаление кокаина из листьев коки при производстве сиропа Coca-Cola. [25]
Токсикология и метаболизм [ править ]
Экологические и токсикологические эффекты толуола широко изучены. [26] В 2013 году мировые продажи толуола составили около 24,5 миллиардов долларов США. [27] Вдыхание толуола в малых и средних дозах может вызвать усталость, спутанность сознания, слабость, поведение в состоянии опьянения, потерю памяти, тошноту, потерю аппетита, потерю слуха и потерю цветового зрения. Некоторые из этих симптомов обычно исчезают после прекращения воздействия. Вдыхание большого количества толуола за короткое время может вызвать головокружение, тошноту или сонливость, потерю сознания и даже смерть . [28] [29] Толуол, однако, намного менее токсичен, чем бензол., и, как следствие, в значительной степени заменил его в качестве ароматического растворителя при химическом приготовлении. Агентство США по охране окружающей среды (EPA) утверждает , что канцерогенный потенциал толуола не может быть оценена из - за недостатка информации. [30]
Как и во многих других растворителях , таких как 1,1,1-трихлорэтан и некоторых алкильных бензолы , толуол было показано, действуют в качестве неконкурентного антагониста рецептора NMDA и ГАМК А рецептора положительного аллостерического модулятора . [31] Кроме того, было показано, что толуол проявляет антидепрессантные эффекты у грызунов в тесте принудительного плавания (FST) и тесте подвешивания за хвост (TST) [31], вероятно, из-за его свойств антагониста NMDA.
Толуол иногда используется как рекреационный ингалятор («нюхание клея»), вероятно, из-за его эйфорического и диссоциативного эффекта. [31]
Толуол подавляет возбуждающие ионные каналы, включая глутамат N-метил-D-аспартата (NMDA) и никотиновые ацетилхолиновые рецепторы (nAChR), и потенцирует функцию ингибирующих ионных каналов, таких как рецепторы гамма-аминомасляной кислоты типа A, рецепторы глицина и серотонина. Кроме того, толуол разрушает потенциал-управляемые кальциевые каналы и АТФ-управляемые ионные каналы. [32]
Рекреационное использование [ править ]
Толуол используется в качестве опьяняющего средства для ингаляции способом, не предусмотренным производителями. Люди вдыхают продукты, содержащие толуол (например, разбавитель для красок , контактный цемент , клей для моделей и т. Д.) Из-за их опьяняющего действия . Владение и использование толуола и продуктов, содержащих его, регулируются во многих юрисдикциях по той причине, что якобы не позволяют несовершеннолетним приобретать эти продукты для употребления наркотиков в развлекательных целях. По состоянию на 2007 год в 24 штатах США действовали законы, предусматривающие наказание за использование, хранение с намерением использовать и / или распространение таких ингалянтов. [33] В 2005 году Европейский Союз запретил общую продажу продуктов, содержащих более 0,5% толуола. [34]
Биовосстановление [ править ]
Несколько типов грибов, включая Cladophialophora , Exophiala , Leptodontium , Pseudeurotium zonatum и Cladosporium sphaerospermum , а также некоторые виды бактерий могут разлагать толуол, используя его в качестве источника углерода и энергии. [35]
Ссылки [ править ]
- ^ Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 139. DOI : 10.1039 / 9781849733069-00130 . ISBN 978-0-85404-182-4.
Толуол и ксилол являются предпочтительными названиями IUPAC, но не могут быть заменены свободно; толуол можно заменить при определенных условиях, но только для общей номенклатуры (см. P-15.1.8 для общих правил замены для сохраненных названий).
- ^ a b c d e f Запись в базе данных веществ GESTIS Института безопасности и гигиены труда
- ^ a b c d e f Карманный справочник NIOSH по химической опасности. «# 0619» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ "toluene_msds" .
- ^ а б «Толуол» . Немедленно опасная для жизни или здоровья концентрация (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ "NFPA Chemicals" . New Environment, Inc.
- ^ Маккеаун, Нафанаил J. (1 февраля 2015). Тарабар, Асим (ред.). «Токсичность толуола, предпосылки, патофизиология, эпидемиология» . WebMD Health Professional Network. Цитировать журнал требует
|journal=( помощь ) - ^ Streicher, HZ; Габоу, Пенсильвания; Moss, AH; Kono, D .; Kaehny, WD (1981). «Синдромы нюхания толуола у взрослых». Анналы внутренней медицины . 94 (6): 758–62. DOI : 10.7326 / 0003-4819-94-6-758 . PMID 7235417 .
- ^ Devathasan, G .; Низкий, D .; Теох, ПК; Ван, Ш; Вонг, ПК (1984). «Осложнения хронического злоупотребления клеем (толуолом) у подростков». Aust NZJ Med . 14 (1): 39–43. DOI : 10.1111 / j.1445-5994.1984.tb03583.x . PMID 6087782 .
- ^ См .:
- Пеллетье и Вальтер (1837 г.) «Examen des produits proventant du traitement de la résine dans la fabrication du gaz pour l'éclairage» (Исследование продуктов, полученных в результате обработки смолы во время производства осветительного газа), Comptes rendus , 4 : 898 –899.
- Пеллетье и Филипп Вальтер (1838) «Examen des produits Provider du traitement de la résine dans la fabrication du gaz pour l'éclairage», Annales de Chimie et de Physique , 2-я серия, 67 : 269-303. Толуол назван на стр. 278–279: «Nous désignerons la субстанция qui nous occupe par le nom de rétinnaphte , qui rappelle son origine et ses propriétés Physiques (ρητίνη-νάφτα)». (Мы будем называть вещество, которое нас занимает, именем ретиннафта , что напоминает о его происхождении и физических свойствах (ρητίνη-νάφτα [смола-нафта]).
- ^ См .:
- Девиль (1841) «Recherches sur les résines. Étude du baume de Tolu» (Исследования смол. Изучение бальзама Толу), Comptes rendus , 13 : 476–478.
- Х. Девиль (1841) «Recherches chimiques sur les résines; Premier mémoire» (Химические исследования смол; первые воспоминания), Annales de Chimie et de Physique , 3-я серия, 3 : 151-195. Девиль называет толуол на стр. 170: «J'ai accepté, pour le corps qui m'occupe dans ce moment, le nom de benzoène , qui rappelle, dans les baumes dont il provient, ce caractère presque générique qui est de contenir de l'acide benzoïque». (Я принял для этого вещества, которое меня в данный момент занимает, название бензоен , которое напоминает в бальзамах, из которых оно происходит, характер, который содержится в бензойной кислоте.)
- Висняк, Хайме (2004). "Анри Этьен Сент-Клер Девиль: врач стал металлургом". Журнал материаловедения и производительности . 13 (2): 117–118. Bibcode : 2004JMEP ... 13..117W . DOI : 10.1361 / 10599490418271 . S2CID 95058552 .
- ↑ Якоб Берцелиус (1843) Jahres Berichte , 22 : 353-354. .
- ^ См .:
- Кахур, Огюст (1850) "Recherches sur les huiles légères obtenues dans la distillation du bois" (Исследования легких масел, полученных путем перегонки древесины), Compte rendus , 30 : 319-323; см. страницу 320.
- Хайме Висняк (октябрь 2013 г.) «Огюст Андре Томас Кахур», « Educación Química» , 24 (4): 451–460.
- ^ BS Furniss et al., Учебник практической органической химии Фогеля , 5-е издание, Longman / Wiley, Нью-Йорк, 1989
- ^ LG Wade, Органическая химия , 5-е изд., Стр. 871, Prentice Hall, Upper Saddle River, Нью-Джерси, 2003 г.
- ^ Дж. Марч, Продвинутая органическая химия , 4-е изд., Стр. 723, Уайли, Нью-Йорк, 1992
- ^ Подгоршек, Айда; Ставбер, Стоян; Зупан, Марко; Искра, Ерней (2006). «Свободнорадикальное бромирование системой H2O2 – HBr на воде». Буквы тетраэдра . 47 (40): 7245. DOI : 10.1016 / j.tetlet.2006.07.109 .
- ^ Генри Се, Родерик П. Куирк. Анионная полимеризация: принципы и практическое применение . п. 41.
- ^ a b Фабри, Йорг; Грэзер, Ульрих; Симо, Томас А. (2005). "Толуол". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a27_147.pub2 .
- ^ Уэйд, Лерой Г. (2014). Органическая химия (новое международное издание Пирсона). Харлоу: Pearson Education Limited. п. 985. ISBN 978-1-292-02165-2.
- ^ «Силиконовые клеи двойного отверждения с низким содержанием растворителей, чувствительные к давлению - компания General Electric» .
- ^ Honda Формула-1 Двигатель V-6 с турбонаддувом 1,5 л (PDF) . Международный конгресс и выставка SAE. 27 февраля - 3 марта 1989 г.
- ^ «Жульничество на точечных испытаниях искр бензина» . Liberty Oil . Архивировано из оригинала 3 марта 2016 года.
- ^ «The World Today Archive - Власти еще не признали проблему с бензиновым мошенничеством» .
- ^ Мерори, Джозеф (1968). Пищевые ароматизаторы: состав, производство и использование (2-е изд.). Вестпорт, Коннектикут: AVI Publishing Company, Inc.
- ↑ Hogan, C. Michael (2011), «Сера» , в Jorgensen, A .; Кливленд, CJ (ред.), Энциклопедия Земли , Вашингтон, округ Колумбия: Национальный совет по науке и окружающей среде , получено 26 октября 2012 г. ,
Сера нерастворима в воде, но растворима в сероуглероде, частично растворима в других
неполярных
органических растворителях, таких как в качестве ароматических углеводородов бензол и толуол.
- ^ Ceresana. «Толуол - Исследование: рынок, анализ, тенденции - Ceresana» .
- ^ «Влияние толуола на здоровье» , Канадский центр гигиены и безопасности труда.
- ↑ «Физиологические эффекты токсичности толуола». Архивировано 12 октября2016 г. в Wayback Machine , Агентство по токсическим веществам и реестру заболеваний.
- ^ [1] , EPA
- ^ а б в Круз, SL; Соберанес-Чавес, П .; Páez-Martinez, N .; Лопес-Рубалькава, К. (июнь 2009 г.). «Толуол оказывает действие, подобное антидепрессанту, на двух моделях животных, используемых для скрининга антидепрессантов». Психофармакология . 204 (2): 279–86. DOI : 10.1007 / s00213-009-1462-2 . PMID 19151967 . S2CID 2235023 .
- ^ "Толуол" .
- ^ Spigel, Савл (8 июля 2009). «Государственные законы об использовании ингалянтов» .
- ^ «ЕС устанавливает 0,1% лимит на использование толуола, ТХБ» . ICIS . Деловая информация компании Reed . 24 сентября 2005 г.
- ^ Prenafeta-Boldu, Francesc X .; Кун, Андреа; Luykx, Дион МАМ; Анке, Хайдрун; van Groenestijn, Johan W .; де Бонт, Ян А.М. (апрель 2001 г.). «Выделение и характеристика грибов, растущих на летучих ароматических углеводородах в качестве единственного источника углерода и энергии» . Микологические исследования . 105 (4): 477–484. DOI : 10.1017 / S0953756201003719 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме толуола . |
| В Викицитатнике есть цитаты, связанные с: Толуол |
- ATSDR - Примеры из экологической медицины: токсичность толуола Министерство здравоохранения и социальных служб США (общественное достояние)
- Американская ассоциация промышленной гигиены , The Ear Poisons , The Synergist, ноябрь 2018 г.
- Toluene CDC - Тема безопасности и гигиены труда NIOSH (DHHS)
- OSHA-NIOSH 2018. Предотвращение потери слуха, вызванной химическими веществами (ототоксичность) и воздействием шума Информационный бюллетень по безопасности и здоровью (SHIB) , Управление по охране труда и Национальный институт охраны труда. SHIB 03-08-2018. Публикация DHHS (NIOSH) № 2018-124.