 | |
| Идентификаторы | |
|---|---|
| MeSH | Уропорфириноген + III |
PubChem CID | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| C 40 H 44 N 4 O 16 | |
| Молярная масса | 836,795 г / моль |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Уропорфириноген III является тетрапирроловым , первой макроциклическим промежуточным продуктом в биосинтезе из гема , хлорофилла , витамин B12 , и сирогем . Это бесцветное соединение, как и другие порфириногены . [1]
Структура [ править ]
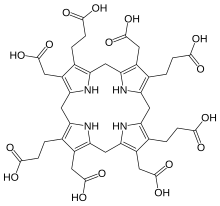
Молекулярная структура из уропорфириногена III может быть описана как hexahydroporphine ядро, где каждый пиррол кольцо имеет водородные атомы на своих два крайних атомах углерода заменен на уксусной кислоте группы ( -CH
2-COOH , «A») и группу пропионовой кислоты ( -CH
2-CH
2−COOH , «П»). Группы прикреплены асимметрично: по макроциклу порядок AP-AP-AP-PA.
Биосинтез и метаболизм [ править ]
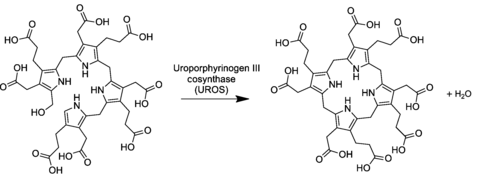
В общем пути биосинтеза порфиринов уропорфириноген III является производным линейного тетрапиррольного преуропорфириногена (замещенного гидроксиметилбилана ) под действием фермента косинтазы уропорфириноген-III . [2] [3]
Превращение влечет за собой обращение последнего пиррольного звена (таким образом, меняя местами группы уксусной и пропионовой кислот) и реакцию конденсации, которая замыкает макроцикл, удаляя конечный гидроксил -ОН с атомом водорода первого кольца.
При биосинтезе гемов и хлорофиллов уропорфириноген III превращается в копропорфириноген III под действием фермента декарбоксилазы уропорфириноген III . В биосинтезе сирогем уропорфириноген III превращается двумя метилтрансферазами в дигидрозирогидрохлорин , который впоследствии окисляется сирогидрохлорин , предшественник простетической группы сирогема .
Медицинское значение [ править ]
Если уропорфириноген-III синтаза отсутствует или неактивна, гидроксиметилбилан самопроизвольно циклизуется в структурный изомер уропорфириноген I , который отличается от изомера III тем, что группы уксусной кислоты («A») и пропионовой кислоты («P») расположены в осесимметричном порядке AP-AP-AP-AP. В этом случае на следующем этапе продуцируется копропорфириноген I , который накапливается - что приводит к патологическому состоянию врожденной эритропоэтической порфирии [3]
См. Также [ править ]
- Уропорфириноген
Ссылки [ править ]
- Перейти ↑ Dalton, J (1969). «Формирование макроциклического кольца в биосинтезе тетрапирролов». Природа . 223 (5211): 1151–1153. Bibcode : 1969Natur.223.1151D . DOI : 10.1038 / 2231151a0 . PMID 5810686 . S2CID 4177167 .
- ^ Пол Р. Ортис де Монтельяно (2008). «Гемы в биологии». Энциклопедия химической биологии Wiley . Джон Вили и сыновья. DOI : 10.1002 / 9780470048672.wecb221 . ISBN 978-0470048672.
- ^ a b С. Сасса и А. Каппас (2000): «Молекулярные аспекты наследственных порфирий». Журнал внутренней медицины , том 247, выпуск 2, страницы 169-178. DOI : 10.1046 / j.1365-2796.2000.00618.x