 | |
| Имена | |
|---|---|
| Другие названия Фторид ванадия, трифторид ванадия | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.141 |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| F 3 В | |
| Молярная масса | 107,9367 г · моль -1 |
| Появление | Желто-зеленый порошок (безводный) Зеленый порошок (тригидрат) [1] |
| Плотность | 3,363 г / см 3 [1] |
| Температура плавления | 1395 ° C (2543 ° F; 1668 K) при 760 мм рт. Ст. (Безводный) ~ 100 ° C (212 ° F, 373 K) при 760 мм рт. Ст. (Тригидрат) разлагается [1] |
| Точка кипения | Возвышенные |
| Нерастворимый [1] | |
| Растворимость | Не растворим в EtOH [1] |
| 2,757 · 10 −3 см 3 / моль [1] | |
| Состав | |
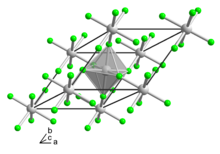
| Ромбоэдрический , hR24 [2] | |
| R 3 c, No. 167 [2] | |
| 3 2 / м [2] | |
a = 5,17 Å, c = 13,402 Å [2] α = 90 °, β = 90 °, γ = 120 ° | |
| Опасности | |
| Пиктограммы GHS |   [3] [3] |
| Сигнальное слово GHS | Опасность |
Положения об опасности GHS | H301 , H311 , H331 , H314 [3] |
Меры предосторожности GHS | P261 , P280 , P301 + 310 , P305 + 351 + 338 , P310 [3] |
| NFPA 704 (огненный алмаз) |  3 0 2 |
| Родственные соединения | |
Другие анионы | Хлорид ванадия (III) Оксид ванадия (III) Нитрид ванадия (III) |
Другие катионы | Фторид ванадия (IV) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Фторид ванадия (III) представляет собой химическое соединение с формулой V F 3 . Это желто-зеленое тугоплавкое твердое вещество получают двухстадийным способом из V 2 O 3 . [4] Подобно другим фторидам переходных металлов (таким как MnF 2 ), он демонстрирует магнитное упорядочение при низких температурах (например, V 2 F 6 .4H 2 O на порядок ниже 12 К [5] ).
Подготовка [ править ]
На первом этапе происходит преобразование в соль гексафторванадата (III) с использованием бифторида аммония :
- V 2 O 3 + 6 (NH 4 ) HF 2 → 2 (NH 4 ) 3 VF 6 + 3 H 2 O
На втором этапе гексафторованадат термически разлагается.
- (NH 4 ) 3 VF 6 → 3 NH 3 + 3 HF + VF 3
Термическое разложение солей аммония - относительно распространенный метод получения неорганических твердых веществ.
VF 3 можно также получить обработкой V 2 O 3 HF. [ необходима ссылка ] VF 3 представляет собой твердое кристаллическое вещество с 6 координированными атомами ванадия с мостиковыми атомами фтора. Магнитный момент указывает на наличие двух неспаренных электронов.
Ссылки [ править ]
- ^ a b c d e f Лиде, Дэвид Р., изд. (2009). CRC Справочник по химии и физике (90-е изд.). Бока-Ратон, Флорида : CRC Press . ISBN 978-1-4200-9084-0.
- ^ a b c d Дуглас, Боди Э .; Хо, Ши-Мин (2007). Структура и химия кристаллических твердых тел . Нью-Йорк: Springer Science + Business Media, Inc., стр. 102. ISBN 978-0-387-26147-8.
- ^ a b c Sigma-Aldrich Co. , Фторид ванадия (III) . Проверено 25 июня 2014.
- ^ Штурм, BJ; Sheridan, C.W. "Неорганический синтез фторида ванадия (III)", 1963 г .; Vol. 7, страницы 52-54. ISBN 0-88275-165-4 .
- ^ S. Nakhal et al., Z. Kristallogr. 228, 347 (2013). DOI : 10,1524 / zkri.2013.1664
- Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.