| |||
| Имена | |||
|---|---|---|---|
| Имена ИЮПАК Пентахлорид сурьмы Хлорид сурьмы (V) | |||
| Другие имена Хлорид сурьмы Хлорид сурьмы | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.729 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| Cl 5 Sb | |||
| Молярная масса | 299,01 г · моль -1 | ||
| Внешность | бесцветная или красновато-желтая (дымящая) жидкость маслянистая | ||
| Запах | острый, зловонный | ||
| Плотность | 2,336 г / см 3 (20 ° C) [1] 2,36 г / см 3 (25 ° C) [2] | ||
| Температура плавления | 2,8 ° С (37,0 ° F, 275,9 К) | ||
| Точка кипения | 140 ° C (284 ° F, 413 K) разлагается от 106 ° C [3] 79 ° C (174 ° F, 352 K) при 22 мм рт. Ст. [1] 92 ° C (198 ° F, 365 K) при 30 мм рт. [2] | ||
| реагирует | |||
| Растворимость | растворим в спирте , HCl , винной кислоте , CHCl 3 , CS 2 , CCl 4 | ||
| Растворимость в оксихлориде селена (IV) | 62,97 г / 100 г (25 ° С) | ||
| Давление газа | 0,16 кПа (25 ° C) 4 кПа (40 ° C) 7,7 кПа (100 ° C) [4] | ||
Магнитная восприимчивость (χ) | -120,0 · 10 −6 см 3 / моль | ||
Показатель преломления ( n D ) | 1,59255 | ||
| Вязкость | 2,034 сП (29,4 ° C) [1] 1,91 сП (35 ° C) | ||
| Структура | |||
Молекулярная форма | Тригональный бипирамидный | ||
Дипольный момент | 0 Д | ||
| Термохимия | |||
Теплоемкость ( C ) | 120,9 Дж / моль · К (газ) [3] | ||
Стандартная мольная энтропия ( S | 295 Дж / моль · К [3] | ||
Std энтальпия формации (Δ F H ⦵ 298 ) | -437,2 кДж / моль [3] | ||
Свободная энергия Гиббса (Δ f G ˚) | -345,35 кДж / моль [3] | ||
| Опасности | |||
| Пиктограммы GHS | [2] | ||
| Сигнальное слово GHS | Опасность | ||
Формулировки опасности GHS | H314 , H411 [2] | ||
Меры предосторожности GHS | P273 , P280 , P305 + 351 + 338 , P310 [2] | ||
| Опасность при вдыхании | Токсичный | ||
| NFPA 704 (огненный алмаз) |  0 3 1 W | ||
| точка возгорания | 77 ° С (171 ° F, 350 К) | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 1115 мг / кг (крыса, перорально) [3] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 0,5 мг / м 3 (как Sb) [5] | ||
REL (рекомендуется) | TWA 0,5 мг / м 3 (как Sb) [5] | ||
| Родственные соединения | |||
Другие анионы | Пентафторид сурьмы | ||
Другие катионы | Пентахлорид фосфора | ||
Родственные соединения | Трихлорид сурьмы | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Пентахлорид сурьмы - это химическое соединение с формулой SbCl 5 . Это бесцветное масло, но типичные образцы желтоватого цвета из-за примесей. Из-за своей склонности к гидролизу до соляной кислоты SbCl 5 является высококоррозионным веществом и должен храниться в контейнерах из стекла или ПТФЭ .
Подготовка и структура [ править ]
Пентахлорид сурьмы получают путем пропускания газообразного хлора в расплав трихлорида сурьмы :
- SbCl 3 + Cl 2 → SbCl 5
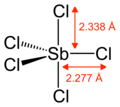
Газообразный SbCl 5 имеет тригонально-бипирамидную структуру. [6]
Реакции [ править ]
Пентахлорид сурьмы гидролизуется с образованием соляной кислоты и оксихлоридов сурьмы . Эта реакция подавляется в присутствии большого избытка хлорида из-за образования комплексного иона гексахлорантимоната :
- SbCl 5 + Cl - → [SbCl 6 ] -
Моно- и тетрагидраты известны: SbCl 5 · H 2 O и SbCl 5 · 4H 2 O.
Это соединение образует аддукты со многими основаниями Льюиса. SbCl 5 представляет собой мягкую кислоту Льюиса, и ее параметры модели ECW равны E A = 3,64 и C A = 10,42. Он используется в качестве стандартной кислоты Льюиса в шкале основности Гутмана . [7] Однако графики Крамера-Боппа показывают, что однопараметрическая шкала основности является неполной и что не существует единого порядка ранжирования базовой силы. Эти графики показывают, что для определения порядка силы основания Льюиса (или силы кислоты Льюиса) необходимо учитывать по крайней мере два свойства. [8] [9]
Это также сильный окислитель . [10]
Приложения [ править ]
Пентахлорид сурьмы используется в качестве катализатора полимеризации и для хлорирования органических соединений.
Меры предосторожности [ править ]
Пентахлорид сурьмы - очень агрессивное вещество, которое следует хранить вдали от источников тепла и влаги. Это хлорирующий агент, который в присутствии влаги выделяет газообразный хлористый водород. Из-за этого он может травить даже инструменты из нержавеющей стали (например, иглы), если обращаться с ним во влажной атмосфере. Не следует работать с нефторированными пластиками (такими как пластиковые шприцы, пластиковые перегородки или иглы с пластиковыми фитингами), так как они плавятся и обугливаются пластмассами. [11]
Ссылки [ править ]
- ^ a b c «Пентахлорид сурьмы (UK PID)» .
- ^ a b c d e Sigma-Aldrich Co. , Хлорид сурьмы (V) . Проверено 29 мая 2014.
- ^ a b c d e f "Хлорид сурьмы (V)" .
- ^ Пентахлорид сурьмы в Linstrom, Peter J .; Маллард, Уильям Г. (ред.); Веб-книга NIST Chemistry, стандартная справочная база данных NIST номер 69 , Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд), http://webbook.nist.gov (получено 29 мая 2014 г.)
- ^ a b Карманный справочник NIOSH по химической опасности. «# 0036» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- ^ В. Гутманн (1976). «Влияние растворителей на химическую активность металлоорганических соединений». Coord. Chem. Ред. 18 (2): 225–255. DOI : 10.1016 / S0010-8545 (00) 82045-7 .
- Перейти ↑ Laurence, C. and Gal, J.-F. Шкалы основности и сродства Льюиса, данные и измерения, (Wiley 2010), стр. 50-51, IBSN 978-0-470-74957-9
- ^ Крамер, RE; Бопп, TT (1977). «Графическое отображение энтальпий образования аддуктов для кислот и оснований Льюиса». Журнал химического образования . 54 : 612–613. DOI : 10.1021 / ed054p612 .На графиках, представленных в этом документе, использовались более старые параметры. Улучшенные параметры E&C перечислены в модели ECW .
- ^ Коннелли, Н.Г .; Гейгер, WE (1996). «Химические окислительно-восстановительные агенты для металлоорганической химии». Chem. Ред. 96 (2): 877–922. DOI : 10.1021 / cr940053x . PMID 11848774 .
- ^ Шекарчи, М .; Бехбахани, Ф. К. Катал. Lett. 2017 147 2950. DOI: 10.1007 / s10562-017-2194-2
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме пентахлорида сурьмы . |
| Этот материал, связанный с неорганическими соединениями, является незавершенным . Вы можете помочь Википедии, расширив ее . |