| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Трихлорид сурьмы | |||
| Систематическое название ИЮПАК Трихлорстибан | |||
| Другие имена Хлорид сурьмы (III), масло сурьмы, хлорид сурьмы, хлорид стибуса, трихлоростибин | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.030.031 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
| MeSH | Сурьма + трихлорид | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1733 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| Cl 3 Sb | |||
| Молярная масса | 228,11 г · моль -1 | ||
| Внешность | Бесцветное твердое вещество, очень гигроскопично | ||
| Запах | Острый, острый | ||
| Плотность | 3,14 г / см 3 (25 ° C) 2,51 г / см 3 (150 ° C) [1] | ||
| Температура плавления | 73,4 ° С (164,1 ° F, 346,5 К) [5] | ||
| Точка кипения | 223,5 ° С (434,3 ° F, 496,6 К) | ||
| 601,1 г / 100 мл (0 ° C) [1] 985,1 г / 100 мл (25 ° C) 1,357 кг / 100 мл (40 ° C) [2] | |||
| Растворимость | Растворим в ацетоне , этаноле , CH 2 Cl 2 , фенилах , эфире , диоксане , CS 2 , CCl 4 , CHCl 3 , циклогексане , оксихлориде селена (IV). Нерастворим в пиридине , хинолине , органических основаниях. | ||
| Растворимость в уксусной кислоте | 143,9 г / 100 г (0 ° C) 205,8 г / 100 г (10 ° C) 440,5 г / 100 г (25 ° C) [3] 693,7 г / 100 г (45 ° C) [2] | ||
| Растворимость в ацетоне | 537,6 г / 100 г (18 ° C) [2] [3] | ||
| Растворимость в бензоилхлориде | 139,2 г / 100 г (15 ° C) 169,5 г / 100 г (25 ° C) [3] 2,76 кг / 100 г (70 ° C) [2] | ||
| Растворимость в соляной кислоте | 20 ° C: 8,954 г / г (4,63% по массе ) 8,576 г / г (14,4% по массе ) 7,898 г / г (36,7% по массе) [2] | ||
| Растворимость в п-Цимене | 69,5 г / 100 г (-3,5 ° C) 85,5 г / 100 г (10 ° C) 150 г / 100 г (30 ° C) 2,17 кг / 100 г (70 ° C) [2] | ||
| Давление газа | 13,33 Па (18,1 ° C) [3] 0,15 кПа (50 ° C) 2,6 кПа (100 ° C) [4] | ||
Магнитная восприимчивость (χ) | -86,7 · 10 −6 см 3 / моль | ||
Показатель преломления ( n D ) | 1,46 [1] | ||
| Структура | |||
Кристальная структура | Орторомбический | ||
Дипольный момент | 3,93 D (20 ° C) [3] | ||
| Термохимия | |||
Теплоемкость ( C ) | 183,3 Дж / моль · К [3] | ||
Стандартная мольная энтропия ( S | 110,5 Дж / моль · К [3] | ||
Std энтальпия формации (Δ F H ⦵ 298 ) | -381,2 кДж / моль [3] | ||
Свободная энергия Гиббса (Δ f G ˚) | -322,5 кДж / моль [3] | ||
| Опасности | |||
| Паспорт безопасности | ICSC 1224 | ||
| Пиктограммы GHS | [5] | ||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H314 , H411 [5] | ||
Меры предосторожности GHS | P273 , P280 , P305 + 351 + 338 , P310 [5] | ||
| NFPA 704 (огненный алмаз) |  2 0 1 | ||
| точка возгорания | Негорючий | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 525 мг / кг (перорально, крысы) | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 0,5 мг / м 3 (как Sb) [6] | ||
REL (рекомендуется) | TWA 0,5 мг / м 3 (как Sb) [6] | ||
| Родственные соединения | |||
Другие анионы | Трифторид сурьмы Трибромид сурьмы Трииодид сурьмы | ||
Другие катионы | Треххлористый азот Треххлористый фосфор Треххлористый мышьяк Хлорид висмута | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
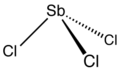
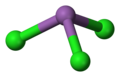
Трихлорид сурьмы - это химическое соединение с формулой SbCl 3 . Мягкое бесцветное твердое вещество с резким запахом было известно алхимикам как масло сурьмы .
Подготовка [ править ]
Сурьма трихлорид получают путем реакции хлора с сурьмой , бромид сурьмы , трехокись сурьмы или сульфид сурьмы . Его также можно получить обработкой триоксида сурьмы концентрированной соляной кислотой .
Реакции [ править ]
SbCl 3 легко гидролизуется, и образцы SbCl 3 необходимо защищать от влаги. В ограниченном количестве воды образует оксихлорид сурьмы с выделением хлористого водорода :
- SbCl 3 + H 2 O → SbOCl + 2 HCl
С большим количеством воды он образует Sb 4 O 5 Cl 2, который при нагревании до 460 ° в атмосфере аргона превращается в Sb 8 O 11 Cl 12 . [7]
SbCl 3 легко образует комплексы с галогенидами, но стехиометрия не является хорошим ориентиром для определения состава, [7] например, (C 5 H 5 NH) SbCl 4 содержит цепной анион с искаженными октаэдрами Sb III . Аналогично соль (C 4 H 9 NH 3 ) 2 SbCl 5 содержит полимерный анион состава [SbCl 5 2- ] n с искаженным октаэдрическим Sb III . [8]
С лигандами-донорами азота, L, образуются комплексы со стереохимически активной неподеленной парой, например-тригонально-бипирамидный LSbCl 3 и Ψ-октаэдрический L 2 SbCl 3 . [9]
SbCl 3 является лишь слабым основанием Льюиса [7], однако известны некоторые комплексы, например, карбонильные комплексы Fe (CO) 3 (SbCl 3 ) 2 и Ni (CO) 3 SbCl 3 . [9]
Структура [ править ]
В газовой фазе SbCl 3 имеет пирамидальную форму с углом Cl-Sb-Cl 97,2 ° и длиной связи 233 мкм. [10] В SbCl 3 каждый Sb имеет три атома Cl в 234 пм, что указывает на устойчивость молекулярного звена SbCl 3 , однако есть еще пять соседних атомов Cl, два в 346 пм, один в 361 пм и два в 374 пм . Эти восемь атомов можно рассматривать как образующие двояковую тригональную призму. Эти расстояния можно сравнить с BiCl 3, у которого есть три ближайших соседа в 250 пм, два в 324 пм и три в среднем 336 пм. Здесь следует отметить, что все восемь ближайших соседей Bi ближе, чем восемь ближайших соседей Sb, что демонстрирует тенденцию Bi принимать более высокие координационные числа.[10] [7]
Использует [ редактировать ]
SbCl 3 - это реагент для определения витамина А и родственных каротиноидов в тесте Карра-Прайса . Трихлорид сурьмы реагирует с каротиноидом с образованием синего комплекса, который можно измерить колориметрическим методом .
Трихлорид сурьмы также использовался в качестве примеси для усиления эффекта луши в абсенте . В прошлом его использовали для растворения и удаления окорочков рогов у телят, не отрезая их.
Он также используется в качестве катализатора реакций полимеризации, гидрокрекинга и хлорирования; как протрава ; и в производстве других солей сурьмы. Его раствор используют в качестве аналитического реагента для хлораля, ароматических соединений и витамина А . [11] Он имеет очень потенциал использования в качестве катализатора кислоты Льюиса в синтетической органической трансформации.
Раствор трихлорида сурьмы в жидком сероводороде является хорошим проводником, хотя его применение ограничено очень низкой температурой или высоким давлением, необходимым для того, чтобы сероводород был жидким. [12]
Ссылки в популярной культуре [ править ]
В 12-й серии третьего сезона популярной британской программы « Все существа, большие и маленькие» (адаптированной из шестой главы книги « Все мудрые и чудесные» ) несколько телят умерли после эпизода неспецифического гастроэнтерита , причина которого позже была установлена. быть проглатыванием трихлорида сурьмы, присутствующего в растворе, используемом для растворения их обрывков рогов.
Ссылки [ править ]
- ^ a b c «Трихлорид сурьмы, SbCl3» .
- ^ a b c d e f Зайделл, Атертон; Линке, Уильям Ф. (1952). Растворимость неорганических и органических соединений . Ван Ностранд.
- ^ a b c d e f g h i "Хлорид сурьмы (III)" .
- ^ Трихлорид сурьмы в Linstrom, Peter J .; Маллард, Уильям Г. (ред.); Веб-книга NIST Chemistry, стандартная справочная база данных NIST номер 69 , Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд), http://webbook.nist.gov (получено 28 мая 2014 г.)
- ^ a b c d Sigma-Aldrich Co. , Хлорид сурьмы (III) . Проверено 29 мая 2014.
- ^ a b Карманный справочник NIOSH по химическим опасностям. «# 0036» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б в г Гринвуд, Норман Н .; Эрншоу, Алан (1984). Химия элементов . Оксфорд: Pergamon Press . С. 558–571. ISBN 978-0-08-022057-4.
- ^ Зарычта, Б .; Залески, Дж. «Механизм фазовых переходов и искажениеоктаэдровSbCl 6 3- в бис ( н- бутиламмоний) пентахлорантимонате (III) (C 4 H 9 NH 3 ) 2 [SbCl 5 ]». Z. Naturforsch. В 2006 , 61 , 1101–1109. Аннотация (PDF)
- ^ a b «Сурьма: неорганическая химия» Р. Брюса Кинга Энциклопедия редактора неорганической химии Р. Брюс Кинг (1994) Джон Вили и сыновья ISBN 0-471-93620-0
- ^ a b Уэллс А.Ф. (1984) Структурная неорганическая химия, 5-е издание, стр. 879-884, Oxford Science Publications, ISBN 0-19-855370-6
- ^ Патнаик, П. Справочник по неорганическим химическим веществам . Макгроу-Хилл , 2002, ISBN 0-07-049439-8 .
- ^ Уилкинсон, Джон А. (1931). «Жидкий сероводород как реакционная среда». Химические обзоры . 8 (2): 237–250. DOI : 10.1021 / cr60030a005 . ISSN 0009-2665 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме трихлорида сурьмы . |