![Кристаллическая структура B2O3 [1]](http://upload.wikimedia.org/wikipedia/commons/thumb/d/d9/B2O3powder.JPG/440px-B2O3powder.JPG) | |
 | |
| Имена | |
|---|---|
| Другие названия оксид бора, триоксид дибора, полуторный оксид бора, оксид бора, борный ангидрид борной кислоты | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.013.751 |
| Номер ЕС |
|
| 11108 | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| В 2 О 3 | |
| Молярная масса | 69,6182 г / моль |
| Появление | белое, стекловидное твердое вещество |
| Плотность | 2,460 г / см 3 , жидкость; 2,55 г / см 3 , тригональная; |
| Температура плавления | 450 ° C (842 ° F, 723 K) (тригональная) 510 ° C (тетраэдрическая) |
| Точка кипения | 1860 ° C (3380 ° F; 2130 K), [2] сублимируется при 1500 ° C [3] |
| 1,1 г / 100 мл (10 ° C) 3,3 г / 100 мл (20 ° C) 15,7 г / 100 мл (100 ° C) | |
| Растворимость | частично растворим в метаноле |
| Кислотность (p K a ) | ~ 4 |
| -39,0 · 10 −6 см 3 / моль | |
| Термохимия | |
Теплоемкость ( C ) | 66,9 Дж / моль К |
Стандартная мольная энтропия ( S | 80,8 Дж / моль К |
Std энтальпия формации (Δ F H ⦵ 298 ) | -1254 кДж / моль |
Свободная энергия Гиббса (Δ f G ˚) | -832 кДж / моль |
| Опасности | |
| Основные опасности | Раздражающий [4] |
| Паспорт безопасности | См .: страницу данных |
| Пиктограммы GHS | |
| Сигнальное слово GHS | Опасность |
Положения об опасности GHS | H360FD |
Меры предосторожности GHS | P201 , P202 , P281 , P308 + 313 , P405 , P501 |
| NFPA 704 (огненный алмаз) |  2 0 0 |
| точка возгорания | негорючий |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 3163 мг / кг (перорально, мышь) [5] |
| NIOSH (пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 15 мг / м 3 [4] |
REL (рекомендуется) | TWA 10 мг / м 3 [4] |
IDLH (Непосредственная опасность) | 2000 мг / м 3 [4] |
| Страница дополнительных данных | |
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. |
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ |
Спектральные данные | УФ , ИК , ЯМР , МС |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Триоксид бора (или триоксид дибора ) - один из оксидов бора . Это белое стеклообразное твердое вещество с формулой B 2 O 3 . Он почти всегда имеет стекловидную (аморфную) форму; однако он может кристаллизоваться после обширного отжига (то есть при длительном нагревании).
Считается, что стекловидный оксид бора (gB 2 O 3 ) состоит из бороксольных колец, которые представляют собой шестичленные кольца, состоящие из чередующихся трехкоординатных бора и двухкоординированного кислорода. Из - за сложности построения неупорядоченных моделей при правильной плотности со многими boroxol кольцами , эта точка зрения была изначально противоречивой, но такие модели были недавно построены и свойства проявляют в хорошем согласии с экспериментом. [6] В настоящее время на основе экспериментальных и теоретических исследований [7] [8] [9] [10] [11] установлено, что доля атомов бора, принадлежащих бороксольным кольцам в стеклообразном B 2 O 3где - то между 0,73 и 0,83, 0,75 ( 3 / 4 ) , соответствующим соотношении 1: 1 между кольцами и без колец единиц. Количество бороксольных колец уменьшается в жидком состоянии с повышением температуры. [12]
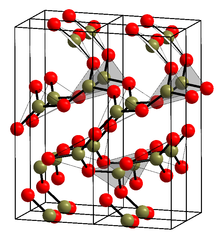
Кристаллическая форма (α-B 2 O 3 ) (см. Структуру в информационном окне [1] ) состоит исключительно из треугольников BO 3 . Эта тригональная кварцевая сетка претерпевает превращение, подобное коэситу, в моноклинный β-B 2 O 3 при нескольких гигапаскалях (9,5 ГПа). [13]
Подготовка [ править ]
Бор триоксид получают путем обработки буры с серной кислотой в слитой печи . При температурах выше 750 ° C слой расплавленного оксида бора отделяется от сульфата натрия . Затем его декантируют, охлаждают и получают с чистотой 96–97%. [3]
Другой метод - нагревание борной кислоты до температуры выше ~ 300 ° C. Борная кислота сначала разложится на пар (H 2 O (г) ) и метаборную кислоту (HBO 2 ) при температуре около 170 ° C, а дальнейшее нагревание выше 300 ° C приведет к образованию большего количества пара и триоксида дибора. Реакции следующие:
- H 3 BO 3 → HBO 2 + H 2 O
- 2 ГБО 2 → В 2 О 3 + Н 2 О
Борная кислота переходит в безводный микрокристаллический B 2 O 3 в нагретом псевдоожиженном слое. [14] Тщательно контролируемая скорость нагрева позволяет избежать образования смол при выделении воды. Расплавленный оксид бора разрушает силикаты. Внутренне графитированные трубки путем термического разложения ацетилена пассивируются. [15]
Кристаллизация расплавленного α-B 2 O 3 при атмосферном давлении сильно кинетически неблагоприятна (сравните плотности жидкости и кристаллов). Пороговые условия кристаллизации аморфного твердого вещества 10 кбар и ~ 200 ° C. [16] Предлагаемая им кристаллическая структура в энантиоморфных пространственных группах P3 1 (# 144); P3 2 (# 145) [17] [18] (например, γ-глицин) был изменен на энантиоморфные пространственные группы P3 1 21 (# 152); P3 2 21 (# 154) [19] (например, α-кварц).
Оксид бора также образуется, когда диборан (B 2 H 6 ) реагирует с кислородом воздуха или следовыми количествами влаги:
- 2B 2 H 6 (г) + 3O 2 (г) → 2B 2 O 3 (т) + 6H 2 (г)
- B 2 H 6 (г) + 3H 2 O (г) → B 2 O 3 (т) + 6H 2 (г) [20]
Приложения [ править ]
- Флюс для стекла и эмалей.
- Исходный материал для синтеза других соединений бора, таких как карбид бора.
- Добавка, используемая в стеклянных волокнах ( оптических волокнах ).
- Компонент, используемый при производстве боросиликатного стекла.
- Инертный закрывающий слой в процессе жидкостной инкапсуляции Чохральского для производства монокристалла арсенида галлия
- Как кислотный катализатор в органическом синтезе
См. Также [ править ]
- недокись бора
- борная кислота
- сассолит
- Трис (2,2,2-трифторэтил) борат
Ссылки [ править ]
- ^ a b Gurr, GE; Montgomery, PW; Knutson, CD; Горрес, БТ (1970). «Кристаллическая структура тригонального диборона триоксида». Acta Crystallographica Б . 26 (7): 906–915. DOI : 10.1107 / S0567740870003369 .
- ^ Высокотемпературная коррозия и химия материалов: материалы симпозиума памяти Пера Кофстада. Труды Электрохимического общества . Электрохимическое общество. 2000. с. 496. ISBN. 978-1-56677-261-7.
- ^ a b Патнаик, П. (2003). Справочник неорганических химических соединений . Макгроу-Хилл. п. 119. ISBN 978-0-07-049439-8. Проверено 6 июня 2009 .
- ^ a b c d Карманный справочник NIOSH по химической опасности. «# 0060» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ «Оксид бора» . Немедленно опасная для жизни или здоровья концентрация (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Ферлат, G .; Шарпантье, Т .; Seitsonen, AP; Takada, A .; Lazzeri, M .; Cormier, L .; Calas, G .; Маури. Ф. (2008). «Кольца бороксола в жидком и стекловидном B 2 O 3 из первых принципов». Phys. Rev. Lett . 101 (6): 065504. Bibcode : 2008PhRvL.101f5504F . DOI : 10.1103 / PhysRevLett.101.065504 . PMID 18764473 . ; Ferlat, G .; Seitsonen, AP; Lazzeri, M .; Маури, Ф. (2012). «Скрытые полиморфы вызывают стеклование в B 2 O 3 ». Письма о материалах природы . 11 (11): 925–929. arXiv : 1209,3482 . Bibcode : 2012NatMa..11..925F . DOI : 10.1038 / NMAT3416 . PMID 22941329 . S2CID 11567458 .
- ^ Hung, I .; и другие. (2009). «Определение межвалентного угла в стекловидном B 2 O 3 методом ротационной ЯМР-спектроскопии». Журнал химии твердого тела . 182 (9): 2402–2408. Bibcode : 2009JSSCh.182.2402H . DOI : 10.1016 / j.jssc.2009.06.025 .
- ^ Soper, AK (2011). «Кольца бороксола по дифракционным данным на стекловидном триоксиде бора» . J. Phys .: Condens. Материя . 23 (36): 365402. Bibcode : 2011JPCM ... 23.5402S . DOI : 10.1088 / 0953-8984 / 23/36/365402 . PMID 21865633 .
- ^ Джу, C .; и другие. (2000). «Кольцевая структура стекла из триоксида бора». Журнал некристаллических твердых тел . 261 (1–3): 282–286. Bibcode : 2000JNCS..261..282J . DOI : 10.1016 / s0022-3093 (99) 00609-2 .
- ^ Zwanziger, JW (2005). «ЯМР-отклик бороксольных колец: исследование теории функционала плотности». Ядерный магнитный резонанс твердого тела . 27 (1–2): 5–9. DOI : 10.1016 / j.ssnmr.2004.08.004 . PMID 15589722 .
- ^ Micoulaut, М. (1997). «Структура стекловидного B 2 O 3 получена из термостатистической модели агломерации». Журнал молекулярных жидкостей . 71 (2–3): 107–114. DOI : 10.1016 / s0167-7322 (97) 00003-2 .
- ^ Олдермен, OLG Ferlat, Г. Барони, А. Salanne, М. Micoulaut, М. Бенмор, CJ Лин, А. Tamalonis, А. Вебер, ДКР (2015). «Жидкий B2O3 до 1700K: дифракция рентгеновских лучей и растворение бороксольного кольца» (PDF) . Журнал физики: конденсированное вещество . 27 (45): 455104. DOI : 10,1088 / 0953-8984 / 27/45/455104 . PMID 26499978 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Бражкин, В.В.; Katayama, Y .; Inamura, Y .; Кондрин М.В.; Ляпин, АГ; Попова С.В.; Волошин, Р.Н. (2003). «Структурные превращения в жидком, кристаллическом и стеклообразном B 2 O 3 под высоким давлением» . Письма в ЖЭТФ . 78 (6): 393–397. Bibcode : 2003JETPL..78..393B . DOI : 10.1134 / 1.1630134 . S2CID 189764568 .
- ^ Kocakuşak, S .; Akçay, K .; Ayok, T .; Koörolu, HJ; Корал, М .; Савашчи, Ö. Т .; Толун Р. (1996). «Производство безводного кристаллического оксида бора в реакторе с псевдоожиженным слоем». Химическая инженерия и обработка . 35 (4): 311–317. DOI : 10.1016 / 0255-2701 (95) 04142-7 .
- ^ Morelock, CR (1961). "Отчет научно-исследовательской лаборатории № 61-РЛ-2672М". General Electric. Cite journal requires
|journal=(help) - ^ Азиз, MJ; Nygren, E .; Hays, JF; Тернбулл Д. (1985). «Кинетика роста кристаллов оксида бора под давлением» . Журнал прикладной физики . 57 (6): 2233. Bibcode : 1985JAP .... 57.2233A . DOI : 10.1063 / 1.334368 .
- ^ Gurr, GE; Montgomery, PW; Knutson, CD; Горрес, БТ (1970). «Кристаллическая структура тригонального диборонтриоксида». Acta Crystallographica Б . 26 (7): 906–915. DOI : 10.1107 / S0567740870003369 .
- ^ Сильный, SL; Уэллс, А.Ф .; Каплов Р. (1971). «О кристаллической структуре B 2 O 3 ». Acta Crystallographica Б . 27 (8): 1662–1663. DOI : 10.1107 / S0567740871004515 .
- ^ Effenberger, H .; Ленгауэр, CL; Парте, Э. (2001). "Тригональный B 2 O 3 с более высокой пространственно-групповой симметрией: результаты переоценки". Monatshefte für Chemie . 132 (12): 1515–1517. DOI : 10.1007 / s007060170008 . S2CID 97795834 .
- ^ AirProducts (2011). "Хранение и доставка диборана" (PDF) . Архивировано из оригинального (PDF) 04 февраля 2015 года . Проверено 21 августа 2013 . Cite journal requires
|journal=(help)
Внешние ссылки [ править ]
- Национальный кадастр загрязнителей: бор и соединения
- Информация правительства Австралии
- Информация об опасности NIH США . См. NIH .
- Паспорт безопасности материала
- CDC - Карманный справочник NIOSH по химической опасности - оксид бора