 | |
| Идентификаторы | |
|---|---|
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.331 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
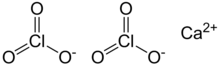
| Ca (ClO 3 ) 2 | |
| Молярная масса | 206,98 г / моль |
| Внешность | белое твердое вещество, расплывающееся |
| Запах | без запаха |
| Плотность | 2,71 г / см 3 |
| Температура плавления | 150 ° C (дигидрат, разл) 325 ° C |
| 209 г / 100 мл (20 ° C) 197 г / 100 мл (25 ° C) | |
| Структура | |
| моноклинический | |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Другие анионы | хлорид кальция бромат кальция бромид кальция |
Другие катионы | хлорат калия хлорат натрия хлорат бария хлорат магния |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Хлорат кальция является кальций солью из хлорноватой кислоты , с химической формулой Ca (ClO 3 ) 2 . Как и другие хлораты , он является сильным окислителем .
Производство [ править ]
Хлорат кальция производится путем пропускания газообразного хлора через горячую суспензию гидроксида кальция в воде с образованием гипохлорита кальция , который диспропорционирует при нагревании с избытком хлора с образованием хлората кальция и хлорида кальция : [1]
- 6 Ca (OH) 2 + 6 Cl 2 → Ca (ClO 3 ) 2 + 5 CaCl 2 + 6 H 2 O
Это также первая стадия процесса Либиха [2] для производства хлората калия .
Теоретически электролиз горячего раствора хлорида кальция дает хлорат [2], аналогично процессу, используемому для производства хлората натрия . На практике электролиз осложняется отложением гидроксида кальция на катоде , препятствующим протеканию тока.
Реакции [ править ]
При объединении концентрированных растворов хлората кальция и хлорида калия хлорат калия выпадает в осадок: [1] [3]
- Ca (ClO 3 ) 2 + 2 KCl → 2 KClO 3 + CaCl 2
Это второй этап процесса производства хлората калия по технологии Либиха. [3]
Растворы хлората кальция реагируют с растворами карбонатов щелочных металлов с образованием осадка карбоната кальция и хлората щелочного металла в растворе:
- Ca (ClO 3 ) 2 + Na 2 CO 3 → 2 NaClO 3 + CaCO 3
При сильном нагревании хлорат кальция разлагается с образованием кислорода и хлорида кальция:
- Ca (ClO 3 ) 2 → CaCl 2 + 3 O 2
Холодные разбавленные растворы хлората кальция и серной кислоты реагируют с образованием осадка сульфата кальция и хлорноватой кислоты в растворе: [4]
- Ca (ClO 3 ) 2 + H 2 SO 4 → 2 HClO 3 + CaSO 4
Контакт с сильной серной кислотой может привести к взрыву [5] из-за нестабильности концентрированной хлорноватой кислоты. Контакт с соединениями аммония также может вызвать бурное разложение из-за образования нестабильного хлората аммония . [5]
Использует [ редактировать ]
Хлорат кальция был использован в качестве гербицида , [2] , как хлорат натрия .
Хлорат кальция иногда используется в пиротехнике , [2] в качестве окислителя и розового пламени красителя. Его гигроскопичность и несовместимость с другими распространенными пиротехническими материалами (такими как сера ) ограничивают его применимость в этих приложениях.
Ссылки [ править ]
- ^ a b Сэмюэл П. Садтлер, Вирджил Кобленц и Жанно Хостманн (1918). Учебник химии, предназначенный для студентов-фармацевтов и студентов-медиков . п. 329.
- ^ a b c d Ропп, Ричард К. (2012). Энциклопедия щелочноземельных соединений . п. 80.
- ^ a b Меллор, Джозеф Уильям (1917). Современная неорганическая химия . п. 287.
- ^ Ira Remsen, Чарльз Август Rouillu (1883). «Американский химический журнал» . 4 : 309.
Раствор чистого хлората кальция, обработанный серной кислотой, конечно же, даст раствор хлорноватой кислоты.
Цитировать журнал требует|journal=( помощь ) - ^ a b PubChem - Хлорат кальция: экспериментальные свойства
