| |||
| Имена | |||
|---|---|---|---|
| Другие имена Хлорат калия (V), Potcrate | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.021.173 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1485 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
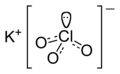
| KClO 3 | |||
| Молярная масса | 122,55 г моль -1 | ||
| Внешность | белые кристаллы или порошок | ||
| Плотность | 2,32 г / см 3 | ||
| Температура плавления | 356 ° С (673 ° F, 629 К) | ||
| Точка кипения | 400 ° C (752 ° F, 673 K) разлагается [1] | ||
| 3,13 г / 100 мл (0 ° C) 4,46 г / 100 мл (10 ° C) 8,15 г / 100 мл (25 ° C) 13,21 г / 100 мл (40 ° C) 53,51 г / 100 мл (100 ° C) 183 г / 100 г (190 ° C) 2930 г / 100 г (330 ° C) [2] | |||
| Растворимость | растворим в глицерине, незначительно в ацетоне и жидком аммиаке [1] | ||
| Растворимость в глицерине | 1 г / 100 г (20 ° C) [1] | ||
| −42,8 · 10 −6 см 3 / моль | |||
Показатель преломления ( n D ) | 1,40835 | ||
| Структура | |||
| моноклинический | |||
| Термохимия | |||
Теплоемкость ( C ) | 100,25 Дж / моль · К [1] | ||
Стандартная мольная энтропия ( S | 142,97 Дж / моль · К [3] [1] | ||
Std энтальпия формации (Δ F H ⦵ 298 ) | -391,2 кДж / моль [3] [1] | ||
Свободная энергия Гиббса (Δ f G ˚) | -289,9 кДж / моль [1] | ||
| Опасности | |||
| Паспорт безопасности | ICSC 0548 | ||
| Пиктограммы GHS | [4] | ||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | Н271 , H302 , H332 , H411 [4] | ||
Меры предосторожности GHS | P220 , P273 [4] | ||
| NFPA 704 (огненный алмаз) |  2 0 3 OX | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 1870 мг / кг (перорально, крыса) [5] | ||
| Родственные соединения | |||
Другие анионы | Бромат калия Йодат калия Нитрат калия | ||
Другие катионы | Хлорат аммония Хлорат натрия Хлорат бария | ||
Родственные соединения | Хлорид калия Гипохлорит калия Хлорит калия Перхлорат калия | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Хлорат калия - это соединение, содержащее калий , хлор и кислород , с молекулярной формулой KClO 3 . В чистом виде это белое кристаллическое вещество. Это наиболее часто используемый в промышленности хлорат . Это используется,
- как окислитель ,
- приготовить кислород ,
- как дезинфицирующее средство ,
- в матчах безопасности ,
- во взрывчатых веществах и фейерверках ,
- при выращивании , форсируя стадию цветения лонган , заставляя его плодоносить в более теплом климате. [6]
Производство [ править ]
В промышленных масштабах хлорат калия производится по технологии Либиха: хлор вводится в горячий гидроксид кальция с последующим добавлением хлорида калия : [7]
- 6 Ca (OH) 2 + 6 Cl 2 → Ca (ClO 3 ) 2 + 5 CaCl 2 + 6 H 2 O
- Ca (ClO 3 ) 2 + 2 KCl → 2 KClO 3 + CaCl 2
Электролиз из KCl в водном растворе, также иногда используется, в котором элементарный хлор образуется на аноде реагирует с KOH на месте . Низкая растворимость KClO 3 в воде приводит к тому, что соль удобно выделяется из реакционной смеси путем простого осаждения из раствора.
Хлорат калия может быть произведен в небольших количествах путем диспропорционирования в растворе гипохлорита натрия с последующей реакцией метатезиса с хлоридом калия: [8]
- 3 NaOCl (водн.) → 2 NaCl (s) + NaClO 3 (водн.)
- KCl (водн.) + NaClO 3 (водн.) → NaCl (водн.) + KClO 3 (т.)
Его также можно получить, пропуская газообразный хлор в горячий раствор едкого калия: [9]
- 3 Cl 2 (г) + 6 КОН (водн.) → KClO 3 (водн.) + 5 KCl (водн.) + 3 H 2 O (л)
Использует [ редактировать ]
Хлорат калия был одним из ключевых ингредиентов ударных капсюлей (капсюлей) раннего огнестрельного оружия . Он продолжается в том приложении, где его не вытеснил перхлорат калия .
Пропелленты на основе хлоратов более эффективны, чем традиционный порох, и менее подвержены повреждению водой. Однако они могут быть крайне нестабильными в присутствии серы или фосфора и намного дороже. Хлоратные пропелленты должны использоваться только в предназначенном для них оборудовании; Несоблюдение этой меры предосторожности является частым источником несчастных случаев. Хлорат калия, часто в сочетании с гремучим серебром , используется в хитрых шумогенераторах, известных как «крекеры», «люцианы», «хлопушки» или «хлопки», популярные типы новинок фейерверков.
Другое применение хлората калия - это окислитель в составе дыма, например, в дымовых гранатах . С 2005 года картридж с хлоратом калия, смешанным с лактозой и канифолью , используется для создания белого дыма, сигнализирующего об избрании нового Папы Папским конклавом . [10]
Хлорат калия часто используется в лабораториях средней школы и колледжа для генерации газообразного кислорода. [ необходима цитата ] Это намного более дешевый источник, чем кислородный баллон под давлением или криогенный кислородный баллон. Хлорат калия легко разлагается при нагревании при контакте с катализатором , обычно с диоксидом марганца (IV) (MnO 2 ). Таким образом, его можно просто поместить в пробирку и нагреть над горелкой. Если пробирка оснащена пробкой с одним отверстием и шлангом, можно отводить теплый кислород. Реакция следующая:
- 2 KClO 3 (т) → 3 O 2 (г) + 2 KCl (т)
Нагревание в отсутствие катализатора превращает его в перхлорат калия : [9]
- 4 KClO 3 → 3 KClO 4 + KCl
При дальнейшем нагревании перхлорат калия разлагается на хлорид калия и кислород:
- KClO 4 → KCl + 2 O 2
Для безопасного проведения этой реакции требуются очень чистые реагенты и тщательный контроль температуры. Расплавленный хлорат калия является чрезвычайно мощным окислителем и самопроизвольно вступает в реакцию со многими распространенными материалами, такими как сахар. Взрывы произошли в результате разбрызгивания жидких хлоратов на латексные или поливинилхлоридные трубки кислородных генераторов, а также в результате контакта хлоратов с углеводородными герметизирующими смазками. Примеси в самом хлорате калия также могут вызывать проблемы. При работе с новой партией хлората калия рекомендуется взять небольшой образец (~ 1 грамм) и сильно нагреть его на открытой стеклянной пластине. Загрязнение может вызвать взрыв этого небольшого количества, указывая на то, что хлорат следует выбросить.
Хлорат калия используется в химических генераторах кислорода (также называемых хлоратными свечами или кислородными свечами), используемых в качестве систем подачи кислорода, например, самолетов, космических станций и подводных лодок, и был ответственен по крайней мере за одну авиакатастрофу . Возгорание на космической станции " Мир" также связано с этим веществом. Разложение хлората калия также использовалось для снабжения кислородом прожекторов .
Хлорат калия используется также как пестицид . В Финляндии он продавался под торговой маркой Fegabit.
Хлорат калия может реагировать с серной кислотой с образованием высокореакционного раствора хлорноватой кислоты и сульфата калия:
- 2 KClO 3 + H 2 SO 4 → 2 HClO 3 + K 2 SO 4
Полученный таким образом раствор является достаточно реактивным, поэтому он самовоспламеняется, если присутствует горючий материал (сахар, бумага и т. Д.).
В школах, расплавленный хлорат калия используется в драматических кричащих желе младенцев , Gummy медведь , Haribo и Тролли конфеты демонстрации , где конфеты опускают в расплавленную соль.
В химических лабораториях он используется для окисления HCl и выделения небольших количеств газообразного хлора.
Повстанцы в Афганистане также широко используют хлорат калия в качестве ключевого компонента при производстве самодельных взрывных устройств . Когда были предприняты значительные усилия по сокращению доступности удобрений на основе нитрата аммония в Афганистане, производители СВУ начали использовать хлорат калия в качестве дешевой и эффективной альтернативы. В 2013 году 60% СВУ в Афганистане использовали хлорат калия, что делает его наиболее распространенным ингредиентом СВУ. [11] Хлорат калия также был основным ингредиентом заминированного автомобиля, использованного во время взрывов на Бали в 2002 году, в результате которых погибли 202 человека.
Безопасность [ править ]
С хлоратом калия следует обращаться осторожно. Он бурно реагирует, а в некоторых случаях самопроизвольно воспламеняется или взрывается при смешивании со многими горючими материалами. Он активно горит в сочетании практически с любыми горючими материалами, даже с теми, которые обычно легко воспламеняются (включая обычную пыль и ворсинки). Смеси хлората калия и топлива могут воспламениться при контакте с серной кислотой, поэтому их следует хранить вдали от этого реагента. Следует избегать серы в пиротехнических композициях, содержащих хлорат калия, так как эти смеси склонны к самопроизвольной дефлаграции.. Большая часть серы содержит следовые количества серосодержащих кислот, и они могут вызвать самовоспламенение - «Цветы серы» или «сублимированная сера», несмотря на общую высокую чистоту, содержат значительное количество серных кислот. Кроме того, смеси хлората калия с любыми соединениями, способствующими воспламенению (например, сульфид сурьмы (III) ), очень опасны в приготовлении, поскольку они чрезвычайно чувствительны к ударам.
См. Также [ править ]
- Хлорная кислота
Ссылки [ править ]
- ^ a b c d e f g "хлорат калия" . Дата обращения 9 июля 2015 .
- ^ Seidell, Atherton; Линке, Уильям Ф. (1952). Растворимость неорганических и органических соединений . Ван Ностранд . Проверено 29 мая 2014 .
- ^ a b Zumdahl, Стивен С. (2009). Химические принципы 6-е изд . Компания Houghton Mifflin. п. A22. ISBN 0-618-94690-X.
- ^ a b c «Хлорат калия» . Дата обращения 9 июля 2015 .
- ^ Майкл Чемберс. «ChemIDplus - 3811-04-9 - VKJKEPKFPUWCAS-UHFFFAOYSA-M - Хлорат калия - Поиск похожих структур, синонимов, формул, ссылок на ресурсы и другой химической информации» . Дата обращения 9 июля 2015 .
- ^ Manochai, P .; Sruamsiri, P .; Wiriya-onkorn, W .; Naphrom, D .; Hegele, M .; Бэнгерт, Ф. (12 февраля 2005 г.). «Круглогодичная индукция цветения в межсезонье у деревьев лонган (Dimocarpus longan, Lour.) С помощью применения KClO3: возможности и проблемы» . Scientia Horticulturae . Департамент садоводства, Университет Маэджо, Чиангмай, Таиланд; Департамент садоводства, Университет Чиангмая, Чиангмай, Таиланд; Институт специальных культур и физиологии сельскохозяйственных культур, Университет Хоэнхайма, 70593 Штутгарт, Германия. 104 (4): 379–390. DOI : 10.1016 / j.scienta.2005.01.004 . Проверено 28 ноября 2010 года .CS1 maint: location ( ссылка )
- ^ Реми, Г. Курс неорганической химиию, т. 1 / Перевод с немецкого под ред. А. В. Новосёловой. Москва: Мир, 1972. - с. 770 // (перевод :) Генрих Реми. Lehrbuch der anorganischen Chemie. XI Auflage. Группа 1. Лейпциг: Geest & Portig K.-G., 1960.
- ^ Anne Marie Helmenstine, Ph.D. «Формула синтеза (заменителя) хлората калия» . About.com Education . Дата обращения 9 июля 2015 .
- ^ а б Прадёт Патнаик. Справочник неорганических химикатов . Макгроу-Хилл, 2002, ISBN 0-07-049439-8
- ↑ Дэниел Дж. Уэйкин и Алан Коуэлл (13 марта 2013 г.). «В новом раунде голосования нет имени Папы» . Нью-Йорк Таймс . Проверено 13 марта 2013 года .
- ^ "Афганские производители бомб переходят на новые взрывчатые вещества для СВУ" . USAToday.com. 25 июня 2013 . Проверено 25 июня 2013 .
- "Хлорат калия. Хлорат натрия", Fichexicol. № 217 , Париж: Национальный институт исследований и безопасности, 2000. 4 стр.
- Непрерывный процесс производства хлората калия путем сочетания с установкой по производству хлората натрия.
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме хлората калия . |