 | |
-nitrate-trihydrate-sample.jpg/440px-Copper(II)-nitrate-trihydrate-sample.jpg) | |
| Имена | |
|---|---|
| Название ИЮПАК Нитрат меди (II) | |
| Другие имена Нитрат меди | |
| Идентификаторы | |
| |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.019.853 |
PubChem CID | |
| Номер RTECS |
|
| UNII |
|
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| Cu (NO 3 ) 2 | |
| Молярная масса | 187,5558 г / моль (безводный) 241,60 г / моль (тригидрат) 232,591 г / моль (гемипентагидрат) |
| Внешность | синие кристаллы гигроскопичны |
| Плотность | 3,05 г / см 3 (безводный) 2,32 г / см 3 (тригидрат) 2,07 г / см 3 (гексагидрат) |
| Температура плавления | 114 ° C (237 ° F, 387 K) (безводный, разлагается) 114,5 ° C (тригидрат) 26,4 ° C (гексагидрат, разлагается) |
| Точка кипения | 170 ° С (338 ° F, 443 К) (тригидрат, разлагается) |
| тригидрат: [1] 381 г / 100 мл (40 ° C) 666 г / 100 мл (80 ° C) гексагидрат: [1] 243,7 г / 100 мл (80 ° C) | |
| Растворимость | гидраты хорошо растворимы в этаноле , аммиаке , воде ; не растворим в этилацетате |
| + 1570,0 · 10 −6 см 3 / моль (~ 3H 2 O) | |
| Структура | |
| орторомбический (безводный) ромбоэдрический (гидраты) | |
| Опасности | |
| Основные опасности | Раздражитель, Окислитель |
| Паспорт безопасности | Cu (NO 3 ) 2 · 3H 2 O |
| NFPA 704 (огненный алмаз) |  0 1 3 OX |
| NIOSH (пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 1 мг / м 3 (как Cu) [2] |
REL (рекомендуется) | TWA 1 мг / м 3 (как Cu) [2] |
IDLH (Непосредственная опасность) | TWA 100 мг / м 3 (как Cu) [2] |
| Родственные соединения | |
Другие анионы | Сульфат меди (II) Хлорид меди (II) |
Другие катионы | Нитрат никеля (II) Нитрат цинка |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Нитрат меди (II) , Cu ( NO 3 ) 2 , представляет собой неорганическое соединение, которое образует голубое кристаллическое твердое вещество . Безводный нитрат меди образует темно-сине-зеленые кристаллы и сублимируется в вакууме при 150-200 ° C. [3] Нитрат меди также представлен в виде пяти различных гидратов , наиболее распространенными из которых являются гемипентагидрат и тригидрат.
Синтез и реакции нитрата меди [ править ]
Гидратированный нитрат меди может быть получен путем гидратации безводного материала или путем обработки металлической меди с водным раствором из нитрата серебра или концентрированной азотной кислоты : [4]
- Cu + 4 HNO 3 → Cu (NO 3 ) 2 + 2 H 2 O + 2 NO 2
Безводная Cu (NO 3 ) 2 образуется при обработке металлической меди N 2 O 4 :
- Cu + 2 N 2 O 4 → Cu (NO 3 ) 2 + 2 NO
Попытка дегидратации любого из гидратированных нитратов меди (II) путем нагревания вместо этого дает оксиды, а не Cu (NO 3 ) 2 . При 80 ° C гидраты превращаются в «основной нитрат меди» (Cu 2 (NO 3 ) (OH) 3 ), который превращается в CuO при 180 ° C. [4] Используя эту реакционную способность, нитрат меди можно использовать для производства азотной кислоты , нагревая ее до разложения и пропуская пары непосредственно в воду. Этот метод аналогичен последнему этапу процесса Оствальда . Уравнения следующие:
- 2 Cu (NO 3 ) 2 → 2 CuO + 4 NO 2 + O 2
- 3НО 2 + Н 2 О → 2 ННО 3 + НЕТ
Природные основные нитраты меди включают редкие минералы герхардтит и руаит , которые являются полиморфами вещества Cu 2 (NO 3 ) (OH) 3 . [5] [6] [7] Гораздо более сложной, основной, гидратированной и содержащей хлориды природной солью является бутгенбахит . [8] [7]
Структура [ править ]
Безводный нитрат меди (II) [ править ]
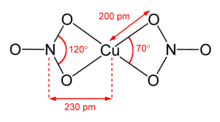
Безводные меди нитрата (II) , была кристаллизует в двух сольватных -свободных полиморфах . [9] [10] α- и β-Cu (NO 3 ) 2 представляют собой полностью трехмерные координационные полимерные сети. Альфа-форма имеет только одно окружение Cu с координацией [4 + 1], но бета-форма имеет два разных медных центра, один с [4 + 1] и один квадратно-плоский. Сольват нитрометана также имеет «[4+ 1] координацию» с четырьмя короткими связями Cu-O приблизительно 200 мкм и одной более длинной связью при 240 мкм. [11] Это координационные полимеры., с бесконечными цепочками центров меди (II) и нитратных групп. В газовой фазе нитрат меди (II) содержит два бидентатных нитратных лиганда (см. Изображение вверху справа). [12] Таким образом, испарение твердого вещества влечет за собой « растрескивание » с образованием молекулы нитрата меди (II).
Гидратированный нитрат меди (II) [ править ]
Сообщалось о пяти гидратах : моногидрат (Cu (NO 3 ) 2 · H 2 O), [10] полуторный гидрат (Cu (NO 3 ) 2 · 1,5H 2 O), [13] гемипентагидрат (Cu (NO 3 ) 2 · 2,5H 2 O), [14] тригидрат (Cu (NO 3 ) 2 · 3H 2 O), [15] и гексагидрат ([Cu (H 2 O) 6 ] (NO 3 ) 2 ). [16] Гексагидрат интересен тем, что все расстояния Cu-O равны, не обнаруживая обычного эффекта ян-теллеровского искажения, который в остальном характерен для октаэдрических комплексов Cu (II). Это отсутствие эффекта объясняется сильной водородной связью, которая ограничивает эластичность связей Cu-O.
Приложения [ править ]
Нитрат меди (II) находит множество применений, главным из которых является его преобразование в оксид меди (II) , который используется в качестве катализатора для множества процессов в органической химии . Его растворы используются в текстиле и полировальных средствах для других металлов. Нитраты меди содержатся в некоторых пиротехнических средствах . [4] Его часто используют в школьных лабораториях для демонстрации химических реакций гальванических элементов . Он входит в состав некоторых керамических глазурей и металлических патин.
Органический синтез [ править ]
Нитрат меди в сочетании с уксусным ангидридом является эффективным реагентом для нитрования ароматических соединений, известного как нитрование Менке в честь голландского химика, который обнаружил, что нитраты металлов являются эффективными реагентами для нитрования. [17] Гидратированный нитрат меди, адсорбированный на глине, дает реагент под названием «Claycop». Полученная глина синего цвета используется в виде суспензии, например, для окисления тиолов до дисульфидов . Claycop также используется для преобразования дитиоацеталей в карбонилы. [18] Соответствующий реагент на основе монтмориллонита оказался полезным для нитрования ароматических соединений.[19]
| Викискладе есть медиафайлы по теме нитрата меди (II) . |
Ссылки [ править ]
- ^ a b Справочник Perrys 'Chem Eng, 7-е изд.
- ^ a b c Карманный справочник NIOSH по химической опасности. «# 0150» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Пасс и Сатклифф (1968). Практическая неорганическая химия . Лондон: Чепмен и Холл.
- ^ a b c Х. Уэйн Ричардсон «Соединения меди» Энциклопедия промышленной химии Ульмана 2005, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a07_567 .
- ^ https://www.mindat.org/min-1680.html
- ^ http://www.mindat.org/min-10588.html
- ^ а б https://www.ima-mineralogy.org/Minlist.htm
- ^ https://www.mindat.org/min-811.html
- ^ Wallwork, SC; Аддисон, WE (1965). «Кристаллические структуры безводных нитратов и их комплексов. Часть I. α-форма нитрата меди (II)». J. Chem. Soc . 1965 : 2925–2933. DOI : 10.1039 / JR9650002925 .
- ^ а б Троянов С.И. Морозов И.В.; Знаменков, КО; Ю; Коренев, М. (1995). «Синтез и рентгеновская структура новых нитратов меди (II): Cu (NO 3 ) 2 · H 2 O и β-модификация Cu (NO 3 ) 2 ». Z. Anorg. Allg. Chem . 621 : 1261–1265. DOI : 10.1002 / zaac.19956210727 .
- ^ Даффин, B .; Wallwork, SC (1966). «Кристаллическая структура безводных нитратов и их комплексов. II. Нитрат-нитрометановый комплекс меди (II), 1: 1» . Acta Crystallographica . 20 (2): 210–213. DOI : 10.1107 / S0365110X66000434 .
- ^ ЛаВилла, RE; Бауэр, Ш. (1963). «Структура газообразного нитрата меди (II), определенная методом дифракции электронов». Варенье. Chem. Soc . 85 (22): 3597–3600. DOI : 10.1021 / ja00905a015 .
- ^ Dornberger-Schiff, K .; Leciejewicz, J. (1958). "Zur Struktur не дез Kupfernitrates Cu (NO 3 ) 2 . 1,5Н 2 О" . Acta Crystallogr . 11 : 825–826. DOI : 10.1107 / S0365110X58002322 .
- ^ Morosin, В. (1970). «Кристаллическая структура Cu (NO 3 ) 2 .2.5H 2 O». Acta Crystallogr . B26 : 1203–1208. DOI : 10.1107 / S0567740870003898 .
- ^ J. Гараж, сборник Prac. Chem.-Technol. Фак. Svst., Cskosl. 1966. С. 35–39.
- ^ Zibaseresht, R .; Хартсхорн, RM (2006). «Динитрат гексааквакоппера (II): отсутствие искажения Яна-Теллера». Acta Crystallogr . E62 : I19-I22. DOI : 10.1107 / S1600536805041851 .
- ^ Menke JB (1925). «Нитрование нитратами». Recueil des Travaux Chimiques des Pays-Bas . 44 : 141. DOI : 10.1002 / recl.19250440209 .
- ^ Балог, М. «Нитрат меди (II) - бентонитовая глина K10» в Энциклопедии реагентов для органического синтеза (Эд: Л. Пакетт) 2004, J. Wiley & Sons, Нью-Йорк. DOI : 10.1002 / 047084289X .
- Перейти ↑ Collet, Christine (1990). «Прямое ароматическое нитрование глин». Angewandte Chemie International Edition на английском языке . 29 (5): 535–536. DOI : 10.1002 / anie.199005351 .
Внешние ссылки [ править ]
- Национальный кадастр загрязнителей - Информационный бюллетень по меди и соединениям
- Информационный бюллетень ICSC по меди и соединениям
| HNO 3 | Он | ||||||||||||||||
| LiNO 3 | Быть (NO 3 ) 2 | B (НЕТ3)- 4 | RONO 2 | НЕТ- 3 NH 4 NO 3 | HOONO 2 | FNO 3 | Ne | ||||||||||
| NaNO 3 | Mg (NO 3 ) 2 | Al (NO 3 ) 3 | Si | п | S | ClONO 2 | Ar | ||||||||||
| KNO 3 | Ca (NO 3 ) 2 | СБН (№ 3 ) 3 | Ti (NO 3 ) 4 | VO (NO 3 ) 3 | Cr (NO 3 ) 3 | Mn (NO 3 ) 2 | Fe (NO 3 ) 2 Fe (NO 3 ) 3 | Co (NO 3 ) 2 Co (NO 3 ) 3 | Ni (NO 3 ) 2 | CuNO 3 Cu (NO 3 ) 2 | Zn (NO 3 ) 2 | Ga (NO 3 ) 3 | Ge | В качестве | Se | Br | Kr |
| RbNO 3 | Sr (NO 3 ) 2 | Д (НЕТ 3 ) 3 | Zr (NO 3 ) 4 | Nb | Пн | Tc | Ru (NO 3 ) 3 | Rh (NO 3 ) 3 | Pd (NO 3 ) 2 Pd (NO 3 ) 4 | AgNO 3 Ag (NO 3 ) 2 | Cd (NO 3 ) 2 | В (NO 3 ) 3 | Sn | Сб (NO 3 ) 3 | Te | INO 3 | Xe (NO 3 ) 2 |
| CsNO 3 | Ba (NO 3 ) 2 | Hf (NO 3 ) 4 | Та | W | Re | Операционные системы | Ir | Pt (NO 3 ) 2 Pt (NO 3 ) 4 | Au (NO 3 ) 3 | Hg 2 (NO 3 ) 2 Hg (NO 3 ) 2 | TlNO 3 Tl (NO 3 ) 3 | Pb (NO 3 ) 2 | Би (NO 3 ) 3 BiO (NO 3 ) | Po (NO 3 ) 4 | В | Rn | |
| Пт № 3 | Ра (NO 3 ) 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og | |
| ↓ | |||||||||||||||||
| Ла (NO 3 ) 3 | Ce (NO 3 ) 3 Ce (NO 3 ) 4 | Pr (NO 3 ) 3 | Nd (NO 3 ) 3 | PM (NO 3 ) 3 | См (NO 3 ) 3 | Eu (NO 3 ) 3 | Б-г (NO 3 ) 3 | Tb (NO 3 ) 3 | Dy (NO 3 ) 3 | Хо (нет 3 ) 3 | Er (NO 3 ) 3 | Тм (№ 3 ) 3 | Yb (NO 3 ) 3 | Лу (NO 3 ) 3 | |||
| Ac (NO 3 ) 3 | Чт (NO 3 ) 4 | PaO 2 (NO 3 ) 3 | UO 2 (NO 3 ) 2 | Np (NO 3 ) 4 | Pu (NO 3 ) 4 | Am (NO 3 ) 3 | См (NO 3 ) 3 | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||