 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Lunesta, Eszop, другие |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a605009 |
| Данные лицензии | |
| Пути администрирования | Внутрь ( таблетки ) |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетические данные | |
| Связывание с белками | 52–59% |
| Метаболизм | Окисление и деметилирование печени ( опосредованное CYP3A4 и CYP2E1 ) |
| Ликвидация Период полураспада | 6 часов |
| Экскреция | Почка |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ |
|
| ЧЭБИ |
|
| ЧЭМБЛ |
|
| Панель управления CompTox ( EPA ) |
|
| ECHA InfoCard | 100.149.304 |
| Химические и физические данные | |
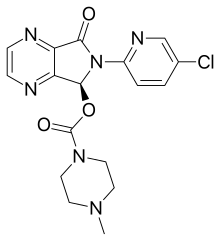
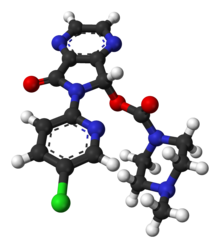
| Формула | C 17 H 17 Cl N 6 O 3 |
| Молярная масса | 388,81 г · моль -1 |
| 3D модель ( JSmol ) |
|
Улыбки
| |
ИнЧИ
| |
| (проверять) | |
Эсзопиклон , продаваемый, среди прочего, под торговой маркой Lunesta , представляет собой лекарство, используемое для лечения бессонницы . [2] Доказательства подтверждают улучшение от незначительного до умеренного в течение периода до шести месяцев. [3] [2] [4] Принимается внутрь. [3]
Общие побочные эффекты включают головную боль, сухость во рту , тошноту и головокружение. [3] Тяжелые побочные эффекты могут включать суицидальные мысли , жестокое обращение, галлюцинации и ангионевротический отек . [3] Более тщательный уход рекомендуется людям с проблемами печени и пожилым людям. [3] Быстрое снижение дозы может привести к отмене. [3] Эзопиклон классифицируется как небензодиазепиновый седативный снотворный и циклопирролон . [5] Это S- стереоизомера из зопиклона . [3]Он работает, взаимодействуя с рецепторами ГАМК . [5]
Эзопиклон, одобренный для медицинского применения в США в 2004 году, доступен в виде дженериков . [3] В 2017 году это было 214-е место среди наиболее часто назначаемых лекарств в Соединенных Штатах: было выписано более двух миллионов рецептов. [6] [7] Эсзопиклон не продается в Европейском Союзе , поскольку в 2009 году EMA постановило, что он слишком похож на зопиклон, чтобы считаться новым патентоспособным продуктом. [8] [9]
Медицинское использование [ править ]
Кокрановский обзор 2018 года показал, что он дает умеренное улучшение наступления и поддержания сна. Авторы предполагают, что там, где предпочтительные немедикаментозные стратегии лечения исчерпаны, эзопиклон обеспечивает эффективное лечение бессонницы. [10] В 2014 году USFDA попросило снизить начальную дозу с 2 миллиграммов до 1 миллиграмма после того, как в исследовании было обнаружено, что даже через 8 часов после приема препарата в ночное время некоторые люди не могли справиться с их следующим. дневные занятия, такие как вождение автомобиля и другие действия, требующие полной бдительности. [11]
Эзопиклон немного эффективен при лечении бессонницы, когда проблема с засыпанием является основной жалобой. [2] Кирш и др. обнаружили, что преимущество перед плацебо имеет сомнительное клиническое значение. [2] Хотя эффект препарата и ответ на плацебо были довольно незначительными и сомнительной клинической значимостью, они вместе дают достаточно большой клинический ответ. [2] Не рекомендуется для хронического применения пожилыми людьми. [12]
Пожилые [ править ]
Седативные снотворные препараты, включая эзопиклон, чаще назначают пожилым людям, чем более молодым пациентам, несмотря на то, что их преимущества обычно не впечатляют. Следует соблюдать осторожность при выборе подходящего снотворного, и если лекарственная терапия начата, ее следует начинать с минимально возможной дозы, чтобы минимизировать побочные эффекты. [13]
В 2015 году Американское гериатрическое общество проанализировало информацию о безопасности эзопиклона и аналогичных препаратов и пришло к выводу, что «небензодиазепиновые снотворные, агонисты бензодиазепиновых рецепторов (эзопиклон, залеплон , золпидем ) следует избегать без учета продолжительности использования из-за их связи с вредом. сбалансированы с их минимальной эффективностью при лечении бессонницы ».
В обзоре было сделано это определение как из-за относительно большой опасности для пожилых людей от золпидема и других «z-препаратов», так и из-за того факта, что эти препараты обладают «минимальной эффективностью при лечении бессонницы». Это было изменение по сравнению с рекомендацией AGS 2012 года, в которой предлагалось ограничить использование до 90 дней или меньше. В обзоре говорилось: «предостережение относительно 90-дневного использования [было] снято с небензодиазепиновых снотворных, агонистов бензодиазепиновых рецепторов, что привело к недвусмысленному заявлению« избегать »(без оговорок) из-за увеличения доказательств вреда в этой области после Обновление 2012 г. " [14]
Обширный обзор медицинской литературы, посвященной лечению бессонницы и пожилых людей, показал, что существуют убедительные доказательства эффективности и долговечности немедикаментозных методов лечения бессонницы у взрослых всех возрастов и что эти вмешательства используются недостаточно. По сравнению с бензодиазепинами небензодиазепиновые седативно-снотворные средства, включая эзопиклон, по-видимому, не давали значительных клинических преимуществ по эффективности или переносимости у пожилых людей, если таковые были. Было обнаружено, что новые агенты с новыми механизмами действия и улучшенными профилями безопасности, такие как агонисты рецепторов мелатонина, многообещающе для лечения хронической бессонницы у пожилых людей. Долгосрочное использование седативных и снотворных средств при бессоннице не имеет доказательной базы и традиционно не рекомендуется по причинам, которые включают опасения по поводу таких потенциальных побочных эффектов лекарств, как когнитивные нарушения ( антероградная амнезия ), дневная седация, нарушение координации движений и повышенный риск движения автотранспорта. аварии и падения. Кроме того, еще предстоит определить эффективность и безопасность длительного использования этих агентов. Был сделан вывод о том, что необходимы дополнительные исследования для оценки долгосрочных эффектов лечения и наиболее подходящей стратегии ведения пожилых людей с хронической бессонницей. [15]
Мета-анализ 2009 года выявил более высокий уровень инфицирования . [16]
Побочные эффекты [ править ]
Снотворные, в том числе эзопиклон, связаны с повышенным риском смерти. [17]
Повышенная чувствительность к эзопиклону является противопоказанием к его применению. Некоторые побочные эффекты встречаются чаще, чем другие. Рекомендации по применению эзопиклона могут быть изменены другими состояниями здоровья. Эти условия или обстоятельства могут возникать у людей с пониженным метаболизмом и другими состояниями. При определении частоты и дозировки можно учитывать наличие нарушения функции печени, период лактации и деятельность, требующую умственной активности (например, вождение). [5]
- неприятный вкус [5]
- головная боль [5]
- периферические отеки [5] [18]
- боль в груди [5]
- ненормальное мышление [5]
- изменения поведения [5]
- депрессия [5] [18]
- галлюцинации [5] [18]
- вождение во сне [5] и лунатизм
- сухость во рту [5]
- сыпь [5] [18]
- измененный режим сна [5]
- нарушение координации [5]
- головокружение [5]
- дневная сонливость [5]
- зуд [18]
- болезненное или частое мочеиспускание [18]
- боль в спине [18]
- агрессивное поведение [18]
- путаница [18]
- агитация [18]
- суицидальные мысли [18]
- обезличивание [18]
- амнезия [18]
Метаанализ 2009 года обнаружил , что у людей, принимающих эзопиклон или другие снотворные препараты, на 44% выше частота легких инфекций , таких как фарингит или синусит , по сравнению с теми, кто принимает плацебо. [19]
Зависимость [ править ]
В Соединенных Штатах эзопиклон является контролируемым веществом из Списка IV согласно Закону о контролируемых веществах . Использование эзопиклона может привести к физической и психологической зависимости. [5] [20] Риск злоупотребления и зависимости увеличивается с дозой и продолжительностью использования и одновременным употреблением других психоактивных препаратов. Риск также выше у пациентов с историей злоупотребления алкоголем или другими наркотиками или с историей психических расстройств. Переносимость может развиться после многократного применения бензодиазепинов и бензодиазепиноподобных препаратов в течение нескольких недель.
Исследование, финансируемое и проведенное Sepracor, не обнаружило признаков толерантности или зависимости в группе пациентов, наблюдаемых в течение шести месяцев. [20]
Нарушение [ править ]
Исследование потенциала злоупотребления эзопиклоном показало, что у лиц с известным анамнезом злоупотребления бензодиазепинами эзопиклон в дозах 6 и 12 мг оказывал влияние, аналогичное эффектам 20 мг диазепама . Исследование показало, что при этих дозах, которые в два или более раз превышают максимальные рекомендуемые дозы, дозозависимое увеличение количества сообщений об амнезии, седативном действии, сонливости и галлюцинациях наблюдалось как для эзопиклона (Lunesta), так и для диазепама ( Валиум ). [18]
Передозировка [ править ]
Согласно информации о назначении в США, сообщалось о передозировках эзопиклона, в 90 раз превышающих рекомендуемую, при которых пациент полностью выздоровел. Согласно выпуску официальной информации о назначении лекарств США за май 2014 г. , смертельные случаи были зарегистрированы только в тех случаях, когда эзопиклон сочетался с другими наркотиками или алкоголем. [21]
Центры по борьбе с отравлениями сообщили, что в период с 2005 по 2006 год в штате Техас было зарегистрировано 525 случаев полной передозировки эзопиклона , большинство из которых были намеренными попытками самоубийства . [22]
При приеме в течение последнего часа передозировку эзопиклона можно лечить с помощью активированного угля или промывания желудка . [23]
Взаимодействия [ править ]
При приеме эзопиклона вместе с другими депрессантами ЦНС, включая антипсихотики , седативные снотворные (например, барбитураты или бензодиазепины), антигистаминные препараты , опиоиды , фенотиазины и некоторые антидепрессанты, повышается риск депрессии центральной нервной системы . Также повышается риск угнетения центральной нервной системы при приеме других лекарств, которые подавляют метаболическую активность ферментной системы CYP3A4 в печени . Лекарства, которые ингибируют эту ферментную систему, включают нелфинавир , ритонавир , кетоконазол ,итраконазол и кларитромицин . Алкоголь также имеет аддитивный эффект при одновременном применении с эзопиклоном. [5] Эзопиклон наиболее эффективен, если его не принимать после тяжелой еды с высоким содержанием жира. [5]
Фармакология [ править ]
Эзопиклон действует на сайт связывания бензодиазепина, расположенный на нейронах ГАМК А, как положительный аллостерический модулятор . [24] Эзопиклон быстро всасывается после перорального приема с пиком в сыворотке между 0,45 и 1,3 часа. [25] [5] Период полувыведения эзопиклона составляет примерно 6 часов, и он интенсивно метаболизируется путем окисления и деметилирования. Примерно от 52% до 59% дозы слабо связывается с белками плазмы. Изоферменты цитохрома P450 (CYP) CYP3A4 и CYP2E1участвуют в биотрансформации эзопиклона; таким образом, препараты, которые индуцируют или ингибируют эти изоферменты CYP, могут влиять на метаболизм эзопиклона. Менее 10% принятой перорально дозы выводится с мочой в виде рацемического зопиклона. [26] С точки зрения связывания бензодиазепиновых рецепторов и соответствующей активности 3 мг эзопиклона эквивалентны 10 мг диазепама . [27]
История [ править ]
В скандальной статье 2009 г. в Медицинском журнале Новой Англии, «Потерянная передача - информация о лекарствах FDA, которая никогда не доходит до клиницистов», сообщалось, что в самом крупном из трех исследований Lunesta было обнаружено, что по сравнению с плацебо Lunesta «превосходит плацебо», хотя в среднем только на 15 минут сокращает время начального засыпания . «Клиницисты, интересующиеся эффективностью препарата, не могут найти информацию об эффективности на этикетке: там указано только, что Lunesta превосходит плацебо. Медицинский обзор FDA предоставляет данные об эффективности, хотя и не раньше, чем на 306 странице 403-страничного документа. В крупнейшем исследовании фазы 3 пациенты в группе Lunesta сообщали, что засыпали в среднем на 15 минут быстрее и спали в среднем на 37 минут дольше, чем пациенты в группе плацебо. Однако в среднемПациенты Lunesta по-прежнему соответствовали критериям бессонницы и не сообщали об клинически значимом улучшении активности или функционирования на следующий день ».[28]
Доступность в Европе [ править ]
11 сентября 2007 года Sepracor подписала маркетинговое соглашение с британской фармацевтической компанией GlaxoSmithKline на право продажи эзопиклона (под названием Lunivia, а не Lunesta) в Европе . [29] Ожидалось, что Sepracor получит около 155 миллионов долларов, если сделка состоится. [29] В 2008 году Sepracor подал заявку в EMA (эквивалент Европейского союза FDA США ) на получение разрешения на продажу препарата в ЕС и сначала получил положительный ответ. [30]Однако Sepracor отозвала свою заявку на разрешение в 2009 году после того, как EMA заявило, что не будет предоставлять эзопиклону статус «нового активного вещества», поскольку он по сути фармакологически и терапевтически слишком похож на зопиклон, чтобы считаться новым патентоспособным продуктом. [31] Поскольку срок действия патента на зопиклон истек, это постановление позволило бы конкурирующим компаниям также законно производить более дешевые генерические версии эзопиклона для европейского рынка. [32] По состоянию на ноябрь 2012 [Обновить]года Sepracor не подавал повторно заявку на авторизацию, и эзопиклон недоступен в Европе. Сделка с GSK сорвалась, и вместо этого GSK заключила сделку на 3,3 миллиарда долларов по продаже Actelion'sСнотворная таблетка альморексанта , от которой до разработки вошли в фазу 3 медицинских испытаний, отказались из-за побочных эффектов. [ необходима цитата ]
Ссылки [ править ]
- ^ Международная рабочая группа ВОЗ по методологии статистики лекарственных средств (27 августа 2008 г.). «Классификация ATC / DDD (ФИНАЛЬНАЯ): Новые коды пятого уровня ATC» . Сотрудничающий центр ВОЗ по методологии статистики лекарственных средств. Архивировано из оригинала на 2008-05-06 . Проверено 5 сентября 2008 .
- ^ a b c d e Уэдо-Медина, ТБ; Кирш, я; Мидлмасс, Дж; Клонизакис, М; Сиривардена, АН (17 декабря 2012 г.). «Эффективность небензодиазепиновых снотворных в лечении бессонницы у взрослых: метаанализ данных, представленных в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов» . BMJ (под ред. Клинических исследований) . 345 : e8343. DOI : 10.1136 / bmj.e8343 . PMC 3544552 . PMID 23248080 .
- ^ a b c d e f g h "Монография Eszopiclone для профессионалов" . Drugs.com . Американское общество фармацевтов систем здравоохранения . Проверено 6 апреля 2019 .
- ^ Rösner, S; Englbrecht, C; Wehrle, R; Hajak, G; Сойка, М. (10 октября 2018 г.). «Эзопиклон от бессонницы» . Кокрановская база данных систематических обзоров . 10 : CD010703. DOI : 10.1002 / 14651858.CD010703.pub2 . PMC 6492503 . PMID 30303519 .
- ^ Б с д е е г ч я J к л м п о р а Q R сек т у V «Eszopiclone» (PDF) . Ф.А. Дэвис. 2017 . Проверено 15 апреля 2017 года .
- ^ «Топ 300 2020» . ClinCalc . Проверено 11 апреля 2020 .
- ^ «Эзопиклон - Статистика употребления наркотиков» . ClinCalc . Проверено 11 апреля 2020 .
- ^ «Конец сделки Sepracor-GSK поднимает вопрос в патентной борьбе Lunesta» . www.cbsnews.com . 13 июня 2009 . Дата обращения 7 апреля 2019 .
- ^ «Сепракор Фармасьютикалз Лтд отзывает заявку на регистрацию препарата Лунивия (эзопиклон)» . Европейское агентство по лекарственным средствам . 15 июня 2009 . Дата обращения 7 апреля 2019 .
- ^ Рёснер, Сюзанна; Englbrecht, Christian; Верле, Ренате; Хаяк, Горан; Сойка, Михаил (10 октября 2018 г.). «Эзопиклон от бессонницы» . Кокрановская база данных систематических обзоров . 10 : CD010703. DOI : 10.1002 / 14651858.CD010703.pub2 . PMC 6492503 . PMID 30303519 .
- ^ «US FDA снижает начальную дозу эзопиклона с 2 мг до 1 мг» .
- ^ Эксперт по обновлению критериев пивоварения Американского гериатрического общества 2012 г., Группа экспертов (апрель 2012 г.). «Американское гериатрическое общество обновило Критерии Пива для потенциально несоответствующего использования лекарств пожилыми людьми» . Журнал Американского гериатрического общества . 60 (4): 616–31. DOI : 10.1111 / j.1532-5415.2012.03923.x . PMC 3571677 . PMID 22376048 .
- ^ Тарик SH, Pulisetty S (февраль 2008). «Фармакотерапия бессонницы». Clin Geriatr Med . 24 (1): 93–105, vii. DOI : 10.1016 / j.cger.2007.08.009 . PMID 18035234 .
- ^ Фик ДЙ , семл Т. П., Бейзер Дж, Брандт Н (2015). «Американское гериатрическое общество, 2015 г. обновило критерии Пива для потенциально несоответствующего использования лекарств у пожилых людей» (PDF) . Журнал Американского гериатрического общества . 63 (11): 2227–2246. DOI : 10.1111 / jgs.13702 . PMID 26446832 . S2CID 38797655 .
- ↑ Bain KT (июнь 2006 г.). «Управление хронической бессонницей у пожилых людей». Am J Geriatr Pharmacother . 4 (2): 168–92. DOI : 10.1016 / j.amjopharm.2006.06.006 . PMID 16860264 .
- ^ Джоя FL, Крипке DF, Любя RT, Dawson A (2009). «Мета-анализ снотворных и инфекций: эзопиклон, рамелтеон, залеплон и золпидем» . J. Clin. Sleep Med . 5 (4): 377–83. DOI : 10,5664 / jcsm.27552 . PMC 2725260 . PMID 19968019 .
- Перейти ↑ Kripke, DF (февраль 2016 г.). «Риск смерти от снотворных: сильные стороны и ограничения доказательств» (PDF) . Безопасность лекарств . 39 (2): 93–107. DOI : 10.1007 / s40264-015-0362-0 . PMID 26563222 . S2CID 7946506 .
- ^ a b c d e f g h i j k l m n Rxlist (26 октября 2016 г.). «Люнеста» . Архивировано из оригинала 5 декабря 2008 года . Проверено 15 апреля 2017 года .
- ^ Джойя, Флорида; Крипке, Д.Ф .; Любящий, RT; Доусон, А; Клайн, Л. Е. (2009). «Мета-анализ снотворных и инфекций: эзопиклон, рамелтеон, залеплон и золпидем» . Журнал клинической медицины сна . 5 (4): 377–383. DOI : 10,5664 / jcsm.27552 . PMC 2725260 . PMID 19968019 .
- ^ a b Brielmaier BD (январь 2006 г.). «Эзопиклон (Лунеста): новый небензодиазепиновый снотворный агент» . Proc (Bayl Univ Med Cent) . 19 (1): 54–9. DOI : 10.1080 / 08998280.2006.11928127 . PMC 1325284 . PMID 16424933 .
- ^ «Информация о назначении Lunesta в Drugs @ FDA» (PDF) . Проверено 22 мая 2014 .
- ^ Forrester MB (октябрь 2007 г.). «Сообщения о приеме внутрь эзопиклона в токсикологические центры Техаса, 2005–2006 гг.». Hum Exp Toxicol . 26 (10): 795–800. DOI : 10.1177 / 0960327107084045 . PMID 18025051 . S2CID 25102558 .
- ^ "Передозировка зопиклона" . MHRA . Агентство по регулированию лекарственных средств и товаров медицинского назначения. Архивировано 6 декабря 2014 года.CS1 maint: bot: исходный статус URL неизвестен ( ссылка ) (Из архива 6 декабря 2014 г.)
- ^ Jufe GS (июль-август 2007). «[Новые снотворные: перспективы из физиологии сна]». Вершина . 18 (74): 294–9. PMID 18265473 .
- ^ Halas CJ (1 января 2006). «Эсзопиклон». Am J Health Syst Pharm . 63 (1): 41–8. DOI : 10,2146 / ajhp050357 . PMID 16373464 .
- ^ Наджиб J (апрель 2006 г.). «Эзопиклон, небензодиазепиновый седативно-снотворное средство для лечения преходящей и хронической бессонницы». Clin Ther . 28 (4): 491–516. DOI : 10.1016 / j.clinthera.2006.04.014 . PMID 16750462 .
- ^ Профессор Эштон (апрель 2007 г.). «ТАБЛИЦА ЭКВИВАЛЕНТНОСТИ БЕНЗОДИАЗЕПИНА» . Проверено 21 марта 2008 года .
- ^ Шварц, Лиза М .; Стивен Волошин (октябрь 2009 г.). «Потеря передачи - информация о лекарствах FDA, которая никогда не доходит до врачей» . Медицинский журнал Новой Англии . NEJM.org. 361 (18): 1717–1720. DOI : 10.1056 / NEJMp0907708 . PMID 19846841 . Архивировано из оригинала (онлайн) 27.10.2010 . Проверено 6 декабря 2010 .
- ^ a b «GlaxoSmithKline и Sepracor Inc. объявляют о международном альянсе для коммерциализации Lunivia» . Архивировано из оригинального 27 декабря 2010 года.
- ^ КОМИТЕТ ПО ЛЕКАРСТВЕННЫМ ПРОДУКТАМ ДЛЯ ЧЕЛОВЕКА РЕЗЮМЕ ПОЛОЖИТЕЛЬНОГО МНЕНИЯ по LUNIVIA - Европейское агентство по лекарственным средствам / Комитет по лекарственным препаратам для человека , 23 октября 2010 г.
- ^ Sepracor Pharmaceuticals Ltd отзывает свою заявку на получение разрешения на продажу Lunivia (эзопиклон) - Европейское агентство по лекарственным средствам , 15 мая 2009 г.
- ^ Эксклюзивность данных и определение нового активного вещества: приостановление действия генерических препаратов, содержащих эсциталопрам, в соответствии с CHMP - Законом о птице и птицах от 23 апреля 2010 г.
Внешние ссылки [ править ]
- «Эсзопиклон» . Информационный портал о наркотиках . Национальная медицинская библиотека США.