 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Jyseleca |
| Другие имена | GLPG0634, GS-6034 [1] |
| Данные лицензии | |
| Пути администрирования | Устно |
| Класс препарата | Ингибитор янус-киназы |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетические данные | |
| Ликвидация Период полураспада | 6 часов [4] |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| Лиганд PDB | |
| Панель управления CompTox ( EPA ) | |
| Химические и физические данные | |
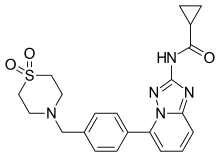
| Формула | C 21 H 23 N 5 O 3 S |
| Молярная масса | 425,51 г · моль -1 |
| 3D модель ( JSmol ) |
|
Улыбки
| |
ИнЧИ
| |
| | |
Филготиниб , продаваемый под торговой маркой Jyseleca , представляет собой лекарство, используемое для лечения ревматоидного артрита (РА). [3] Он был разработан бельгийской - голландской биотехнологической компанией Galapagos NV . [5]
Наиболее частые побочные эффекты включают тошноту (плохое самочувствие), инфекцию верхних дыхательных путей (инфекцию носа и горла), инфекцию мочевыводящих путей и головокружение. [3]
Филготиниб был одобрен для медицинского применения как в Европейском союзе, так и в Японии в сентябре 2020 года. [3] [5] [6]
Медицинское использование [ править ]
Филготиниб показан для лечения активного ревматоидного артрита от умеренной до тяжелой степени у взрослых, которые неадекватно ответили на один или несколько модифицирующих заболевание противоревматических препаратов (DMARD) или которые не переносят его. [3] Филготиниб можно использовать в качестве монотерапии или в комбинации с метотрексатом (МТ). [3]
Механизм действия [ править ]
Филготиниб является ингибитором киназы Янус с селективностью в отношении подтипа JAK1 этого фермента. Он считается многообещающим агентом, поскольку он избирательно ингибирует JAK1, подобно уже продаваемому на рынке упадацитинибу . [ требуется медицинская ссылка ] Менее селективные ингибиторы JAK (например, тофацитиниб и барицитиниб ) уже продаются. [ требуется медицинская ссылка ] Они показывают долгосрочную эффективность при лечении различных воспалительных заболеваний. [ необходима медицинская ссылка ] Однако их недостаточная избирательность приводит к ограничивающим дозу побочным эффектам. [4]Считается, что ингибирование всех изоферментов JAK полезно при ревматоидном артрите. [ требуется медицинская ссылка ] Однако ингибирование пан-JAK может также привести к нежелательным побочным эффектам, которые не могут перевесить его преимущества. [ необходима медицинская цитата ] Это основание для разработки новых и более селективных ингибиторов, таких как филготиниб. [ требуется медицинская цитата ]
Передача сигнала большого количества провоспалительных цитокинов зависит от JAK1. [ требуется медицинская ссылка ] Ингибирование JAK2 может также способствовать эффективности против ревматоидного артрита. [ требуется медицинская ссылка ] Тем не менее, считается, что ингибирование JAK2 может привести к анемии и тромбопении за счет воздействия на эритропоэтин и тромбопоэтин и фактор, стимулирующий колонию гранулоцитов-макрофагов . [ требуется медицинская цитата ]Следовательно, можно предпочесть выбор более селективного ингибитора JAK1 в качестве основного терапевтического варианта. [ требуется медицинская ссылка ] Филготиниб обладает 30-кратной селективностью в отношении JAK1 по сравнению с JAK2. [7] Однако еще предстоит увидеть, до какой степени следует избегать ингибирования JAK2. [ требуется медицинская цитата ]
Хронология [ править ]
- Июнь 2011: результаты первого исследования фазы II.
- Ноябрь 2014 г .: начало испытаний DARWIN 1 и 2
- Июль 2015: опубликованы результаты DARWIN 1
- Август 2015: опубликованы результаты испытаний DARWIN 2
- Сентябрь 2015 г .: AbbVie отказалась от сотрудничества с Galapagos [8]
- Декабрь 2015 г .: Галапагосские острова подписали соглашение о партнерстве с Gilead для совместной разработки и коммерциализации филготиниба для лечения различных заболеваний.
- Декабрь 2019 г .: Gilead подала заявку на новый лекарственный препарат (NDA) с ваучером на приоритетное рассмотрение в Управление по контролю за продуктами и лекарствами США (FDA) для филготиниба. [9]
- 23 июля 2020 года Комитет по лекарственным средствам для человека (CHMP) Европейского агентства по лекарственным средствам (EMA) принял положительное заключение, рекомендуя выдачу разрешения на продажу лекарственного препарата Jyseleca, предназначенного для лечения ревматоидного артрита. [10] Заявителем данного лекарственного препарата является Gilead Sciences Ireland UC. [10] [11] [12]
- 19 августа 2020 г .: FDA отклоняет заявку компании Gilead на одобрение филготиниба из-за опасений по поводу токсичности [13]
- Сентябрь 2020 г .: Филготиниб был одобрен для медицинского применения как в Европейском союзе, так и в Японии. [3] [5] [6]
Исследование [ править ]
Клинические испытания [ править ]
Эффективность филготиниба изучается в программе фазы IIb (испытания DARWIN 1, 2) с участием 886 пациентов с ревматоидным артритом и 180 пациентов с болезнью Крона. [ необходима цитата ]
Исследование фазы I [ править ]
В исследованиях фазы I было показано, что фармакокинетика метаболизма филготиниба не зависит от ферментативной деградации CYP450 в печени . Однако метаболизм лекарства опосредуется карбоксилэстеразами . Нет сообщений о влиянии на метаболизм метотрексата или каких-либо исследованных транспортных белков. [14]
Исследование фазы II: Доказательство концепции (2011 г.) [ править ]
В ноябре 2011 года Галапагосские острова опубликовали результаты своего исследования фазы II (идентификационный номер: NCT01384422, Eudract: 2010-022953-40), в котором лечили 36 пациентов с ревматоидным артритом, которые показали неоптимальный клинический ответ на лечение метотрексатом . [15] [ требуется полная ссылка ] Три группы из двенадцати пациентов получали либо 200 мг филготиниба в разовой дозе, либо 200 мг, разделенные на две дозы, либо плацебо. Первичной конечной точкой был показатель ACR20., который отслеживает улучшение симптоматики пациента. После запланированных 4 недель лечения 83% респондентов показали улучшение по шкале ACR20. У половины пролеченных пациентов наблюдалась полная (или почти полная) ремиссия заболевания. Сообщений об анемии или изменении липидемии не поступало. Компания заявила в своем пресс-релизе, что филготиниб является первым селективным ингибитором JAK1, который демонстрирует клиническую эффективность. В результате этого исследования компания заявила, что «GLPG0634 показывает один из самых высоких показателей начального ответа, когда-либо сообщавшихся при лечении ревматоидного артрита». [16]
Пробная версия DARWIN 1 [ править ]
Испытание DARWIN 1 представляло собой 24-недельное двойное слепое плацебо-контролируемое испытание с участием 599 пациентов с ревматоидным артритом. Все участники страдали ревматоидным артритом от умеренной до тяжелой степени и продемонстрировали недостаточный ответ на стандартное лечение метотрексатом . В испытании сравнивали три дозы филготиниба по схеме один или два раза в день. [17] [ требуется полная ссылка ] Во время испытания все участники продолжали принимать метотрексат. Испытание завершилось в феврале 2015 года, а результаты были опубликованы в июле 2015 года. [18] [19] Галапагосские острова объявили, что препарат соответствовал ключевым критериям эффективности, показал реакцию ACR70 до 39% и сохранил свой профиль безопасности. [19][20]
Пробная версия DARWIN 2 [ править ]
Испытание DARWIN 2 было двойным слепым плацебо-контролируемым испытанием с участием 280 пациентов с ревматоидным артритом, которые показали недостаточный ответ на стандартное лечение метотрексатом. В отличие от предыдущего исследования DARWIN 1, метотрексат был прекращен. Таким образом, в данном исследовании филготиниб рассматривается как монотерапия второй линии. [21] Набор участников исследования DARWIN 2b закончился в ноябре 2014 года. [22] В августе 2015 года Галапагосские острова объявили, что исследование подтвердило предыдущие результаты. [23]
Пробная версия DARWIN 3 [ править ]
Пациенты, прошедшие DARWIN 1 и 2, имели право на DARWIN 3. В ноябре 2017 года компания объявила о последовательных результатах исследования безопасности и продолжительной активности на 84-й неделе исследования. [24] Предполагаемый срок завершения исследования - май 2019 г. [25] [ требуется полная ссылка ]
Испытания фазы III FINCH [ править ]
FINCH 1 рассматривает пациентов, у которых лечение первой линии метотрексатом (МТ) не работает. В нем сравнивается филготиниб, адалимумаб / хумира и плацебо. [26] FINCH 2 изучает пациентов, у которых не работает биологический препарат. FINCH 3 рассматривает филготиниб как препарат первой линии, в отличие от предыдущих исследований, в которых этот препарат рассматривался как препарат второй линии.
Исследование FINCH 2 выявило пациентов с активным ревматоидным артритом, у которых был неадекватный ответ или непереносимость одного или нескольких DMARD , филготиниб показал значимость в ответе на лечение по сравнению с плацебо. [27]
МАНТА [ править ]
Из-за опасений по поводу токсичности яичек у мужчин в исследовании MANTA изучается безопасность препарата в контексте лечения язвенного колита. [28] [ требуется полная ссылка ] Несмотря на эти опасения, FDA разрешило суточную дозу 200 мг для мужчин в исследованиях фазы III FINCH. [29]
Ссылки [ править ]
- ^ «Трубопровод» . Gilead Sciences . 27 июля 2020 . Проверено 27 июля 2020 .
- ^ "Jyseleca 100 мг таблетки, покрытые пленочной оболочкой - Краткое описание характеристик продукта (SmPC)" . (ЭМС) . 1 октября 2020 . Проверено 4 октября 2020 года .
- ^ a b c d e f g "Jyseleca EPAR" . Европейское агентство по лекарственным средствам (EMA) . 26 мая 2020 . Проверено 4 октября 2020 года .Текст был скопирован из этого источника © Европейское агентство по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ a b Намур F, Дидериксен PM, Кокс Э, Вайссьер Б, Ван дер Аа А, Тассет С, Вант Клостер G (август 2015 г.). «Фармакокинетика и фармакокинетическое / фармакодинамическое моделирование филготиниба (GLPG0634), селективного ингибитора JAK1, в поддержку выбора дозы фазы IIB» . Клиническая фармакокинетика . 54 (8): 859–74. DOI : 10.1007 / s40262-015-0240-Z . PMC 4513223 . PMID 25681059 .
- ^ a b c «Европейская комиссия выдает разрешение на продажу препарата Jyseleca (филготиниб) для лечения взрослых с умеренным и тяжелым активным ревматоидным артритом» (пресс-релиз). Gilead Sciences. 25 сентября 2020 . Проверено 4 октября 2020 г. - через Business Wire.
- ^ a b «Jyseleca (Филготиниб) одобрен в Японии для лечения ревматоидного артрита» . Gilead Sciences. 25 сентября 2020 . Проверено 4 октября 2020 г. - через Business Wire.
- ^ Ван Rompaey L, Galien R, van der Aar EM, Clement-Lacroix P, Nelles L, Smets B, et al. (Октябрь 2013). «Доклиническая характеристика GLPG0634, селективного ингибитора JAK1, для лечения воспалительных заболеваний» . Журнал иммунологии . 191 (7): 3568–77. DOI : 10.4049 / jimmunol.1201348 . PMID 24006460 .
- ^ "AbbVie для продвижения ежедневного ABT-494 до фазы 3 при ревматоидном артрите к концу года | Центр новостей AbbVie" . news.abbvie.com .
- ^ «Компания Gilead подает заявку на новый препарат филготиниба в Управление по контролю за продуктами и лекарствами США в рамках приоритетного рассмотрения для лечения ревматоидного артрита» . Gilead Sciences, Inc. (Пресс-релиз). 19 декабря 2019 . Проверено 27 июля 2020 .
- ^ a b «Jyseleca: Ожидается решение ЕС» . Европейское агентство по лекарственным средствам (EMA) . 23 июля 2020 . Проверено 27 июля 2020 .Текст был скопирован из этого источника © Европейское агентство по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ "Gilead и Galapagos объявляют о положительном европейском мнении CHMP о Jyseleca (Filgotinib) для лечения взрослых с умеренным и тяжелым ревматоидным артритом" (пресс-релиз). 24 июля 2020 . Проверено 27 июля 2020 .
- ^ "Gilead и Galapagos объявляют о положительном европейском мнении CHMP о Jyseleca (Filgotinib) для лечения взрослых с умеренным и тяжелым ревматоидным артритом" . Gilead Sciences, Inc. (Пресс-релиз). 24 июня 2020 . Проверено 27 июля 2020 .
- ^ «FDA отклоняет потенциальный блокбастер филготиниба Gilead из-за опасений по поводу токсичности» . 19 августа 2020.
- ^ Флоренс N, Джули D, Ван дер Аа А, Tasset С, Вант Klooster G (2014). «Данные фазы 1 и фазы 2 подтверждают, что GLPG0634, селективный ингибитор JAK1, имеет низкий потенциал для лекарственного взаимодействия» . Встреча тезисов . Ежегодное собрание ACR / ARHP 2014 г. Американский колледж ревматологии. 1481.
- ^ Номер клинического испытания NCT01384422 "Безопасность и предварительная эффективность GLPG0634 при резистентном к метотрексату активном ревматоидном артрите" на ClinicalTrials.gov
- ^ «GLPG0634 Галапагосских островов демонстрирует превосходную эффективность и безопасность при исследовании фазы II ревматоидного артрита» (PDF) (пресс-релиз) . Проверено 26 февраля 2015 .
- ^ Номер клинического испытания NCT01888874 "Исследование по подбору дозы GLPG0634 в качестве дополнения к метотрексату у пациентов с активным ревматоидным артритом (DARWIN1)" на ClinicalTrials.gov
- ^ «Галапагосские острова сообщают, что последний пациент в DARWIN 1 завершил 12 недель лечения» (PDF) (пресс-релиз) . Проверено 26 февраля 2015 .
- ^ a b «Селективный ингибитор JAK1 на Галапагосских островах филготиниб соответствует ключевым критериям эффективности, показывает реакцию ACR70 до 39% и сохраняет профиль безопасности после 24 недель лечения в исследовании DARWIN 1 Phase 2B» (пресс-релиз). Galapagos NV. 29 июля 2015 г. - через GlobeNewswire.
- ^ Вестховенс Р., Тейлор П.К., Альтен Р., Павлова Д., Энрикес-Соса Ф., Мазур М. и др. (Июнь 2017 г.). «Филготиниб (GLPG0634 / GS-6034), пероральный селективный ингибитор JAK1, эффективен в комбинации с метотрексатом (МТ) у пациентов с активным ревматоидным артритом и недостаточным ответом на метотрексат: результаты рандомизированного исследования по подбору дозы (DARWIN 1) " . Анналы ревматических болезней . 76 (6): 998–1008. DOI : 10.1136 / annrheumdis-2016-210104 . PMID 27993829 .
- ^ «Галапагосские острова завершают набор участников для исследования Дарвина 1 с GLPG0634 (филготиниб) в РА» (пресс-релиз). Galapagos NV . Проверено 26 февраля 2015 г. - через GlobeNewswire.
- ^ «Галапагосские острова завершают набор участников для исследования монотерапии Darwin 2 с GLPG0634 (филготиниб) в РА» (пресс-релиз). Galapagos NV . Проверено 26 февраля 2015 г. - через GlobeNewswire.
- ^ «Данные о 24-недельной монотерапии DARWIN 2 при РА подтверждают предыдущие результаты и подтверждают лучший в своем классе потенциал для филготиниба» (пресс-релиз). Galapagos NV. 10 августа 2015 г. - через GlobeNewswire.
- ^ «Последовательные результаты по безопасности и длительная активность при лечении филготинибом пациентов с ревматоидным артритом до 84 недели в исследовании DARWIN 3» (пресс-релиз). Galapagos NV. 5 ноября 2017 г. - через GlobeNewswire.
- ^ Номер клинического испытания NCT02065700 «Долгосрочное последующее исследование GLPG0634 у пациентов с активным ревматоидным артритом» на ClinicalTrials.gov
- ^ «Программа Filgotinib в РА - Годовой отчет Галапагосских островов 2016» . Галапагосские острова . Проверено 8 января 2018 .
- ^ Genovese MC, Kalunian K, Gottenberg JE, Mozaffarian N, Bartok B, Matzkies F, et al. (Июль 2019 г.). «Эффект филготиниба по сравнению с плацебо на клинический ответ у пациентов со средним и тяжелым ревматоидным артритом, резистентным к модифицирующей заболевание антиревматической лекарственной терапии: рандомизированное клиническое испытание FINCH 2» . ДЖАМА . 322 (4): 315–325. DOI : 10,1001 / jama.2019.9055 . PMC 6652745 . PMID 31334793 .
- ^ Номер клинического испытания NCT03201445 «Исследование по оценке тестикулярной безопасности филготиниба у взрослых мужчин с умеренно или сильно активным язвенным колитом» на ClinicalTrials.gov
- ^ "Галапагосские острова, Gilead включают высокую дозу в испытание PhIII RA после разговора с FDA" . FierceBiotech . Проверено 8 января 2018 .
Внешние ссылки [ править ]
- «Филиготиниб» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- Номер клинического испытания NCT02889796 «Филготиниб в комбинации с метотрексатом у взрослых с умеренно или сильно активным ревматоидным артритом, которые имеют неадекватный ответ на метотрексат (FINCH 1)» на ClinicalTrials.gov
- Номер клинического испытания NCT02873936 «Филготиниб по сравнению с плацебо у взрослых с активным ревматоидным артритом (РА), у которых наблюдается неадекватный ответ на лечение антиревматическими препаратами (БПВП), модифицирующими биологическое заболевание (БПВП) (FINCH 2)» на ClinicalTrials.gov
- Номер клинического испытания NCT02886728 для «Филготиниба в отдельности и в комбинации с метотрексатом (MTX) у взрослых с умеренно или сильно активным ревматоидным артритом, которые не привыкли к терапии MTX (FINCH 3)» на ClinicalTrials.gov
- Номер клинического испытания NCT02914522 «Филготиниб в индукции и поддержании ремиссии у взрослых с умеренно или сильно активным язвенным колитом (SELECTION1)» на сайте ClinicalTrials.gov
- Номер клинического испытания NCT02914561 «Филготиниб в индукции и поддержании ремиссии у взрослых с умеренно или сильно активной болезнью Крона (Diversity1)» на ClinicalTrials.gov
- Номер клинического испытания NCT04115748 «Исследование для оценки эффективности и безопасности филготиниба у участников с активным псориатическим артритом, которые не привыкли к биологической терапии DMARD (PENGUIN 1)» на ClinicalTrials.gov
- Номер клинического испытания NCT04115839 «Исследование для оценки эффективности и безопасности филготиниба у участников с активным псориатическим артритом, которые имеют неадекватный ответ или не переносят биологическую терапию DMARD (PENGUIN 2)» на ClinicalTrials.gov
- СМИ, связанные с Филготинибом, на Викискладе?