 | |
 | |
 | |
| Имена | |
|---|---|
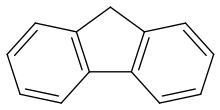
| Предпочтительное название IUPAC 9 H -флуорен | |
| Систематическое название ИЮПАК Трицикло [7.4.0.0 2,7 ] тридека-2,4,6,9,11,13-гексаен | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100,001,541 |
| Номер ЕС |
|
| КЕГГ | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| С 13 Н 10 | |
| Молярная масса | 166,223 г · моль -1 |
| Плотность | 1,202 г / мл |
| Температура плавления | От 116 до 117 ° C (от 241 до 243 ° F, от 389 до 390 K) |
| Точка кипения | 295 ° С (563 ° F, 568 К) |
| 1,992 мг / л | |
| Растворимость | органические растворители |
| журнал P | 4,18 |
| Кислотность (p K a ) | 22,6 |
| -110,5 · 10 −6 см 3 / моль | |
| Опасности | |
| Паспорт безопасности | Сигма-Олдрич |
| NFPA 704 (огненный алмаз) |  1 1 0 |
| точка возгорания | 152 ° С (306 ° F, 425 К) |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 16000 мг / кг (перорально, крыса) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Флуорен / е л ʊər я п / или 9 Н -флуорен представляет собой органическое соединение с формулой (С 6 Н 4 ) 2 СН 2 . Он образует белые кристаллы с характерным ароматным запахом, похожим на запах нафталина . Он имеет фиолетовую флуоресценцию , отсюда и его название. Для коммерческих целей его получают из каменноугольной смолы . [2] Он нерастворим в воде и растворим во многих органических растворителях. Хотя иногда классифицируется как полициклический ароматический углеводород, пятичленное кольцо не имеет ароматических свойств. Флуорен слабокислый.
Синтез, структура и реакционная способность [ править ]
Хотя флуорен получают из каменноугольной смолы, его также можно получить дегидрированием дифенилметана . [2] В качестве альтернативы, он может быть получен восстановлением флуоренона с цинком . [3] Молекула флуорена почти плоская, [4] хотя каждое из двух бензольных колец копланарно с центральным углеродом 9. [5]
Кислотность [ править ]
C9-H участки флуоренового кольца являются слабокислотными ( pK a = 22,6 в ДМСО . [6] ) Депротонирование дает стабильный флуоренильный анион, номинально C 13 H 9 - , который является ароматическим и имеет интенсивный оранжевый цвет. Анион является нуклеофилом . Электрофилы реагируют с ним прибавлением к 9-позиции. При очистке флуорена используются его кислотность и низкая растворимость его производного натрия в углеводородных растворителях.
Оба протона могут быть удалены из C9. Например, 9,9-флуоренилдокалий можно получить обработкой флуорена металлическим калием в кипящем диоксане . [7]
Свойства лиганда [ править ]
Флуорен и его производные можно депротонировать с образованием лигандов, родственных циклопентадиениду .
Использует [ редактировать ]
Флуорен является предшественником других соединений флуорена; у родительского вида мало приложений. Флуорен-9-карбоновая кислота является предшественником фармацевтических препаратов. Окисление флуорена дает флуоренон , который нитруют с получением коммерчески полезных производных. 9-флуоренилметилхлорформиат (Fmoc хлорид) используется для введения защитной группы 9-флуоренилметилкарбамата (Fmoc) на аминах при синтезе пептидов . [2]
Полифлуореновые полимеры (где углерод 7 одного звена соединен с углеродом 2 следующего, замещая два атома водорода) электропроводны и электролюминесцентны , и их много исследовали как люминофор в органических светодиодах .
Флуореновые красители [ править ]
Хорошо развиты флуореновые красители. Большинство из них получают конденсацией активной метиленовой группы с карбонилами. 2-аминофлуорен, 3,6-бис- (диметиламино) флуорен и 2,7-дийодофлуорен являются предшественниками красителей. [9]
См. Также [ править ]
- CataCXium F сульф
- Флуоренол
- Индекаинид
- ПД-137889
Ссылки [ править ]
- ^ Индекс Мерк , 11-е издание, 4081
- ^ a b c Грисбаум, Карл; Бер, Арно; Биденкапп, Дитер; Фогес, Хайнц-Вернер; Гарбе, Доротея; Паец, Кристиан; Коллин, Герд; Майер, Дитер; Хёке (2000). «Углеводороды». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a13_227 .
- ^ Фиттиг, Руд. (1873), "Ueber einen neuen Kohlenwasserstoff aus dem Diphenylenketon" Бер. Dtsch. Chem. Ges. том 6, с. 187. doi : 10.1002 / cber.18730060169
- ^ Д. Бернс, Джон Iball (1954), молекулярная структура флуорен объема Nature 173, с. 635. doi : 10.1038 / 173635a0
- ^ Геркин, RE; Lundstedt, AP; Реппарт, WJ (1984). «Структура флуорена C13H10 при 159 K». Acta Crystallographica Раздел C Связь с кристаллической структурой . 40 (11): 1892–1894. DOI : 10.1107 / S0108270184009963 .
- ^ FG Бордвелл (1988). «Равновесные кислотности в растворе диметилсульфоксида». Соотв. Chem. Res . 21 (12): 456–463. DOI : 10.1021 / ar00156a004 .
- ^ GW Scherf; Р. К. Браун (1960). «Калиевые производные флуорена в качестве промежуточных соединений при получении C9-замещенных флуоренов. I. Получение 9-флуоренил калия и инфракрасные спектры флуорена и некоторых C9-замещенных флуоренов». Канадский химический журнал . 38 : 697. DOI : 10,1139 / v60-100 ..
- ^ Юэн, JA; Джонс, Р.Л .; Разави, А .; Феррара, Дж. Д. (1988). «Синдиоспецифическая полимеризация пропилена с металлоценами группы IVB». Журнал Американского химического общества . 110 (18): 6255–6256. DOI : 10.1021 / ja00226a056 . PMID 22148816 .
- ^ Курдюкова, И.В. Ищенко, А.А. (2012). «Органические красители на основе флуорена и его производных». Российские химические обзоры . 81 (3): 258–290. Bibcode : 2012RuCRv..81..258K . DOI : 10,1070 / RC2012v081n03ABEH004211 .CS1 maint: использует параметр авторов ( ссылка )
Внешние ссылки [ править ]
- Флуорен в базе данных Национального института стандартов и технологий.