Глюкуронизация часто участвует в метаболизме лекарственных веществ, таких как лекарства , загрязнители, билирубин , андрогены , эстрогены , минералокортикоиды , глюкокортикоиды , производные жирных кислот , ретиноиды и желчные кислоты . Эти связи включают гликозидные связи . [1]
Механизм [ править ]
Глюкуронизация заключается в переносе глюкуроновой кислоты, составляющей уридиндифосфатглюкуроновую кислоту, на субстрат с помощью любого из нескольких типов UDP-глюкуронозилтрансферазы .
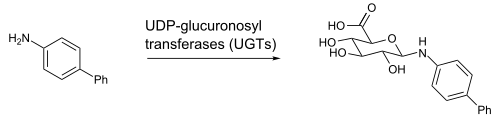
UDP-глюкуроновая кислота (глюкуроновая кислота, связанная гликозидной связью с дифосфатом уридина ) является промежуточным звеном в этом процессе и образуется в печени . Одним из примеров является N-глюкуронирование ароматического амина , 4-аминобифенила , с помощью UGT1A4 или UGT1A9 из печени человека, крысы или мыши. [2]
Вещества , полученные в результате глюкуронизации известны как глюкуронидов (или glucuronosides) и , как правило , гораздо больше воды - растворимы , чем не-глюкуроновой кислоты , содержащие вещества , из которых они были первоначально синтезированы. Организм человека использует глюкуронизацию, чтобы сделать большое количество веществ более растворимыми в воде и, таким образом, обеспечить их последующее выведение из организма с мочой или калом (с желчью из печени). Гормоны глюкуронидированы, чтобы облегчить перенос по телу. Фармакологи связали лекарства с глюкуроновой кислотой, чтобы обеспечить более эффективную доставку широкого спектра потенциальных терапевтических средств. Иногда токсические вещества также менее токсичны после глюкуронизации.
Конъюгация молекул ксенобиотиков с гидрофильными молекулами, такими как глюкуроновая кислота, известна как метаболизм фазы II .
Сайты [ править ]
Глюкуронизация происходит в основном в печени , хотя фермент, ответственный за его катализ , UDP-глюкуронилтрансфераза , обнаружен во всех основных органах тела (например, в кишечнике , почках , головном мозге , надпочечниках , селезенке и тимусе ). [3] [4]
Общие влияющие факторы [ править ]
Различные факторы влияют на скорость глюкуронизации, что, в свою очередь, влияет на выведение этих молекул из организма. Как правило, повышенная скорость глюкуронизации приводит к потере эффективности целевых лекарственных средств или соединений.
| Фактор | Влияние на глюкуронизацию [5] | Основные пораженные наркотики или соединения [5] | |
|---|---|---|---|
| Возраст | Младенец | ↑ | Хлорамфеникол , морфин , парацетамол , билирубин , стероиды |
| Пожилые люди | ↑ или без изменений | Для парацетамола, оксазепама , темазепама или пропранолола изменений не обнаружено . Обнаружено снижение клиренса кодеин- 6-глюкуронида и снижение несвязанного клиренса оксазепама у очень пожилых людей. | |
| Пол | Самки | ↓ | Клиренс парацетамола, оксазепама, темазепама и пропранолола выше у мужчин. Возможная аддитивная роль CYP1A2, приводящая к более высоким концентрациям клозапина и оланзапина у женщин |
| Самцы | ↑ | ||
| Габитус тела | Избыточный вес | ↑ | Удаление лоразепама, оксазепама, темазепама и парацетамола, вероятно, является результатом увеличения размера печени и количества ферментов. |
| Недостаточный вес / недоедание | ↓ | Хлорамфеникол, парацетамол | |
| Состояния болезни | Фульминантный гепатит, цирроз | ↓ | Зидовудин, оксазепам, ламотриджин |
| Гипотиреоз | ↓ | Оксазепам, парацетамол | |
| ВИЧ | ↓ | Парацетамол | |
| Курение табака | ↑ | Пропранолол, оксазепам, лоразепам, парацетамол. Возможная аддитивная роль с индукцией CYP1A2, вызывающая снижение концентрации клозапина и оланзапина. | |
Затронутые наркотики [ править ]
На многие препараты, которые являются субстратами для глюкуронизации в рамках их метаболизма, в значительной степени влияют ингибиторы или индукторы их конкретных типов глюкуронизилтрансфераз:
| Субстрат | Ингибиторы глюкуронизации [5] | Индукторы глюкуронизации [5] [6] |
|---|---|---|
| Морфий |
|
|
| Оксазепам |
|
|
| Билирубин |
| |
| Парацетамол |
| |
| Андростерон |
| |
| Карбамазепин- 10,1 1-трансдиол |
| |
| Кодеин |
| |
| Ламотриджин |
| |
| Лоразепам |
| |
| Темазепам |
| |
| Тестостерон |
| |
| Зидовудин |
|
Ссылки [ править ]
- ^ Кинг С, G Rios, зеленый М, Tephly Т (2000). «УДФ-глюкуронозилтрансферазы». Curr. Drug Metab . 1 (2): 143–61. DOI : 10.2174 / 1389200003339171 . PMID 11465080 .
- ^ Al-Zoughool М., Talaska, G. (2006). «4-Аминобифенил-N-глюкуронирование микросомами печени: оптимизация условий реакции и характеристика изоформ UDP-глюкуронозилтрансферазы». J. Appl. Токсикология . 26 (6): 524–532. DOI : 10.1002 / jat.1172 . PMID 17080401 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Оно, Сюдзи; Накадзин, Шизуо (2008-10-06). «Определение экспрессии мРНК человеческих UDP-глюкуронозилтрансфераз и применение для локализации в различных тканях человека с помощью цепной реакции обратной транскриптазы-полимеразы в реальном времени» . Метаболизм и диспозиция лекарств . Американское общество фармакологии и экспериментальной терапии . 37 (1): 32–40. DOI : 10,1124 / dmd.108.023598 . PMID 18838504 . S2CID 5150289 . Проверено 7 ноября 2010 .
- ^ Bock K, Köhle C (2005). «UDP-глюкуронозилтрансфераза 1A6: структурные, функциональные и регуляторные аспекты». Методы Энзимол . Методы в энзимологии. 400 : 57–75. DOI : 10.1016 / S0076-6879 (05) 00004-2 . ISBN 9780121828059. PMID 16399343 .
- ^ a b c d Если иное не указано в полях, тогда ссылка: Liston, H .; Марковиц, Дж .; Девейн, К. (2001). «Лекарственная глюкуронизация в клинической психофармакологии». Журнал клинической психофармакологии . 21 (5): 500–515. DOI : 10.1097 / 00004714-200110000-00008 . PMID 11593076 .
- ^ Нил Б. Сэндсон, Учебник по взаимодействию наркотиков и лекарств