 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Трихлорид золота (III) | |
| Другие имена Хлорид аурической кислоты Трихлорид золота | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.033.280 |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| AuCl 3 (существует как Au 2 Cl 6 ) | |
| Молярная масса | 606,6511 г / моль |
| Внешность | Красные кристаллы (безводные); золотые, желтые кристаллы (моногидрат) [1] |
| Плотность | 4,7 г / см 3 |
| Температура плавления | 254 ° С (489 ° F, 527 К) (разлагается) |
| 68 г / 100 мл (холодная) | |
| Растворимость | растворим в эфире , мало растворим в жидком аммиаке |
| −112 · 10 −6 см 3 / моль | |
| Структура | |
| моноклинический | |
| Квадратный плоский | |
| Опасности [2] | |
| Основные опасности | Раздражающий |
| Паспорт безопасности | См .: страницу данных |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| H315 , H319 , H335 | |
| P261 , P305 + 351 + 338 | |
| Родственные соединения | |
Другие анионы | Фторид золота (III) Бромид золота (III) Нитрат золота (III) |
Другие катионы | Хлорид золота (I) Хлорид серебра (I) Хлорид платины (II) Хлорид ртути (II) |
| Страница дополнительных данных | |
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. |
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ |
Спектральные данные | УФ , ИК , ЯМР , МС |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Золото (III) хлорид , традиционно называют аурический хлоридом , представляет собой химическое соединение , из золота и хлора . С молекулярной формулой Au 2 Cl 6 название трихлорид золота является упрощением, ссылаясь на эмпирическую формулу AuCl 3 . В римские цифры в названии указывают , что золото имеет степень окисления +3, который является общим для соединений золота. Существует также другой родственный хлорид золота - хлорид золота (I) (AuCl). Хлористоводородная кислота , HAuCl 4 , продукт, образующийся при растворении золота вцарская водка , иногда упоминается как «хлорид золота» или «кислотный трихлорид золота». Хлорид золота (III) очень гигроскопичен и хорошо растворяется в воде, а также в этаноле . Разлагается выше 160 ° C или на свету.
Структура [ править ]
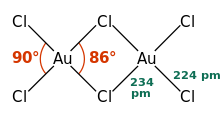
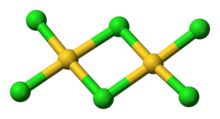
AuCl 3 существует в виде димера с мостиковыми связями хлорида как в твердом, так и в парообразном состоянии, по крайней мере, при низких температурах. [3] Бромид золота (III) ведет себя аналогично. [1] Структура подобна хлориду йода (III) .
В хлориде золота (III) каждый центр золота имеет плоскую квадратную форму [1], что типично для металлического комплекса с числом электронов ad 8 . Связь в AuCl 3 считается в некоторой степени ковалентной .
Подготовка [ править ]
Хлорид золота (III) чаще всего получают пропусканием газообразного хлора над золотым порошком при 180 ° C: [1]
- 2 Au + 3 Cl 2 → Au 2 Cl 6
Другой способ получения - взаимодействие частиц Au 3+ с хлоридом с образованием тетрахлораурата. Затем его кислота, хлористоводородная кислота , нагревается для удаления газообразного хлористого водорода . Реакция с царской водкой дает хлорид золота (III):
- Au (s) + 3 NO-
3(водн.) + 6 H + (водн.) ⇌ Au 3+ (водн.) + 3 NO 2 (г) + 3 H 2 O (л) - Au 3+ (водн.) + 3 NOCl (г) + 3 NO-
3(водн.) → AuCl 3 (водн.) + 6 NO 2 (г) - AuCl 3 (водн.) + Cl - (водн.) ⇌ AuCl-
4(водн.) - 2 HAuCl 4 ( тв. ) → Au 2 Cl 6 (тв.) + 2 HCl (г)
Реакции [ править ]
При контакте с водой AuCl
3образует кислые гидраты и конъюгат основания [AuCl
3(ОЙ)]-
. Может быть уменьшено Fe2+вызывая осаждение элементарного золота из раствора. [1]
Безводный AuCl 3 начинает разлагаться до AuCl примерно при 160 ° C; однако это, в свою очередь, подвергается диспропорционированию при более высоких температурах с образованием металлического золота и AuCl 3 .
- AuCl 3 → AuCl + Cl 2 (> 160 ° C)
- 3 AuCl → AuCl 3 + 2 Au (> 420 ° C)
AuCl 3 является кислотой Льюиса и легко образует комплексы . Например, он реагирует с соляной кислотой с образованием золотохлористоводородной кислоты ( HAuCl
4):
- HCl + AuCl
3(водный) → H+
+ [AuCl
4]-
Другие источники хлорида, такие как KCl , также превращают AuCl 3 в AuCl.-
4. Водные растворы AuCl 3 реагируют с водным основанием, таким как гидроксид натрия, с образованием осадка Au (OH) 3 , который растворяется в избытке NaOH с образованием аурата натрия (NaAuO 2 ). При осторожном нагревании Au (OH) 3 разлагается на оксид золота (III) , Au 2 O 3 , а затем на металлическое золото. [4] [5] [6] [7] [8]
Хлорид золота (III) является отправной точкой для синтеза многих других соединений золота. Например, реакция с цианидом калия дает водорастворимый комплекс K [Au (CN) 4 ]:
- AuCl
3+ 4 KCN → K [Au (CN)
4] + 3 KCl
Приложения в органическом синтезе [ править ]
AuCl 3 вызвал интерес химиков-органиков как слабокислый катализатор для множества реакций [9], хотя коммерческие преобразования не применялись. Соли золота (III) , особенно Na [AuCl 4 ] (полученные из AuCl 3 + NaCl ), представляют собой альтернативу солям ртути (II) в качестве катализаторов реакций с участием алкинов . Иллюстративной реакцией является гидратация концевых алкинов с образованием ацетильных соединений. [10]
Некоторые алкины подвергаются аминированию в присутствии золотых (III) катализаторов. Золото катализирует алкилирование определенных ароматических колец и превращение фуранов в фенолы . Так , например, смесь ацетонитрила и золото (III) хлорид катализирует алкилирование 2-метилфурана по метилвинилкетону в 5-положении:
Эффективность этой реакции с золотоорганическими соединениями заслуживает внимания, потому что и фуран, и кетон чувствительны к побочным реакциям, таким как полимеризация в кислых условиях. В некоторых случаях, когда присутствуют алкины , иногда образуются фенолы (Ts = тозил ): [11]
Эта реакция включает перегруппировку, которая дает новое ароматическое кольцо. [12]
В качестве стехиометрического реагента хлорид ауры реагирует с бензолом (и рядом других аренов) в чрезвычайно мягких условиях (минуты при комнатной температуре) с образованием димерного дихлорида фенилзолота (III): [13]
PhH + ½ Au 2 Cl 6 → ½ [PhAuCl 2 ] 2 + HCl
Ссылки [ править ]
- ^ а б в г д Эгон Виберг; Нильс Виберг; А.Ф. Холлеман (2001). Неорганическая химия (101-е изд.). Академическая пресса. С. 1286–1287. ISBN 978-0-12-352651-9.
- ^ «Хлорид золота» . Американские элементы . Проверено 22 июля 2019 года .
- ^ ES Кларк; Д.Х. Темплтон; CH MacGillavry (1958). «Кристаллическая структура хлорида золота (III)» . Acta Crystallogr . 11 (4): 284–288. DOI : 10.1107 / S0365110X58000694 . Проверено 21 мая 2010 .
- ^ Н. Н. Гринвуд, А. Эрншоу, Химия элементов , 2-е изд., Баттерворт-Хайнеманн, Оксфорд, Великобритания, 1997
- ^ Справочник по химии и физике , 71-е издание, CRC Press, Анн-Арбор, Мичиган, 1990
- ^ Индекс Merck . Энциклопедия химикатов, лекарств и биологических препаратов . 14. Ред., 2006, с. 780, ISBN 978-0-911910-00-1 .
- ^ Х. Нечамкин, Химия элементов , McGraw-Hill, Нью-Йорк, 1968
- ^ AF Wells, Структурная неорганическая химия , 5-е изд., Oxford University Press, Оксфорд, Великобритания, 1984
- ^ Г. Дайкер, Эльдорадо для гомогенного катализа? , в Organic Synthesis Highlights V , H.-G. Шмальц, Т. Вирт (ред.), Стр 48-55, Wiley-VCH, Weinheim, 2003
- ↑ Ю. Фукуда; К. Утимото (1991). «Эффективное превращение неактивированных алкинов в кетоны или ацетали с катализатором золота (III)». J. Org. Chem. 56 (11): 3729. DOI : 10.1021 / jo00011a058 .
- ^ СПРОСИТЕ Хашми; ТМ Frost; JW Летучие мыши (2000). «Высокоселективный синтез арена, катализируемый золотом». Варенье. Chem. Soc. 122 (46): 11553. DOI : 10.1021 / ja005570d .
- ^ А. Стивен; К. Хашми; М. Рудольф; JP Weyrauch; М. Вёльфле; В. Фрей; JW Летучие мыши (2005). «Золотой катализ: доказательство наличия оксидов арена в качестве промежуточных продуктов в синтезе фенола». Angewandte Chemie International Edition . 44 (18): 2798–801. DOI : 10.1002 / anie.200462672 . PMID 15806608 .
- ^ Ли, Зиганг; Брауэр, Чад; Хэ, Чуан (1 августа 2008 г.). "Органические превращения, катализируемые золотом". Химические обзоры . 108 (8): 3239–3265. DOI : 10.1021 / cr068434l . ISSN 0009-2665 . PMID 18613729 .
Внешние ссылки [ править ]
- СМИ, связанные с трихлоридом золота на Викискладе?