| |||
| Имена | |||
|---|---|---|---|
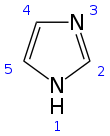
| Предпочтительное название IUPAC 1 H- имидазол [1] | |||
| Систематическое название ИЮПАК 1,3-диазациклопента-2,4-диен | |||
| Другие имена 1,3-Диазол Глиоксалин (архаичный) | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.005.473 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 3 H 4 N 2 | |||
| Молярная масса | 68,077 г / моль | ||
| Внешность | Белое или бледно-желтое твердое вещество | ||
| Плотность | 1,23 г / см 3 , твердый | ||
| Температура плавления | От 89 до 91 ° C (от 192 до 196 ° F, от 362 до 364 K) | ||
| Точка кипения | 256 ° С (493 ° F, 529 К) | ||
| 633 г / л | |||
| Кислотность (p K a ) | 6,95 (для конъюгированной кислоты ) [2] | ||
| УФ-видимый (λ макс. ) | 206 нм | ||
| Структура | |||
| Моноклиника | |||
| Планарное 5-членное кольцо | |||
Дипольный момент | 3.61 D | ||
| Опасности | |||
| Основные опасности | Коррозионный | ||
| Паспорт безопасности | Внешний паспорт безопасности материалов | ||
Формулировки опасности GHS | H302 , H314 , H360D | ||
Меры предосторожности GHS | P263 , P270 , P280 , P301 + 310 , P305 + 351 + 338 , P308 + 313 [3] | ||
| точка возгорания | 146 ° С (295 ° F, 419 К) | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Имидазол представляет собой органическое соединение с формулой C 3 N 2 H 4 . Это белое или бесцветное твердое вещество, растворимое в воде с образованием слабощелочного раствора. В химии это ароматический гетероцикл , классифицируемый как диазол , с несмежными атомами азота .
Многие натуральные продукты, особенно алкалоиды , содержат имидазольное кольцо. Эти имидазолы имеют общее кольцо 1,3-C 3 N 2, но имеют различные заместители. Эта кольцевая система присутствует в важных биологических строительных блоках, таких как гистидин и связанный с ним гормон гистамин . Многие препараты содержат имидазольное кольцо, например, некоторые противогрибковые препараты , антибиотики из ряда нитроимидазолов и седативный мидазолам . [4] [5] [6] [7] [8]
Когда он конденсируется с пиримидиновым кольцом, он образует пурин , который является наиболее широко встречающимся азотсодержащим гетероциклом в природе. [9]
Название «имидазол» было придумано в 1887 году немецким химиком Артуром Рудольфом Ганчем (1857–1935). [10]
Структура и свойства [ править ]
Имидазол представляет собой плоское 5-членное кольцо. Он существует в двух эквивалентных таутомерных формах, потому что водород может быть связан с одним или другим атомом азота . Имидазола является весьма полярным соединением, о чем свидетельствует его электрическим дипольный момент 3,67 D . [11] Он хорошо растворяется в воде. Соединение классифицируется как ароматическое из-за наличия плоского кольца, содержащего 6 π-электронов (пара электронов от протонированного атома азота и по одному от каждого из оставшихся четырех атомов кольца). Некоторые резонансные структуры имидазола показаны ниже:
Амфотеризм [ править ]
Имидазол амфотерный . То есть он может действовать как кислота и как основание. Как кислота, p K a имидазола составляет 14,5, что делает его менее кислым, чем карбоновые кислоты, фенолы и имиды, но немного более кислым, чем спирты. Кислый протон связан с азотом. Депротонирование дает анион имидазолида, который является симметричным. В качестве основания p K a конъюгированной кислоты (обозначается как p K BH +, чтобы избежать путаницы между ними) составляет примерно 7, что делает имидазол примерно в шестьдесят раз более основным, чем пиридин.. Основной сайт - это азот с неподеленной парой (и не связанный с водородом). Протонирование дает катион имидазолия, который является симметричным.
Подготовка [ править ]
Впервые об имидазоле сообщил в 1858 году немецкий химик Генрих Дебус , хотя различные производные имидазола были открыты еще в 1840-х годах. Было показано, что глиоксаль , формальдегид и аммиак конденсируются с образованием имидазола (глиоксалина, как его первоначально называли). [12] Этот синтез, хотя и дает относительно низкие выходы, все еще используется для получения C- замещенных имидазолов.
В одной микроволновой модификации реагентами являются бензил , бензальдегид и аммиак в ледяной уксусной кислоте , образуя 2,4,5-трифенилимидазол («лофин»). [13]
Имидазол можно синтезировать множеством методов помимо метода Дебуса . Многие из этих синтезов можно также применять к замещенным имидазолам, варьируя функциональные группы реагентов. Эти методы обычно классифицируются по количеству реагирующих компонентов.
- Один компонент
Связь (1,5) или (3,4) может быть образована реакцией имидата и α- аминоальдегида или α- аминоацеталя . Приведенный ниже пример применим к имидазолу, когда R 1 = R 2 = водород.
- Двухкомпонентный
В (1,2) и (2,3) связи могут быть образованы путем обработки 1,2-диамино алкан , при высоких температурах, с спирта , альдегида или карбоновой кислоты . Требуется катализатор дегидрирования, такой как платина на оксиде алюминия .
Связи (1,2) и (3,4) также могут быть образованы из N- замещенных α-аминокетонов и формамида при нагревании. Продуктом будет 1,4-дизамещенный имидазол, но здесь, поскольку R 1 = R 2 = водород, сам имидазол является продуктом. Выход этой реакции невелик, но, по-видимому, это наиболее эффективный метод получения 1,4-замещения.
- Три компонента
Этот метод дает хорошие выходы для замещенных имидазолов. Это адаптация метода Дебуса, он называется синтез имидазола Дебуса-Радзишевского . Исходные материалы представляют собой замещенный глиоксаль, альдегид, амин и аммиак или соль аммония. [14]
- Образование из других гетероциклов
Имидазол может быть синтезирован с помощью фотолиза из 1-винилтетразола . Эта реакция даст существенные выходы только в том случае, если 1-винилтетразол эффективно получить из оловоорганического соединения , такого как 2-трибутилстаннилтетразол. Реакция, показанная ниже, дает имидазол, когда R 1 = R 2 = R 3 = водород.
Имидазол также может образовываться в парофазной реакции. Реакция происходит с формамидом , этилендиамином и водородом над платиной на оксиде алюминия , и она должна происходить при температуре от 340 до 480 ° C. Это образует очень чистый имидазольный продукт.
- Реакция Ван Лойзена [15]
Реакция Ван Лойзена также может быть использована для образования имидазолов, начиная с TosMIC и альдимина . Синтез имидазола Ван Лойзена позволяет получать имидазолы из альдиминов путем реакции с тозилметилизоцианидом (TosMIC). Позднее реакция была расширена до двухэтапного синтеза, в котором альдимин образуется in situ: трехкомпонентная реакция Ван Лойзена (vL-3CR).
Биологическое значение и применение [ править ]
Имидазол входит во многие важные биологические соединения. Наиболее распространенной является аминокислота гистидин , которая имеет боковую цепь имидазола . Гистидин присутствует во многих белках и ферментах и играет жизненно важную роль в структуре и связывающих функциях гемоглобина . Гистидиновые соединения на основе имидазола играют очень важную роль во внутриклеточной буферизации. [16] Гистидин можно декарбоксилировать до гистамина , который также является обычным биологическим соединением. Гистамин может вызывать крапивницу (крапивницу), если вырабатывается во время аллергической реакции.реакция. Взаимосвязь между гистидином и гистамином показана ниже:
Одним из применений имидазола является очистка белков, меченных His, в аффинной хроматографии с иммобилизованным металлом (IMAC). Имидазол используется для элюирования меченых белков, связанных с ионами никеля , прикрепленными к поверхности шариков в хроматографической колонке. Избыток имидазола пропускается через колонку, что вытесняет His-метку из координации никеля, освобождая His-меченные белки.
Имидазол стал важной частью многих фармацевтических препаратов. Синтетические имидазолы присутствуют во многих фунгицидов и противогрибковые , антипротозойная и антигипертензивных препаратов. Имидазол является частью молекулы теофиллина , содержащейся в чайных листьях и кофейных зернах, которая стимулирует центральную нервную систему . Он присутствует в противоопухолевом препарате меркаптопурин , который борется с лейкемией , нарушая активность ДНК .
Ряд замещенных имидазолов, включая клотримазол , являются селективными ингибиторами синтазы оксида азота , что делает их интересными мишенями для лечения воспалений , нейродегенеративных заболеваний и опухолей нервной системы. [17] [18] Другие биологические активности фармакофора имидазола связаны с подавлением внутриклеточных потоков Ca 2+ и K + и вмешательством в инициацию трансляции. [19]
Фармацевтические производные [ править ]
Замещенные производные имидазола ценны при лечении многих системных грибковых инфекций . [20] Имидазолы относятся к классу азольных противогрибковых средств , который включает кетоконазол , миконазол и клотримазол .
Для сравнения, другая группа азолов - это триазолы, в которую входят флуконазол , итраконазол и вориконазол . Разница между имидазолами и триазолами заключается в механизме ингибирования фермента цитохрома P450 . N3 имидазольного соединения связывается с атомом железа гема цитохрома трехвалентного железа P450, тогда как N4 триазолов связывается с гемовой группой. Было показано, что триазолы обладают более высокой специфичностью к цитохрому P450, чем имидазолы, что делает их более активными, чем имидазолы. [21]
Некоторые производные имидазола оказывают действие на насекомых, например, нитрат сульконазола оказывает сильное антипитательное действие на переваривающих кератин личинок австралийского коврового жука Anthrenocerus australis , равно как и нитрат эконазола в отношении обыкновенной платочной моли Tineola bisselliella . [22]
Промышленное применение [ править ]
Сам имидазол не имеет прямого применения. Вместо этого он является предшественником множества агрохимикатов, в том числе enilconazole , климбазола , клотримазол , прохлораза и бифоназол . [23]
Соли имидазола [ править ]
Соли имидазола, в которых имидазольное кольцо является катионом , известны как соли имидазолия (например, хлорид или нитрат имидазолия ). [24] Эти соли образуются в результате протонирования или замещения имидазола по азоту . Эти соли использовались в качестве ионных жидкостей и предшественников стабильных карбенов . Также хорошо известны соли, в которых депротонированный имидазол является анионом ; эти соли известны как имидазолаты (например, имидазолат натрия, NaC 3 H 3 N 2 ).
Связанные гетероциклы [ править ]
- Бензимидазол , аналог с конденсированным бензольным кольцом
- Дигидроимидазол или имидазолин, аналог, где 4,5- двойная связь является насыщенной
- Пиррол , аналог только с одним атомом азота в положении 1
- Оксазол , аналог с атомом азота в положении 1, замененным на кислород
- Тиазол , аналог с атомом азота в положении 1, замененным на серу
- Пиразол , аналог с двумя соседними атомами азота
- Триазолы , аналоги с тремя атомами азота
Безопасность [ править ]
Имидазол имеет низкую острую токсичность, на что указывает ЛД 50, равная 970 мг / кг (крыса, перорально). [23]
См. Также [ править ]
- 1-метилимидазол
- 4-метилимидазол
Ссылки [ править ]
- ^ "Front Matter". Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 140. DOI : 10.1039 / 9781849733069-FP001 . ISBN 978-0-85404-182-4.
- ^ Walba, H .; Isensee, RW (1961). «Константы кислотности некоторых арилимидазолов и их катионов». J. Org. Chem . 26 (8): 2789–2791. DOI : 10.1021 / jo01066a039 .
- ^ «Имидазол» . molkula.com . Молекула Групп.
- ^ Карицкий, АР ; Рис, CWR; Скривен, EFV (1984). Комплексная гетероциклическая химия . 5 . С. 469–498. ISBN 978-0-08-042072-1.
- ^ Гримметт, М. Росс (1997). Синтез имидазола и бензимидазола . Академическая пресса. ISBN 978-0-08-053445-9.
- ^ Браун, EG (1998). Кольцевой азот и ключевые биомолекулы . Kluwer Academic Press. ISBN 978-94-011-4906-8.
- ^ Пожарский, АФ; и другие. (1997). Гетероциклы в жизни и обществе . Джон Вили и сыновья. ISBN 978-0-471-96033-1.
- Перейти ↑ Gilchrist, TL (1985). Гетероциклическая химия . Пресс для ванны. ISBN 978-0-582-01421-3.
- ^ Rosemeyer, Х. (2004). «Химическое разнообразие пурина как компонента натуральных продуктов». Химия и биоразнообразие . 1 (3): 361–401. DOI : 10.1002 / cbdv.200490033 . PMID 17191854 .
- ^ Ганча, А. и Вебер, JH (1887) "Ueber Verbindungen де Thiazols (Pyridins дер Thiophenreihe)" (О соединений тиазола (пиридинов серии тиофен), Berichte дер Deutschen Gesellschaft Chemischen , 20 : 3118-3132, см 3119. См. Также: Hantzsch, A. (1888) «Allegemeine Bemerkungen über Azole» (Общие замечания об азолах), Annalen der Chemie , 249 : 1–6. Ханцш предложил реформу номенклатуры азольных соединений, включая предложение чтобы назвать гетероциклическое кольцо C 3 H 3 (NH) N «имидазолом», см. стр. 2 и 4.
- ^ Кристен, обедает; Гриффитс, Джон Х .; Шеридан, Джон (1981). "Микроволновый спектр имидазола; Полная структура и распределение электронов от ядерных квадрупольных тензоров взаимодействия и ориентации дипольного момента". Zeitschrift für Naturforschung . 36 (12): 1378–1385. Bibcode : 1981ZNatA..36.1378C . DOI : 10.1515 / зна-1981-1220 .
- ^ Дебус, Генрих (1858). "Ueber die Einwirkung des Ammoniaks auf Glyoxal" [О реакции аммиака на глиоксаль]. Annalen der Chemie und Pharmacie . 107 (2): 199–208. DOI : 10.1002 / jlac.18581070209 .С п. 205: "Die gereinigte Substanz stellt das oxalsaure Salz einer Basis dar, die ich mit Glyoxalin bezeichenen werde." (Очищенное вещество представляет собой щавелевую соль основания, которую я обозначу как «глиоксалин».)
- ^ Крауч, Р. Дэвид; Ховард, Джессика Л .; Zile, Jennifer L .; Баркер, Кэтрин Х. (2006). «Микроволновый синтез лофина: разработка механизма объяснения продукта». J. Chem. Educ . 83 (11): 1658. Bibcode : 2006JChEd..83.1658C . DOI : 10.1021 / ed083p1658 .
- ^ Патент США 6177575 , Arduengo, AJ , «Процесс для производства имидазола», выданного 2001-01-23
- ^ Ван Леузен, Альберт М .; Уайлдеман, Юрьен; Oldenziel, Отто Х. (1977). «Химия сульфонилметилизоцианидов. 12. Индуцированное основанием циклоприсоединение сульфонилметилизоцианидов к углеродным, азотным двойным связям. Синтез 1,5-дизамещенных и 1,4,5-тризамещенных имидазолов из альдиминов и имидоилхлоридов». Журнал органической химии . 42 (7): 1153–1159. Bibcode : 1977JOrgC..42.1153A . DOI : 10.1021 / jo00427a012 .
- ^ Хочачка, П.В.; Somero, GN (2002). Биохимическая адаптация: механизмы и процессы физиологической эволюции . Нью-Йорк: Издательство Оксфордского университета.
- ^ Castaño, T .; Encinas, A .; Pérez, C .; Castro, A .; Кампильо, Северная Каролина; Гил, К. (2008). «Дизайн, синтез и оценка потенциальных ингибиторов синтазы оксида азота» (PDF) . Биоорг. Med. Chem. (Представлена рукопись). 16 (11): 6193–6206. DOI : 10.1016 / j.bmc.2008.04.036 . ЛВП : 10261/87090 . PMID 18477512 .
- ^ Богл, RG; Уитли, GS; Soo, SC; Джонстон, AP; Валланс, П. (1994). «Влияние противогрибковых имидазолов на уровни мРНК и ферментативную активность индуцибельной синтазы оксида азота» . Br. J. Pharmacol . 111 (4): 1257–1261. DOI : 10.1111 / j.1476-5381.1994.tb14881.x . PMC 1910171 . PMID 7518297 .
- ^ Халид, MH; Tokunaga, Y .; Caputy, AJ; Уолтерс, Э. (2005). «Подавление роста опухоли и продление срока выживания крыс с внутричерепными глиомами после введения клотримазола». J. Neurosurg . 103 (1): 79–86. DOI : 10,3171 / jns.2005.103.1.0079 . PMID 16121977 .
- ^ Leon Shargel. Всесторонний обзор аптек (6-е изд.). п. 930. ISBN 9780781765619.
- ^ Дэвис, Дженнифер Л .; Папич, Марк Г .; Хейт, Марк К. (2009). «Глава 39: Противогрибковые и противовирусные препараты» . В Ривьере, Джим Э .; Папич, Марк Г. (ред.). Ветеринарная фармакология и терапия (9-е изд.). Вили-Блэквелл. С. 1019–1020. ISBN 978-0-8138-2061-3.
- ^ Сандерленд, MR; Cruickshank, RH; Ли, SJ (2014). «Эффективность противогрибкового азола и противопротозойных соединений в защите шерсти от личинок насекомых, переваривающих кератин». Текстиль Res. Дж . 84 (9): 924–931. DOI : 10.1177 / 0040517513515312 .
- ^ а б Эбель, К., Кёлер, Х., Геймер, АО, и Джек, Р. (2002). «Имидазол и производные». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a13_661 .CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Zolfigol, Mohammad A .; Хазаеи, Ардешир; Moosavi-Zare, Ahmad R .; Заре, Абдолкарим; Крюгер, Хендрик G .; Асгари, Жила; Хакызаде, Вахид; Казем-Ростами, Масуд (06.04.2012). «Дизайн ионной жидкости нитрата имидазолия 3-метил-1-сульфоновой кислоты в качестве реагента для нитрования ароматических соединений путем генерации NO2 в кислой среде in situ». Журнал органической химии . 77 (7): 3640–3645. DOI : 10.1021 / jo300137w . ISSN 0022-3263 . PMID 22409592 .