 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Карбонат натрия | |
| Предпочтительное название IUPAC Карбонат натрия | |
| Другие названия Кальцинированная сода, стиральная сода, кристаллы соды, триоксокарбонат натрия | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.007.127 |
| Номер ЕС |
|
| Номер E | E500 (i) (регуляторы кислотности, ...) |
PubChem CID | |
| Номер RTECS |
|
| UNII |
|
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
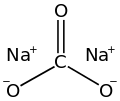
| Na 2 CO 3 | |
| Молярная масса | 105,9888 г / моль (безводный) 286,1416 г / моль (декагидрат) |
| Появление | Белое твердое вещество, гигроскопично |
| Запах | Без запаха |
| Плотность | |
| Температура плавления | 851 ° C (1564 ° F, 1124 K) (безводный) 100 ° C (212 ° F, 373 K) разлагается (моногидрат) 33,5 ° C (92,3 ° F, 306,6 K) разлагается (гептагидрат) 34 ° C (93 ° F; 307 K) (декагидрат) [2] [6] |
Безводный, г / 100 мл:
| |
| Растворимость | Растворим в водн. щелочи , [3] глицерин. Слабо растворим в водн. спирт Нерастворим в CS 2 , ацетоне , алкилацетатах , спирте, бензонитриле , жидком аммиаке [4] |
| Растворимость в глицерине | 98,3 г / 100 г (155 ° C) [4] |
| Растворимость в этандиоле | 3,46 г / 100 г (20 ° C) [5] |
| Растворимость в диметилформамиде | 0,5 г / кг [5] |
| Кислотность (p K a ) | 10,33 |
Магнитная восприимчивость (χ) | −4,1 · 10 −5 см 3 / моль [2] |
Показатель преломления ( n D ) | 1,485 (безводный) 1,420 (моногидрат) [6] 1,405 (декагидрат) |
| Вязкость | 3,4 сП (887 ° C) [5] |
| Состав | |
Кристальная структура | Моноклинный (γ-форма, β-форма, δ-форма, безводный) [7] Орторомбический (моногидрат, гептагидрат) [1] [8] |
Космическая группа | C2 / m, № 12 (γ-форма, безводная, 170 K) C2 / m, № 12 (β-форма, безводная, 628 K) P2 1 / n, № 14 (δ-форма, безводная, 110 K) [7] Pca2 1 , № 29 (моногидрат) [1] Pbca, № 61 (гептагидрат) [8] |
Группа точек | 2 / м (γ-форма, β-форма, δ-форма, безводный) [7] мм2 (моногидрат) [1] 2 / м 2 / м 2 / м (гептагидрат) [8] |
Постоянная решетки | a = 8,920 (7) Å, b = 5,245 (5) Å, c = 6,050 (5) Å (γ-форма, безводная, 295 K) [7] α = 90 °, β = 101,35 (8) °, γ = 90 ° |
Координационная геометрия | Октаэдрический (Na + , безводный) |
| Термохимия | |
Теплоемкость ( C ) | 112,3 Дж / моль · К [2] |
Стандартная мольная энтропия ( S | 135 Дж / моль · К [2] |
Std энтальпия формации (Δ F H ⦵ 298 ) | -1130,7 кДж / моль [2] [5] |
Свободная энергия Гиббса (Δ f G ˚) | -1044,4 кДж / моль [2] |
| Опасности | |
| Основные опасности | Раздражающий |
| Паспорт безопасности | Паспорт безопасности |
| Пиктограммы GHS | [9] |
| Сигнальное слово GHS | Предупреждение |
Положения об опасности GHS | H319 [9] |
Меры предосторожности GHS | P305 + 351 + 338 [9] |
| NFPA 704 (огненный алмаз) | [11]  2 0 0 |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 4090 мг / кг (крыса, перорально) [10] |
| Родственные соединения | |
Другие анионы | Бикарбонат натрия |
Другие катионы | Карбонат лития Карбонат калия Карбонат рубидия Карбонат цезия |
Родственные соединения | Сесквикарбонат натрия Перкарбонат натрия |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Карбонат натрия , Na 2 CO3.10.H2O, (также известный как стиральная сода , кальцинированная сода и кристаллы соды ) представляет собой неорганическое соединение с формулой Na 2 CO 3 и его различные гидраты. Все формы представляют собой белые водорастворимые соли без запаха, образующие умеренно щелочные растворы в воде. Исторически его добывали из золы растений, произрастающих на богатых натрием почвах. Поскольку зола этих богатых натрием растений заметно отличалась от древесной золы (когда-то использовавшейся для производства поташа ), карбонат натрия стал известен как «кальцинированная сода». [12] Он производится в больших количествах из хлорида натрия и известняка с помощьюСольвеевский процесс .
Увлажняет [ править ]
Карбонат натрия получают в виде трех гидратов и безводной соли:
- декагидрат карбоната натрия ( натрон ), Na 2 CO 3 · 10H 2 O, который легко выцветает с образованием моногидрата.
- гептагидрат карбоната натрия (минеральная форма неизвестна), Na 2 CO 3 · 7H 2 O.
- моногидрат карбоната натрия ( термонатрит ), Na 2 CO 3 · H 2 O. Также известен как кристаллический карбонат .
- безводный карбонат натрия, также известный как кальцинированная сода, образуется при нагревании гидратов. Он также образуется при нагревании (кальцинировании) гидрокарбоната натрия, например, на последней стадии процесса Сольвея .
Декагидрат образуется из водных растворов, кристаллизующихся в диапазоне температур от -2,1 до +32,0 ° C, гептагидрат в узком диапазоне от 32,0 до 35,4 ° C, а выше этой температуры образуется моногидрат. [13] В сухом воздухе декагидрат и гептагидрат теряют воду с образованием моногидрата. Сообщалось о других гидратах, например, с 2,5 единицами воды на единицу карбоната натрия («пентагемигидрат»). [14]
Стиральная сода [ править ]
Декагидрат карбоната натрия (Na 2 CO 3 · 10H 2 O), также известный как стиральная сода, является наиболее распространенным гидратом карбоната натрия, содержащим 10 молекул кристаллизационной воды . Кальцинированную соду растворяют в воде и кристаллизуют, чтобы получить стиральную соду.
- Это белое кристаллическое вещество.
- Это один из немногих карбонатов металлов , растворимых в воде.
- Щелочной с уровнем pH 11; он превращается из красной лакмусовой бумажки в синюю.
- Он обладает моющими или очищающими свойствами, поскольку может удалять грязь и жир с грязной одежды и т. Д. Он воздействует на грязь и жир с образованием водорастворимых продуктов, которые затем смываются при полоскании водой.
Приложения [ править ]
Некоторые общие применения карбоната натрия (или стиральной соды) включают:
- Карбонат натрия (или стиральная сода) используется в качестве очищающего средства в домашних целях, например, для стирки одежды. Карбонат натрия входит в состав многих сухих мыльных порошков.
- Используется для удаления временной и постоянной жесткости воды . [15] (см. Умягчение воды ).
- Его используют при производстве стекла , мыла и бумаги . (см. производство стекла )
- Он используется в производстве соединений натрия, таких как бура.
Производство стекла [ править ]
Карбонат натрия служит флюсом для кремнезема , понижая температуру плавления смеси до чего-то достижимого без специальных материалов. Это "содовое стекло" слабо растворимо в воде, поэтому в расплавленную смесь добавляют немного карбоната кальция, чтобы сделать стекло нерастворимым. Стекло для бутылок и окон ( натриево-известковое стекло ) изготавливается путем плавления таких смесей карбоната натрия, карбоната кальция и кварцевого песка ( диоксида кремния (SiO 2 )). Когда эти материалы нагреваются, карбонаты выделяют диоксид углерода. Таким образом, карбонат натрия является источником оксида натрия. Натриевое стекло на протяжении веков было самой распространенной формой стекла. [16]
Умягчение воды [ править ]
Жесткая вода содержит растворенные соединения, обычно соединения кальция или магния. Карбонат натрия используется для снятия временной и постоянной жесткости воды. [15]
В качестве карбоната натрия является водорастворимым и карбонат магния и карбонат кальция нерастворимы, поэтому он используется для смягчения воды путем удаления Mg 2+ и Ca 2+ . Эти ионы образуют нерастворимые твердые осадки при обработке карбонат- ионами:
По аналогии,
Вода смягчается, поскольку в ней больше нет растворенных ионов кальция и ионов магния. [15]
Пищевая добавка и приготовление пищи [ править ]
Карбонат натрия - это пищевая добавка (E500), используемая в качестве регулятора кислотности, антислеживающего агента, разрыхлителя и стабилизатора. Это один из компонентов кансуи (か ん 水) , раствора щелочных солей, используемых для придания лапше рамэн характерного вкуса и текстуры. Он используется в производстве снюса для стабилизации pH конечного продукта. Карбонат натрия используется при производстве порошка шербета . Ощущение охлаждения и шипения возникает в результате эндотермической реакции между карбонатом натрия и слабой кислотой, обычно лимонной кислотой., выделяя углекислый газ, который возникает при смачивании шербета слюной. В Китае его используют для замены щелочной воды в корке традиционных кантонских лунных пирожных , а также во многих других китайских булочках и лапше, приготовленных на пару. В кулинарии его иногда используют вместо гидроксида натрия для подкрашивания , особенно с немецкими кренделями и булочками с щелочью . Эти блюда обрабатывают раствором щелочного вещества, чтобы изменить pH поверхности продуктов и улучшить потемнение. Карбонат натрия вызывает коррозию алюминиевой посуды, посуды и фольги. [17]
Недорогая, слабая база [ править ]
Карбонат натрия также используется в качестве относительно сильного основания в различных областях. Как обычная щелочь, ее предпочитают во многих химических процессах, потому что она дешевле гидроксида натрия и намного безопаснее в обращении. Его мягкость особенно рекомендует его использование в домашних условиях.
Например, он используется в качестве регулятора pH для поддержания стабильных щелочных условий, необходимых для действия большинства проявителей фотопленки . Это также обычная добавка в плавательных бассейнах и аквариумной воде для поддержания желаемого pH и карбонатной жесткости (KH). При окрашивании красителями, реагирующими с волокнами, карбонат натрия (часто под названием, например, фиксатор кальцинированной соды или активатор кальцинированной соды) используется для обеспечения надлежащего химического связывания красителя с целлюлозными (растительными) волокнами, обычно перед окрашиванием (для связующих красок). , смешанный с красителем (для окрашивания красителем) или после окрашивания (для окрашивания иммерсией). Он также используется в процессе пенной флотации для поддержания благоприятногоpH в качестве плавающего кондиционера помимо CaO и других слабощелочных соединений.
Предшественник других соединений [ править ]
Натрия бикарбоната (NaHCO 3 ) или выпечки соды, а также компонент в огнетушителях, часто генерируется из карбоната натрия. Хотя NaHCO 3 сам по себе является промежуточным продуктом процесса Solvay, нагревание, необходимое для удаления загрязняющего его аммиака, разлагает некоторое количество NaHCO 3 , что делает более экономичным взаимодействие готового Na 2 CO 3 с CO 2 :
- Na 2 CO 3 + CO 2 + H 2 O → 2 NaHCO 3
В родственной реакции карбонат натрия используется для получения бисульфита натрия (NaHSO 3 ), который используется для «сульфитного» метода отделения лигнина от целлюлозы. Эта реакция используется для удаления диоксида серы из дымовых газов на электростанциях:
- Na 2 CO 3 + SO 2 + H 2 O → NaHCO 3 + NaHSO 3
Это приложение стало более распространенным, особенно там, где станции должны соответствовать строгим ограничениям выбросов.
Карбонат натрия используется в хлопковой промышленности для нейтрализации серной кислоты, необходимой для кислотной очистки нечетких семян хлопка.
Разное [ править ]
Карбонат натрия используется в кирпичной промышленности в качестве смачивающего агента для уменьшения количества воды, необходимой для экструзии глины. При отливке он называется «связующим агентом» и используется для того, чтобы влажный альгинат прилипал к гелеобразному альгинату. Карбонат натрия используется в зубных пастах, где он действует как пенообразователь и абразив, а также для временного повышения pH во рту.
Карбонат натрия также используется при обработке и дублении шкур животных. [ необходима цитата ]
Физические свойства [ править ]
Интегральная энтальпия раствора карбоната натрия составляет -28,1 кДж / моль для 10% -ного водного раствора. [18] Мооса твердость моногидрата карбоната натрия составляет 1,3. [6]
Встречается как природный минерал [ править ]
Карбонат натрия растворим в воде и может встречаться в естественных условиях в засушливых регионах, особенно в минеральных отложениях ( эвапоритах ), образующихся при испарении сезонных озер. Залежи минерального натрона добывались на дне сухих озер в Египте с древних времен, когда натрон использовался при приготовлении мумий и в раннем производстве стекла.
Безводная минеральная форма карбоната натрия встречается довольно редко и называется натритом. Карбонат натрия также извергается из Ол Доиньо Ленгаи , уникального вулкана Танзании, и предполагается, что он извергался из других вулканов в прошлом, но из-за нестабильности этих минералов на поверхности земли, вероятно, подвергнется эрозии. Все три минералогические формы карбоната натрия, а также трона , дигидрат тринатрийгидрогендикарбоната, также известны из ультращелочных пегматитовых пород , которые встречаются, например, на Кольском полуострове в России.
Известный инопланетный карбонат натрия встречается редко. Отложения были идентифицированы как источник ярких пятен на Церере , внутреннем материале, который был вынесен на поверхность. [19] Хотя на Марсе есть карбонаты , и ожидается, что они будут включать карбонат натрия, [20] отложения еще не подтверждены, это отсутствие объясняется некоторыми как глобальное преобладание низкого pH в ранее водной марсианской почве. . [21]
Производство [ править ]
Горное дело [ править ]
Трона , дигидрат тринатрийгидрогендикарбоната (Na 3 HCO 3 CO 3 · 2H 2 O), добывается в нескольких районах США и обеспечивает почти все внутреннее потребление карбоната натрия. Крупные природные месторождения, обнаруженные в 1938 году, такие как месторождение возле Грин-Ривер, штат Вайоминг , сделали добычу полезных ископаемых более экономичной, чем промышленное производство в Северной Америке. В Турции есть важные запасы троны; два миллиона тонн кальцинированной соды добыто из запасов под Анкарой. Его также добывают в некоторых щелочных озерах, таких как озеро Магади.в Кении дноуглубительными работами. Горячие солевые источники постоянно пополняют запас соли в озере, поэтому при условии, что скорость дноуглубительных работ не превышает скорость восполнения, источник является полностью устойчивым. [ необходима цитата ]
Барилла и водоросли [ править ]
Некоторые виды растений- галофитов и морских водорослей могут быть переработаны для получения неочищенной формы карбоната натрия, и эти источники преобладали в Европе и других странах до начала 19 века. Наземные растения (обычно солянки или солянки ) или водоросли (обычно виды фукусов ) собирали, сушили и сжигали. Затем золу « выщелачивали » (промывали водой) с образованием щелочного раствора. Этот раствор кипятили досуха, чтобы создать конечный продукт, который назвали «кальцинированной содой»; это очень старое название происходит от арабского слова сода , которое, в свою очередь, применяется к содовой сальсе., один из многих видов прибрежных растений, собираемых для выращивания. «Барилла» - это коммерческий термин, применяемый к нечистой форме калия, полученной из прибрежных растений или водорослей . [22]
Концентрация карбоната натрия в кальцинированной соде варьировалась в очень широких пределах: от 2–3 процентов для формы, полученной из морских водорослей (« ламинария »), до 30 процентов для лучшей бариллы, полученной из растений солянки в Испании. Источники кальцинированной соды, а также связанной с ней щелочи « поташ » из растений и морских водорослей , к концу 18 века становились все более неадекватными, и поиск коммерчески жизнеспособных путей синтеза кальцинированной соды из соли и других химикатов активизировался. [23]
Процесс Леблана [ править ]
В 1792 году французский химик Николя Леблан запатентовал процесс производства карбоната натрия из соли, серной кислоты , известняка и угля. На первом этапе хлорид натрия обрабатывают серной кислотой в процессе Мангейма . Эта реакция дает сульфат натрия ( соляной кек ) и хлористый водород :
- 2NaCl + H 2 SO 4 → Na 2 SO 4 + 2HCl
Соляной корок и измельченный известняк ( карбонат кальция ) восстанавливали нагреванием с углем . [16] Это преобразование состоит из двух частей. Во- первое это карботермическая реакция в результате чего угль, источник углерода , уменьшает в сульфат до сульфида :
- Na 2 SO 4 + 2C → Na 2 S + 2CO 2
Вторая стадия - это реакция с образованием карбоната натрия и сульфида кальция :
- Na 2 S + CaCO 3 → Na 2 CO 3 + CaS
Эта смесь называется черным ясенем . Кальцинированную соду извлекают из черной золы водой. Выпаривание этого экстракта дает твердый карбонат натрия. Этот процесс экстракции был назван выщелачиванием .
Соляная кислота, полученная в процессе Леблана, была основным источником загрязнения воздуха, а побочный продукт - сульфид кальция также создавал проблемы с удалением отходов. Однако он оставался основным методом производства карбоната натрия до конца 1880-х годов. [23] [24]
Процесс Solvay [ править ]
В 1861 году бельгийский промышленный химик Эрнест Сольвей разработал метод получения карбоната натрия путем взаимодействия хлорида натрия , аммиака , воды и углекислого газа с образованием бикарбоната натрия и хлорида аммония : [16]
- NaCl + NH 3 + CO 2 + H 2 O → NaHCO 3 + NH 4 Cl
Затем полученный бикарбонат натрия был преобразован в карбонат натрия путем его нагревания с выделением воды и диоксида углерода:
- 2NaHCO 3 → Na 2 CO 3 + H 2 O + CO 2
Между тем, аммиак регенерировали из побочного продукта хлорида аммония путем обработки его известью ( оксидом кальция ), оставшейся от образования диоксида углерода:
- 2NH 4 Cl + CaO → 2NH 3 + CaCl 2 + H 2 O
Процесс Solvay перерабатывает аммиак. Он потребляет только рассол и известняк, а хлорид кальция - единственный продукт его жизнедеятельности. Этот процесс значительно более экономичен, чем процесс Леблана, при котором образуются два продукта отходов: сульфид кальция и хлористый водород . Процесс Solvay быстро стал доминирующим в производстве карбоната натрия во всем мире. К 1900 году 90% карбоната натрия производилось с помощью процесса Solvay, а последний технологический завод Leblanc был закрыт в начале 1920-х годов. [16]
Вторая стадия процесса Solvay, нагревание бикарбоната натрия, в небольших масштабах используется домашними поварами и в ресторанах для приготовления карбоната натрия в кулинарии (включая крендели и щелочную лапшу). Этот метод привлекателен для таких пользователей, потому что бикарбонат натрия широко продается как пищевая сода, а температуры, необходимые (от 250 ° F (121 ° C) до 300 ° F (149 ° C)) для преобразования пищевой соды в карбонат натрия, легко достигаются. в обычных кухонных плитах . [25]
Процесс Хоу [ править ]
Этот процесс был разработан китайским химиком Хоу Дэбангом в 1930-х годах. Полученный ранее побочный продукт парового риформинга диоксид углерода прокачивали через насыщенный раствор хлорида натрия и аммиака для получения бикарбоната натрия по следующим реакциям:
- СН 4 + 2 Н 2 О → СО 2 + 4 Н 2
- 3 Н 2 + N 2 → 2 NH 3
- NH 3 + CO 2 + H 2 O → NH 4 HCO 3
- NH 4 HCO 3 + NaCl → NH 4 Cl + NaHCO 3
Бикарбонат натрия собирали в виде осадка из-за его низкой растворимости, а затем нагревали примерно до 80 ° C (176 ° F) или 95 ° C (203 ° F) с получением чистого карбоната натрия, аналогичного последней стадии процесса Сольвея. К оставшемуся раствору хлоридов аммония и натрия добавляют еще хлорид натрия; Кроме того, в этот раствор перекачивается больше аммиака при 30-40 ° C. Затем температуру раствора понижают до менее 10 ° C. Растворимость хлорида аммония выше, чем хлорида натрия при 30 ° C и ниже при 10 ° C. Из-за этой зависящей от температуры разницы растворимости и эффекта обычных ионов хлорид аммония осаждается в растворе хлорида натрия.
Китайское название процесса Хоу, lianhe zhijian fa (联合 制碱 法), означает «комбинированный щелочной метод производства»: процесс Хоу связан с процессом Хабера и предлагает лучшую атомную экономию за счет исключения производства хлорида кальция, поскольку аммиак больше не нужен быть восстановленным. Побочный продукт хлорида аммония может продаваться как удобрение.
См. Также [ править ]
- Натрон
- Индекс остаточного карбоната натрия
- Бикарбонат натрия
Ссылки [ править ]
- ^ а б в г Харпер, JP (1936). Антипов Евгений; Бисмайер, Ульрих; Гуппертц, Губерт; Петричек, Вацлав; Пёттген, Райнер; Шмаль, Вольфганг; Тикинк, ERT; Цзоу, Сяодун (ред.). «Кристаллическая структура моногидрата карбоната натрия, Na 2 CO 3. H 2 O» . Zeitschrift für Kristallographie - Кристаллические материалы . 95 (1): 266–273. DOI : 10.1524 / zkri.1936.95.1.266 . ISSN 2196-7105 . Проверено 25 июля 2014 .
- ^ a b c d e f g Лиде, Дэвид Р., изд. (2009). CRC Справочник по химии и физике (90-е изд.). Бока-Ратон, Флорида : CRC Press . ISBN 978-1-4200-9084-0.
- ^ a b Зейделл, Атертон; Линке, Уильям Ф. (1919). Растворимость неорганических и органических соединений (2-е изд.). Нью-Йорк : Компания Д. Ван Ностранд. п. 633 .
- ^ a b Коми, Артур Мессинджер; Хан, Дороти А. (февраль 1921 г.). Словарь химических растворимостей: неорганические (2-е изд.). Нью-Йорк: Компания MacMillan. С. 208–209.
- ^ a b c d Анатольевич, Кипер Руслан. «карбонат натрия» . chemister.ru . Проверено 25 июля 2014 .
- ^ a b c Прадёт, Патнаик (2003). Справочник неорганических химикатов . McGraw-Hill Companies, Inc. стр. 861. ISBN 978-0-07-049439-8.
- ^ a b c d Дусек, Михал; Шапюи, Жерве; Мейер, Матиас; Петричек, Вацлав (2003). «Новый взгляд на карбонат натрия» (PDF) . Acta Crystallographica Раздел B . 59 (3): 337–352. DOI : 10.1107 / S0108768103009017 . ISSN 0108-7681 . PMID 12761404 . Проверено 25 июля 2014 .
- ^ a b c Betzel, C .; Saenger, W .; Левус Д. (1982). «Гептагидрат карбоната натрия». Acta Crystallographica Раздел B . 38 (11): 2802–2804. DOI : 10.1107 / S0567740882009996 .
- ^ a b c Sigma-Aldrich Co. , Карбонат натрия . Проверено 6 мая 2014.
- ^ Чемберс, Майкл. «ChemIDplus - 497-19-8 - CDBYLPFSWZWCQE-UHFFFAOYSA-L - Карбонат натрия [NF] - Поиск похожих структур, синонимов, формул, ссылок на ресурсы и другой химической информации» .
- ^ "Паспорт безопасности материала - карбонат натрия, безводный" (PDF) . conservationsupportsystems.com . ConservationSupportSystems . Проверено 25 июля 2014 .
- ^ "Minerals.usgs.gov/minerals" (PDF) .
- ^ TWRichards и AH Fiske (1914). «О температурах перехода температур перехода гидратов карбоната натрия как фиксированных точках термометрии» . Журнал Американского химического общества . 36 (3): 485–490. DOI : 10.1021 / ja02180a003 .
- ^ А. Пабст. «О гидратах карбоната натрия» .[ постоянная мертвая ссылка ]
- ^ а б в https://www.ccmr.cornell.edu/wp-content/uploads/sites/2/2015/11/Water-Hardness-Reading.pdf
- ^ a b c d Кристиан Тим (2000). «Карбонаты натрия». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a24_299 . ISBN 978-3527306732.
- ^ «Карбонат натрия» . Корорпедия . Janalta Interactive . Дата обращения 9 ноября 2020 .
- ^ "Tatachemicals.com/north-america/product/images/fig_2_1.jpg" .
- ^ Де Санктис, MC; и другие. (29 июня 2016 г.). «Яркие карбонатные отложения как свидетельство водного изменения на (1) Церере». Природа . 536 (7614): 54–57. Bibcode : 2016Natur.536 ... 54D . DOI : 10.1038 / nature18290 . PMID 27362221 . S2CID 4465999 .
- ↑ Джеффри С. Каргель (23 июля 2004 г.). Марс - более теплая и влажная планета . Springer Science & Business Media. С. 399–. ISBN 978-1-85233-568-7.
- ^ Гротцингер, Дж. И Р. Милликен (ред.) 2012. Осадочная геология Марса. SEPM
- ^ Хупер, Роберт (1802). Lexicon Medicum (изд. 1848 г.). Лондон: Лонгман. С. 1198–9. OCLC 27671024 .
- ^ a b Клоу, Арчибальд и Клоу, Нэн Л. (1952). Химическая революция, (Ayer Co Pub, июнь 1952 г.), стр. 65–90. ISBN 0-8369-1909-2 .
- ↑ Кифер, Дэвид М. (январь 2002 г.). «Все дело в щелочах» . Сегодняшний химик за работой . 11 (1): 45–6.
- ↑ Макги, Гарольд (24 сентября 2010 г.). «Для старомодного вкуса испеките пищевую соду» . Нью-Йорк Таймс . Проверено 25 апреля 2019 года .
Дальнейшее чтение [ править ]
- Эггеман, Т. (2011). "Карбонат натрия". Энциклопедия химической технологии Кирка-Отмера . DOI : 10.1002 / 0471238961.1915040918012108.a01.pub3 . ISBN 978-0471238966.
- Тиме, К. (2000). «Карбонаты натрия». Энциклопедия промышленной химии Ульмана . DOI : 10.1002 / 14356007.a24_299 . ISBN 978-3527306732.
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме карбоната натрия . |
- Американская компания по производству кальцинированной соды
- Международная карта химической безопасности 1135
- FMC Wyoming Corporation
- Использование карбоната натрия при крашении
- Производство карбоната натрия синтетическими методами



