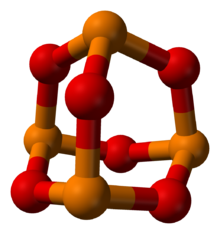
 Фосфор в оранжевом, кислород в красном | |
 | |
| Имена | |
|---|---|
| Другие имена | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.032.414 |
PubChem CID | |
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| P 4 O 6 | |
| Молярная масса | 219,88 г моль -1 |
| Внешность | бесцветные моноклинные кристаллы или жидкость |
| Плотность | 2,135 г / см 3 |
| Температура плавления | 23,8 ° С (74,8 ° F, 296,9 К) |
| Точка кипения | 173,1 ° С (343,6 ° F, 446,2 К) |
| реагирует | |
| Кислотность (p K a ) | 9,4 |
| Структура | |
| См. Текст | |
| 0 | |
| Опасности | |
Классификация ЕС (DSD) (устарела) | Токсичный (T +) |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Другие анионы | Трисульфид фосфора |
Другие катионы | Триоксид диазота Триоксид мышьяка Триоксид сурьмы |
Родственные соединения | Пятиокись фосфора Фосфорная кислота |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Триоксид фосфора - это химическое соединение с молекулярной формулой P 4 O 6 . Хотя молекулярная формула предполагает название гексоксид тетрафосфора, название триоксид фосфора предшествовало знанию молекулярной структуры соединения, и его использование продолжается и сегодня. Это бесцветное твердое вещество структурно связано с адамантаном . Это формально ангидрид из фосфористой кислоты , H 3 PO 3 , но не могут быть получены путем дегидратации кислоты. Это белое твердое вещество, плавящееся при комнатной температуре, воскообразное, кристаллическое и высокотоксичное твердое вещество с запахом чеснока. [1]
Подготовка [ править ]
Его получают путем сжигания фосфора в ограниченном количестве воздуха при низкой температуре.
- P 4 + 3 O 2 → P 4 O 6
Побочные продукты включают недокись красного фосфора. [1]
Химические свойства [ править ]
Триоксид фосфора реагирует с водой с образованием фосфористой кислоты , что отражает тот факт, что это ангидрид этой кислоты. [2]
- P 4 O 6 + 6 H 2 O → 4 H 3 PO 3
Он реагирует с хлористым водородом с образованием H 3 PO 3 и трихлорида фосфора .
- P 4 O 6 + 6 HCl → 2 H 3 PO 3 + 2 PCl 3
С хлором или бромом он образует соответствующий фосфорилгалогенид и реагирует с йодом в запаянной трубке с образованием тетраиодида дифосфора . [1]
P 4 O 6 реагирует с озоном при 195 K с образованием нестабильного соединения P 4 O 18 . [3]
P 4 O 18 разлагается в растворе при температуре выше 238 K с выделением газообразного O 2 . Разложение сухого P 4 O 18 взрывоопасно.
В реакции диспропорционирования P 4 O 6 превращается в смешанный P (III) P (V) P 4 O 8 при нагревании в запаянной трубке до 710 K, причем побочным продуктом является красный фосфор. [3]
Как лиганд [ править ]
P 4 O 6 - лиганд переходных металлов, сравнимый с фосфитом . Иллюстративный комплекс представляет собой P 4 O 6 · Fe (CO) 4 . [4] С BH 3 образуется димерный аддукт: [3]
- Структура P 8 O 12 (BH 3 ) 2 .
Ссылки [ править ]
- ^ a b c А. Ф. Холлеман; Виберг, Эгон; Виберг, Нильс (2001). Неорганическая химия . Бостон: Academic Press. ISBN 0-12-352651-5.
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- ^ а б в . Кэтрин Э. Хаукрофт; Алан Г. Шарп (2008). «Глава 15: Группа 15 элементов». Неорганическая химия, 3-е издание . Пирсон. п. 473. ISBN 978-0-13-175553-6.
- ^ М. Янсен и Дж. Клэйд (ноябрь 1996 г.). «Тетракарбонил (гексаоксид тетрафосфора) железо» . Acta Crystallogr. C . 52 (11): 2650–2652. DOI : 10.1107 / S0108270196004398 .
