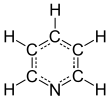
Пиридин
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Пиридин [1] | |||
| Систематическое название ИЮПАК Азабензол | |||
| Другие имена Азин Азинин 1-Азациклогекса-1,3,5-триен | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.464 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 5 H 5 N | |||
| Молярная масса | 79,102 г · моль -1 | ||
| Появление | Бесцветная жидкость [2] | ||
| Запах | Тошнотворное, похожее на рыбу [3] | ||
| Плотность | 0,9819 г / мл [4] | ||
| Температура плавления | -41,6 ° С (-42,9 ° F, 231,6 К) | ||
| Точка кипения | 115,2 ° С (239,4 ° F, 388,3 К) | ||
| Смешиваемый | |||
| журнал P | 0,73 [5] | ||
| Давление газа | 16 мм рт. Ст. (20 ° C) [3] | ||
| Основность (p K b ) | 8,77 [6] | ||
| Конъюгированная кислота | Пиридиний | ||
Показатель преломления ( n D ) | 1,5093 | ||
| Вязкость | 0,88 сП 25 ℃ | ||
Дипольный момент | 2.2 D [7] | ||
| Опасности [10] | |||
| Паспорт безопасности | См .: страницу данных | ||
| Пиктограммы GHS | [8] | ||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H225 , H302 , H312 , H332 , H315 , H319 [8] | ||
Меры предосторожности GHS | P210 , P280 , P301 + 312 , P303 + 361 + 353 , P304 + 340 + 312 , P305 + 351 + 338 [8] | ||
| NFPA 704 (огненный алмаз) |  2 3 0 | ||
| точка возгорания | 21 ° С (70 ° F, 294 К) | ||
| Пределы взрываемости | 1,8–12,4% [3] | ||
Пороговое предельное значение (ПДК) | 5 частей на миллион (TWA) | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 891 мг / кг (крыса, перорально) 1500 мг / кг (мышь, перорально) 1580 мг / кг (крыса, перорально) [9] | ||
ЛК 50 ( средняя концентрация ) | 9000 частей на миллион (крыса, 1 час) [9] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 5 частей на миллион (15 мг / м 3 ) [3] | ||
REL (рекомендуется) | TWA 5 частей на миллион (15 мг / м 3 ) [3] | ||
IDLH (Непосредственная опасность) | 1000 частей на миллион [3] | ||
| Родственные соединения | |||
Родственные амины | пиколин хинолин | ||
Родственные соединения | Анилин Пиримидин Пиперидин | ||
| Страница дополнительных данных | |||
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. | ||
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ | ||
Спектральные данные | УФ , ИК , ЯМР , МС | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Пиридин - это основное гетероциклическое органическое соединение с химической формулой C5ЧАС5N . Он структурно связан с бензолом , с одной метиновой группой (= CH-), замещеннойатомом азота . Это легковоспламеняющаяся, слабощелочная , смешивающаяся с водой жидкость с характерным неприятным запахом рыбы. Пиридин бесцветен, но старые или нечистые образцы могут иметь желтый цвет. Пиридиновое кольцо присутствует во многих важных соединениях, включая агрохимикаты , фармацевтические препараты и витамины . Исторически пиридин производился из каменноугольной смолы . По состоянию на 2016 год он синтезируется в масштабе около 20 000 тонн в год во всем мире. [2]
Характеристики
Физические свойства
Молекулярный электрический дипольный момент составляет 2,2 дебай . [7] Пиридин диамагнитен и имеет диамагнитную восприимчивость -48,7 × 10 -6 см 3 · моль -1 . [12] стандартная энтальпия образования составляет 100,2 кДж · моль -1 в жидкой фазе [13] и 140,4 кДж · моль -1 в газовой фазе. При 25 ° C пиридин имеет вязкость [14] 0,88 мПа / с и теплопроводность 0,166 Вт · м -1 · К -1 . [15] [8]Энтальпия испарения является 35.09 кДж · моль -1 при температуре кипения и нормальном давлении. [16] энтальпия плавления составляет 8,28 кДж · моль -1 при температуре плавления . [17]
Эти критические параметры пиридина давление 6,70 МПа, температура 620 К и объем 229 см 3 · моль -1 . [18] В интервале температур 340–426 ° C его давление пара p можно описать уравнением Антуана.
где T - температура, A = 4,16272, B = 1371,358 K и C = -58,496 K. [19]
Состав
Пиридиновый цикл образует C
5Шестигранник N. Наблюдаются небольшие изменения расстояний C − C и C − N, а также валентных углов.
Кристаллография
Пиридин кристаллизуется в орторомбической кристаллической системе с пространственной группой Pna2 1 и параметрами решетки a = 1752 пм , b = 897 пм, c = 1135 пм и 16 формульных единиц на элементарную ячейку (измерено при 153 К). Для сравнения, кристаллический бензол также является ромбическим, с пространственной группой Pbca , a = 729,2 пм, b = 947,1 пм, c = 674,2 пм (при 78 К), но количество молекул на ячейку составляет всего 4. [11]Это различие частично связано с более низкой симметрией отдельной молекулы пиридина (C 2v против D 6h для бензола). Известен тригидрат (пиридин · 3H 2 O); он также кристаллизуется в орторомбической системе в пространственной группе Pbca , параметры решетки a = 1244 пм, b = 1783 пм, c = 679 пм и восемь формульных единиц на элементарную ячейку (измерено при 223 К). [20]
Спектроскопия
Спектр оптического поглощения пиридина в гексане содержит три полосы на длинах волн 195 нм (переход π → π *, молярная поглощающая способность ε = 7500 л · моль −1 · см −1 ), 251 нм (переход π → π *, ε = 2000 л · моль -1 · см -1 ) и 270 нм (переход n → π *, ε = 450 л · моль -1 · см -1 ). [21] 1 Н ядерного магнитного резонанса(ЯМР) спектр пиридина содержит три сигнала с соотношением интегральных интенсивностей 2: 1: 2, которые соответствуют трем химически различным протонам в молекуле. Эти сигналы исходят от α-протонов (положения 2 и 6, химический сдвиг 8,5 м.д.), γ-протонов (положение 4, 7,5 м.д.) и β-протонов (положения 3 и 5, 7,1 м.д.). Углеродный аналог пиридина, бензол, имеет только один сигнал протона при 7,27 м.д. Большие химические сдвиги α- и γ-протонов по сравнению с бензолом являются результатом более низкой электронной плотности в α- и γ-положениях, что может быть получено из резонансных структур. Для спектров ЯМР 13 C пиридина и бензола ситуация довольно похожа : пиридин имеет триплет при δ(α-C) = 150 частей на миллион, δ (β-C) = 124 частей на миллион и δ (γ-C) = 136 частей на миллион, тогда как бензол имеет единственную линию при 129 частях на миллион. Все смены указаны для веществ, не содержащих растворителей. [22] Пиридин обычно обнаруживают методами газовой хроматографии и масс-спектрометрии . [23]
Химические свойства
Из-за электроотрицательного азота в пиридиновом кольце молекула относительно электронодефицитна. Следовательно, он менее легко вступает в реакции электрофильного ароматического замещения, чем производные бензола. Соответственно, пиридин более склонен к нуклеофильному замещению , о чем свидетельствует легкость металлирования сильными металлоорганическими основаниями. [24] [25] По реакционной способности пиридин можно выделить три химические группы. С электрофильными , электрофильное замещение имеет место , где пиридин выражающее ароматические свойства. С нуклеофиламипиридин реагирует в положениях 2 и 4 и, таким образом, ведет себя аналогично иминам и карбонилам . Реакция со многими кислотами Льюиса приводит к присоединению к атому азота пиридина, что аналогично реакционной способности третичных аминов. Способность пиридина и его производных окисляться с образованием оксидов аминов ( N- оксидов) также является особенностью третичных аминов. [26]
Центр азота пиридина имеет основную одну пару из электронов . Эта неподеленная пара не перекрывается с кольцом ароматической π-системы, следовательно, пиридин является основным , имеющим химические свойства, аналогичные свойствам третичных аминов . Протонирование дает пиридиний , С 5 Н 5 NH + .The р К из сопряженной кислоты (пиридиния катионов) составляет 5,25. Строения пиридина и пиридиния практически идентичны. [27] Катион пиридиния изоэлектронен бензолу. Пиридиний p- толуолсульфонат (PPTS) представляет собой иллюстративную соль пиридиния; его получают обработкой пиридина п- толуолсульфоновой кислотой . Помимо протонирования , пиридин подвергается N-центрированному алкилированию , ацилированию и N- окислению .
Склеивание
Пиридин имеет сопряженную систему из шести π-электронов , которые делокализованы по кольцу. Молекула плоская и, таким образом, следует критериям Хюккеля для ароматических систем. В отличие от бензола, электронная плотность распределена по кольцу неравномерно, что отражает отрицательный индуктивный эффект атома азота. По этой причине пиридин имеет дипольный момент и более слабую резонансную стабилизацию, чем бензол ( резонансная энергия 117 кДж · моль -1 в пиридине против 150 кДж · моль -1 в бензоле). [28]
Атомы кольца в молекуле пиридина являются sp 2 -гибридизированными . Азот участвует в π-связывающей ароматической системе, используя свою негибридизированную p-орбиталь. Неподеленной пары находится в зр 2 орбитали, выступающие наружу от кольца в одной и той же плоскости, что и сг облигаций . В результате неподеленная пара не вносит вклад в ароматическую систему, но существенно влияет на химические свойства пиридина, поскольку она легко поддерживает образование связи посредством электрофильной атаки. Однако из-за отделения неподеленной пары от ароматической кольцевой системы атом азота не может проявлять положительный мезомерный эффект .
Известно много аналогов пиридина, в которых N замещен другими гетероатомами (см. Рисунок ниже). Замена одного C – H в пиридине на второй N дает диазиновые гетероциклы (C 4 H 4 N 2 ) с названиями пиридазин , пиримидин и пиразин .
Длины связей и углы бензол, пиридин, phosphorine , arsabenzene , stibabenzene и bismabenzene | Атомные орбитали в пиридине |
Резонансные структуры пиридина | Атомные орбитали в протонированном пиридине |
История
Нечистый пиридин, несомненно, был получен ранними алхимиками путем нагревания костей животных и других органических веществ [29], но самое раннее задокументированное упоминание приписывается шотландскому ученому Томасу Андерсону . [30] [31] В 1849 году Андерсон исследовал содержание масла, полученного при высокотемпературном нагревании костей животных. [31] Среди других веществ он выделил из масла бесцветную жидкость с неприятным запахом, из которой два года спустя выделил чистый пиридин. Он описал его как хорошо растворимый в воде, легко растворимый в концентрированных кислотах и солях при нагревании и мало растворимый в маслах.
Из-за его воспламеняемости Андерсон назвал новое вещество пиридином в честь греческого : πῦρ (пир), что означает огонь . Суффикс идин был добавлен в соответствии с химической номенклатурой, как в толуидине , для обозначения циклического соединения, содержащего атом азота. [32] [33]
Химическая структура пиридина была определена спустя десятилетия после его открытия. Вильгельм Кёрнер (1869) [34] и Джеймс Дьюар (1871) [35] [36] предположили, что, по аналогии между хинолином и нафталином , структура пиридина образована из бензола путем замены одного C – H звена на атом азота. [37] [38] Предположение Кёрнера и Дьюара было позже подтверждено в эксперименте, в котором пиридин был восстановлен до пиперидина с натрием в этаноле . [39] В 1876 году Уильям Рамзи объединилацетилен и цианистый водород в пиридин в раскаленной железной трубчатой печи. [40] Это был первый синтез гетероароматического соединения. [23] [41]
Первый крупный синтез производных пиридина был описан в 1881 году Артуром Рудольфом Ганчем . [42] В синтезе пиридина по Ганцу обычно используется смесь 2: 1: 1 β- кетокислоты (часто ацетоацетат ), альдегида (часто формальдегида ) и аммиака или его соли в качестве донора азота. Сначала получают двойной гидрированный пиридин, который затем окисляют до соответствующего производного пиридина. Эмиль Кневенагель показал, что с помощью этого процесса могут быть получены асимметрично-замещенные производные пиридина. [43]
Современные методы производства пиридина имели низкий выход, и растущий спрос на новое соединение побудил искать более эффективные пути. Прорыв произошел в 1924 году, когда русский химик Алексей Чичибабин изобрел реакцию синтеза пиридина , в основе которой лежали недорогие реагенты. [44] Этот метод до сих пор используется для промышленного производства пиридина. [2]
Вхождение
Пиридина в природе мало, за исключением листьев и корней красавки ( Atropa belladonna ) [45] и зефира ( Althaea officinalis ). [46] Производные пиридина, однако, часто входят в состав биомолекул, таких как алкалоиды .
В повседневной жизни, следовые количества пиридина являются компонентами летучих органических соединений , которые образуются в обжиге и консервировании процессов, например , в жареной курице, [47] сукияки , [48] жареный кофе, [49] картофельные чипсы, [50] и жареный бекон . [51] Следы пиридина можно найти в сыре Бофорт , [52] вагинальных выделениях , [53] черном чае , [54] слюне людей, страдающих гингивитом , [55] и подсолнечном меде .[56]
4-бромпиридин
2,2'- бипиридин
пиридин-2,6-дикарбоновая кислота ( дипиколиновая кислота )
Общая форма катиона пиридиния
Производство
Исторически пиридин извлекали из каменноугольной смолы или получали как побочный продукт газификации угля . Процесс был трудоемким и неэффективным: каменноугольная смола содержит только около 0,1% пиридина [57], поэтому требовалась многоступенчатая очистка, которая дополнительно снижала выход. В настоящее время большая часть пиридина производится синтетически с использованием различных именных реакций , основные из которых обсуждаются ниже. [2]
В 1989 году во всем мире было произведено 26 000 тонн пиридина. [2] Среди 25 крупнейших предприятий по производству пиридина одиннадцать расположены в Европе (по состоянию на 1999 год). [23] Основные производители пиридина включают Evonik Industries , Rütgers Chemicals, Jubilant Life Sciences, Imperial Chemical Industries и Koei Chemical. [2] Производство пиридина значительно увеличилось в начале 2000-х, с годовой производственной мощностью 30 000 тонн только в материковом Китае. [58] Совместное американо-китайское предприятие Vertellus в настоящее время является мировым лидером в производстве пиридина. [59]
Синтез чичибабина
О синтезе пиридина Чичибабина сообщили в 1924 году, и он до сих пор используется в промышленности. [44] В общем виде реакци может быть описана как реакции конденсации с альдегидами , кетонами , & alpha ; , & beta; ненасыщенными карбонильными соединениями , или любой комбинации вышеуказанного, в аммиака или аммиака производных . [60] В частности, незамещенный пиридин получают из формальдегида и ацетальдегида , которые недороги и широко доступны. Сначала акролеин образуется при конденсации Кневенагеля.из ацетальдегида и формальдегида. Затем акролеин конденсируется с ацетальдегидом и аммиаком с образованием дигидропиридина , который окисляется твердотельным катализатором до пиридина. Этот процесс осуществляется в газовой фазе при 400–450 ° C. Продукт состоит из смеси пиридина, простых метилированных пиридинов ( пиколинов и лутидинов ); его состав зависит от используемого катализатора и может быть адаптирован к потребностям производителя. Катализатор обычно представляет собой соль переходного металла, такую как фторид кадмия (II) или фторид марганца (II) , но кобальт и таллий.также могут быть использованы соединения. Восстановленный пиридин отделяется от побочных продуктов в многоступенчатом процессе. [2]
Практическое применение традиционного синтеза пиридина Чичибабина ограничено его стабильно низким выходом, обычно около 20%. Этот низкий выход вместе с высоким преобладанием побочных продуктов делает немодифицированные формы метода Чичибабина непопулярными. [60]
Деалкилирование алкилпиридинов
Пиридин можно получить деалкилированием алкилированных пиридинов, которые получаются как побочные продукты при синтезе других пиридинов. Окислительное деалкилирование проводят либо с использованием катализатора на основе воздуха над оксидом ванадия (V) [61], либо путем деалкилирования паром на катализаторе на основе никеля , [62] [63] или гидродеалкилирования с использованием катализатора на основе серебра или платины . [64] Выход пиридина до 93% может быть достигнут с катализатором на основе никеля. [2]
Циклизация Беннемана
Тримеризация части молекулы нитрила и двух частей ацетилена в пиридин называется циклизацией Беннемана . Эта модификация синтеза Reppe может быть активирована либо теплом, либо светом . В то время как термическая активация требует высоких давлений и температур, фотоиндуцированное циклоприсоединение протекает в условиях окружающей среды с CoCp 2 (треска) (Cp = циклопентадиенил, cod = 1,5-циклооктадиен ) в качестве катализатора и может осуществляться даже в воде. [65] Таким способом можно получить ряд производных пиридина. При использовании ацетонитрила в качестве нитрила получают 2-метилпиридин, который можно деалкилировать до пиридина.
Другие методы
Синтез пиридина Kröhnke обеспечивает достаточно общий способ генерации замещенных пиридинов с использованием пиридина в качестве реагента , который не становится включен в конечный продукт. Реакция пиридина с α-бромовыми эфирами дает родственную соль пиридиния , в которой метиленовая группа является сильно кислой. Этот вид претерпевает присоединение типа Михаэля к α, β-ненасыщенным карбонилам в присутствии ацетата аммония, чтобы претерпеть замыкание цикла и образование целевого замещенного пиридина, а также бромида пиридиния. [66]
Перегруппировки Ciamician-Dennstedt влечет за собой кольцевое расширение пиррола с дихлоркарбена к 3-хлорпиридину . [67] [68] [69]
В синтезе Гаттермана-Skita , [70] через малонат сложного эфира соли реагирует с дихлор метиламина . [71]
Другой метод - синтез пиридина Богера .
Пиридин может быть также получен путем декарбоксилирования никотиновой кислоты с хромитом меди . [72]
Биосинтез
Некоторые производные пиридина играют важную роль в биологических системах. Хотя его биосинтез полностью не изучен, никотиновая кислота (витамин B 3 ) содержится в некоторых бактериях , грибах и млекопитающих . Млекопитающие синтезируют никотиновую кислоту путем окисления аминокислоты триптофана , при этом промежуточный продукт, анилин , создает производное пиридина, кинуренин . Напротив, бактерии Mycobacterium tuberculosis и Escherichia coli производят никотиновую кислоту путем конденсации глицеральдегид-3-фосфата и аспарагиновой кислоты.. [73]
Реакции
Несмотря на общие структурные и связывающие черты бензола и пиридина, их реакционная способность значительно различается. Напротив, по своей реакционной способности пиридин больше похож на нитробензол . [74]
Электрофильные замещения
Из-за пониженной электронной плотности в ароматической системе электрофильные замещения в пиридине и его производных подавляются. Алкилирование или ацилирование Фриделя-Крафтса обычно не дает пиридина, потому что они приводят только к присоединению по атому азота. Замещения обычно происходят в 3-м положении, которое является наиболее богатым электронами атомом углерода в кольце и, следовательно, более восприимчивым к электрофильному присоединению.
Прямое нитрование пиридина происходит вяло. [75] [76] Производные пиридина, в которых атом азота подвергается стерической и / или электронной экранировке, могут быть получены нитрованием тетрафторборатом нитрония (NO 2 BF 4 ). Таким образом, 3-нитропиридин может быть получен путем синтеза 2,6-дибромпиридина с последующим дебромированием. [77] [78]
Сульфирование пиридина даже сложнее нитрования. Однако можно получить пиридин-3-сульфоновую кислоту. Реакция с группой SO 3 также облегчает добавление серы к атому азота, особенно в присутствии катализатора на основе сульфата ртути (II) . [24] [79]
В отличие от медленных процессов нитрования и сульфирования, бромирование и хлорирование пиридина протекают хорошо. [2]
Пиридин-N-оксид
Окисление пиридина происходит при азоте с образованием пиридин-N-оксида. Окисление может быть достигнуто с помощью перкислоты : [80]
- C 5 H 5 N + RCO 3 H → C 5 H 5 NO + RCO 2 H
Некоторые электрофильные замены пиридина эффективно осуществляются с использованием пиридин- N- оксида с последующим дезоксигенированием. Добавление кислорода подавляет дальнейшие реакции по атому азота и способствует замещению по 2- и 4-углеродным атомам. Затем атом кислорода можно удалить, например, с помощью цинковой пыли. [81]
Нуклеофильные замены
В отличие от бензольного кольца пиридин эффективно поддерживает несколько нуклеофильных замещений. Причина этого - относительно более низкая электронная плотность атомов углерода кольца. Эти реакции включают замещения с отщеплением гидрид- иона и присоединения с отщеплением с образованием промежуточной конфигурации арина и обычно протекают в 2- или 4-положении. [24] [25]
Многие нуклеофильные замены легче происходят не с чистым пиридином, а с пиридином, модифицированным бромом, хлором, фтором или фрагментами сульфоновой кислоты, которые затем становятся уходящей группой. Таким образом, фтор является лучшей уходящей группой для замещения литийорганическими соединениями . Нуклеофильные атакующие соединения могут представлять собой алкоксиды , тиолаты, амины и аммиак (при повышенном давлении). [82]
Как правило, ион гидрида является плохо уходящей группой и встречается только в нескольких гетероциклических реакциях. Они включают реакцию Чичибабина , которая дает производные пиридина, аминированные по 2-положению. Здесь амид натрия используется в качестве нуклеофила, дающего 2-аминопиридин. Ион гидрида, высвобождаемый в этой реакции, соединяется с протоном доступной аминогруппы, образуя молекулу водорода. [25] [83]
Аналогично бензол, реакции нуклеофильного замещения в пиридине может привести к образованию pyridyne промежуточных соединений в качестве гетероатома ариновым . Для этой цели производные пиридина могут быть удалены с хорошими уходящими группами с использованием сильных оснований, таких как трет-бутоксид натрия и калия . Последующее присоединение нуклеофила к тройной связи имеет низкую селективность, и в результате получается смесь двух возможных аддуктов. [24]
Радикальные реакции
Пиридин поддерживает ряд радикальных реакций, которые используются при его димеризации до бипиридинов. Радикальные димеризации пиридина с элементарным натрием или никелем Ренея селективно дает 4,4'-бипиридин , [84] или 2,2'-бипиридин , [85] , которые являются важными реагентами - предшественников в химической промышленности. Одна из реакций имен с участием свободных радикалов является реакция миниски . Он может производить 2- трет- бутилпиридин при взаимодействии пиридина с пивалевой кислотой , нитратом серебра и аммонием в серной кислоте.с доходностью 97%. [24]
Реакции на атоме азота
Кислоты Льюиса легко присоединяются к атому азота пиридина, образуя соли пиридиния. Реакция с алкилгалогенидами приводит к алкилированию атома азота. Это создает положительный заряд в кольце, который увеличивает реакционную способность пиридина как к окислению, так и к восстановлению. Реакция Цинке используется для селективного введения радикалов в соединения пиридиния (не имеет отношения к химическому элементу цинку ).
Гидрирование и восстановление
Пиперидин получают путем гидрирования пиридина с катализатором на основе никеля , кобальта или рутения при повышенных температурах. [86] Гидрирование пиридина до пиперидина высвобождает 193,8 кДж · моль -1 , [87] что немного меньше энергии гидрирования бензола (205,3 кДж · моль -1 ). [87]
Частично гидрированные производные получают в более мягких условиях. Например, восстановление алюмогидридом лития дает смесь 1,4-дигидропиридина, 1,2-дигидропиридина и 2,5-дигидропиридина. [88] Селективный синтез 1,4-дигидропиридина достигается в присутствии металлоорганических комплексов магния и цинка , [89] и (Δ3,4) -тетрагидропиридин получают электрохимическим восстановлением пиридина. [90]
Основность Льюиса и координационные соединения
Пиридин - это основание Льюиса , которое отдает свою пару электронов кислоте Льюиса. Его базовые свойства Льюиса обсуждаются в модели ECW . Его относительная донорская сила по отношению к ряду кислот по сравнению с другими основаниями Льюиса может быть проиллюстрирована графиками CB . [91] [92] Одним из примеров является комплекс триоксида серы и пиридина (точка плавления 175 ° C), который представляет собой агент сульфатирования, используемый для преобразования спиртов в сложные эфиры сульфатов . Пиридин - боран ( С
5ЧАС
5NBH
3, точка плавления 10–11 ° C) - мягкий восстановитель.
Пиридиновые комплексы переходных металлов многочисленны. [93] [94]
Типичные октаэдрические комплексы имеют стехиометрию MCl
2(ру)
4и MCl
3(ру)
3. Октаэдрические гомолептические комплексы типа M (py)+
6редки или имеют тенденцию к диссоциации пиридина. Известны многочисленные плоские квадратные комплексы, такие как катализатор Крэбтри . [95] Пиридиновый лиганд, замененный в ходе реакции, восстанавливается после ее завершения.
Режим координации η 6 , как и в бензольных комплексах η 6 , наблюдается только в производных с пространственными ограничениями , которые блокируют азотный центр. [96]
Приложения
Пестициды
В основном пиридин используется как предшественник гербицидов паракват и дикват . [2] Первая стадия синтеза инсектицида хлорпирифоса состоит из хлорирования пиридина. Пиридин также является исходным соединением для получения фунгицидов на основе пиритиона . [23] Цетилпиридиний и лаурилпиридиний, которые могут быть получены из пиридина с помощью реакции Цинке , используются в качестве антисептиков в продуктах для ухода за полостью рта и зубов. [7] Пиридин легко разрушается алкилирующими агентами с образованием солей N- алкилпиридиния. Одним из примеров является цетилпиридиния хлорид .
Растворитель
Пиридин используется как полярный щелочной растворитель с низкой реакционной способностью, например, при конденсации Кнёвенагеля . [23] Он особенно подходит для дегалогенирования, где он действует как основа реакции элиминирования и связывает полученный галогенид водорода с образованием соли пиридиния. При этерификации и ацилировании пиридин активирует галогениды или ангидриды карбоновых кислот . Еще более активными в этих реакциях являются производные пиридина 4-диметиламинопиридин (DMAP) и 4- (1-пирролидинил) пиридин. Пиридин также используется в качестве основания в реакциях конденсации . [98]
Он также используется в текстильной промышленности для увеличения пропускной способности хлопковых сетей. [7]
Специальные реагенты на основе пиридина
В качестве основания в качестве реагента Карла Фишера можно использовать пиридин , но его обычно заменяют альтернативами с более приятным запахом, такими как имидазол . [99]
Хлорхромат пиридиния , дихромат пиридиния и реагент Коллинза (комплекс оксида хрома (VI) используются для окисления спиртов. [100]
Опасности
Пиридин - ядовитая легковоспламеняющаяся жидкость с сильным и неприятным запахом рыбы. Его пороговое значение запаха от 0,04 до 20 частей на миллион близко к пороговому пределу в 5 частей на миллион для побочных эффектов [101], таким образом, большинство (но не все) взрослые люди смогут определить, когда он присутствует в опасных количествах. Пиридин легко растворяется в воде и наносит вред как животным, так и растениям в водных системах. [102]
Огонь
Пиридин имеет температуру вспышки 17 ° C и поэтому легко воспламеняется. При сгорании образуются токсичные пары, которые могут включать бипиридины , оксиды азота и монооксид углерода . [8]
Кратковременное воздействие
Пиридин может вызвать химические ожоги при контакте с кожей, а его пары могут вызывать раздражение глаз или при вдыхании. [103] Пиридин угнетает нервную систему, вызывая симптомы, похожие на интоксикацию, концентрация паров выше 3600 ppm представляет больший риск для здоровья. [2] Эффекты могут проявляться с задержкой на несколько часов и включать головокружение, головную боль, нарушение координации , тошноту, слюноотделение и потерю аппетита. Они могут перерасти в боль в животе, заложенность легких и потерю сознания. [104] Самая низкая известная летальная доза (LD Lo) при приеме внутрь пиридина человеком составляет 500 мг · кг -1 .
Долгосрочное воздействие
Продолжительное воздействие пиридина может привести к повреждению печени, сердца и почек. [8] [23] [105] Оценки в качестве возможного канцерогенного агента показали, что у людей недостаточно данных о канцерогенности пиридина, хотя имеется достаточно доказательств на экспериментальных животных. Таким образом, IARC считает пиридин канцерогенным веществом для человека (группа 2B). [106]
Вхождение
В табачном дыме были обнаружены следовые количества до 16 мкг · м -3 . [23] Незначительные количества пиридина выбрасываются в окружающую среду в результате некоторых промышленных процессов, таких как производство стали, [107] переработка горючего сланца , газификация угля , коксование и мусоросжигательные заводы . [23] Атмосфера на заводах по переработке горючего сланца может содержать концентрации пиридина до 13 мкг · м -3 , [108] и 53 мкг · м -3 уровни были измерены в подземных водах вблизи завода по газификации угля. [109]Согласно исследованию Национального института безопасности и гигиены труда США , около 43 000 американцев работают в контакте с пиридином. [110]
В продуктах питания
Исторически пиридин добавляли в пищу для придания ей горького вкуса, хотя сейчас эта практика запрещена в США [111] [112]. Его все еще можно добавлять в этанол, чтобы сделать его непригодным для питья. [7]
Метаболизм
Воздействие пиридина обычно приводит к его вдыханию и всасыванию в легких и желудочно-кишечном тракте, где он либо остается неизменным, либо метаболизируется . Основными продуктами метаболизма пиридина являются гидроксид N- метилпиридиния, который образуется N- метилтрансферазами (например, пиридин- N- метилтрансфераза ), а также N- оксид пиридина и 2-, 3- и 4-гидроксипиридин, которые образуются. под действием монооксигеназы . В организме человека пиридин метаболизируется только в гидроксид N- метилпиридиния. [8] [105]
Экологическая судьба
Пиридин легко разлагается бактериями до аммиака и углекислого газа. [113] Незамещенное пиридиновое кольцо разлагается быстрее, чем пиколин , лутидин , хлорпиридин или аминопиридины , [114], а также было показано, что ряд пиридиновых разлагателей избыточно продуцируют рибофлавин в присутствии пиридина. [115] Ионизируемые N- гетероциклические соединения, в том числе пиридин, взаимодействуют с поверхностями окружающей среды (такими как почвы и отложения) посредством множества pH-зависимых механизмов, включая разделение на органическое вещество почвы , катионный обмен и поверхностное комплексообразование.[116] Такая адсорбция на поверхности снижает биодоступность пиридинов для микробных деструкторов и других организмов, тем самым замедляя темпы разложения и снижая экотоксичность . [117]
Номенклатура
Систематическое название пиридина в номенклатуре Ганча – Видмана, рекомендованное IUPAC , - азинин . Однако систематические названия простых соединений используются очень редко; вместо этого, гетероциклическая номенклатура следует исторически сложившимся общепринятым названиям. ИЮПАК не рекомендует использовать азинин / азин в пользу пиридина . [118] Нумерация кольцевых атомов в пиридине начинается с азота (см. Инфобокс). Распределение позиций по буквам греческого алфавита (α-γ) и номенклатура паттернов замещения, общая для гомоароматических систем ( орто , мета , пара) иногда используются. Здесь α ( орто ), β ( мета ) и γ ( пара ) относятся к позиции 2, 3 и 4 соответственно. Систематическое название производных пиридина - пиридинил , в котором положению замещенного атома предшествует число. Однако историческое название пиридил поощряется IUPAC и используется вместо систематического названия. [119] катионные производный , образованный путем добавления электрофильного к атому азота, называется пиридиния .
Смотрите также
- 6-членный ароматические кольца с одним углеродом заменен на другую группу: борабензольный , silabenzene , germabenzene , stannabenzene , пиридин, phosphorine , arsabenzene , stibabenzene , bismabenzene , пирилиевая , thiopyrylium , selenopyrylium , telluropyrylium
- 6-членные кольца с двумя атомами азота: диазины
- 6-членные кольца с тремя атомами азота: триазины
- 6-членные кольца с четырьмя атомами азота: тетразины
- 6-членные кольца с пятью атомами азота: пентазин
- 6-членные кольца с шестью атомами азота: гексазин
использованная литература
- ^ Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 141. DOI : 10.1039 / 9781849733069-FP001 . ISBN 978-0-85404-182-4.
- ^ a b c d e f g h i j k Shimizu, S .; Watanabe, N .; Катаока, Т .; Shoji, T .; Abe, N .; Morishita, S .; Ичимура, Х. "Пиридин и производные пиридина". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a22_399 .
- ^ a b c d e f Карманный справочник NIOSH по химической опасности. «# 0541» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Лиде , стр. 3–474
- ^ "Пиридин - CAS #: 110-86-1" . ChemSrc . 8 января 2020.
- ^ «455. Сила гетероциклических оснований» .
- ^ a b c d e RÖMPP Online - Версия 3.5 . Thieme Chemistry . Штутгарт: Георг Тиме. 2009 г.
- ^ a b c d e f g Запись о пиридине в базе данных веществ GESTIS Института безопасности и гигиены труда
- ^ a b «Пиридин» . Немедленно опасная для жизни или здоровья концентрация (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ "Пиридин MSDS" . fishersci.com . Фишер.
- ^ a b Кокс, Э. (1958). «Кристаллическая структура бензола». Обзоры современной физики . 30 (1): 159–162. Bibcode : 1958RvMP ... 30..159C . DOI : 10.1103 / RevModPhys.30.159 .
- ^ Лиде , стр. 3-673
- ^ Лиде , стр. 5–28
- ^ Лиде , стр. 6-211
- ^ Лиде , стр. 6-221
- ^ Majer, V .; Свобода, В. (1985). Энтальпии испарения органических соединений: критический обзор и сбор данных . Оксфорд: Научные публикации Блэквелла. ISBN 0-632-01529-2.
- ^ Домальский, Евгений С .; Слух, Элизабет Д. (1996). «Теплоемкость и энтропии органических соединений в конденсированной фазе». Журнал физических и химических справочных данных . 25 (1): 1. Bibcode : 1996JPCRD..25 .... 1D . DOI : 10.1063 / 1.555985 .
- ^ Лиде , стр. 6-67
- ^ Маккалоу, JP; Дуслин, Д.Р .; Мессерли, Дж. Ф.; Хоссенлопп, ИА; Kincheloe, TC; Уоддингтон, Гай (1957). «Пиридин: экспериментальные и расчетные химические термодинамические свойства между 0 и 1500 ° K. Пересмотренное определение вибрации». Журнал Американского химического общества . 79 (16): 4289. DOI : 10.1021 / ja01573a014 .
- ^ Mootz, D. (1981). «Кристаллические структуры пиридина и тригидрата пиридина». Журнал химической физики . 75 (3): 1517–1522. Bibcode : 1981JChPh..75.1517M . DOI : 10.1063 / 1.442204 .
- ^ Джоуль , стр. 14
- ^ Джоуль , стр. 16
- ^ a b c d e f g h Пиридин (PDF) . Монографии МАИР 77 . Вашингтон, округ Колумбия: OSHA. 1985 г.
- ^ a b c d e Джоуль , стр. 125–141
- ^ a b c Дэвис, Д. Т. (1992). Ароматическая гетероциклическая химия . Издательство Оксфордского университета. ISBN 0-19-855660-8.
- ^ Milcent, R .; Чау, Ф. (2002). Chimie organique hétérocyclique: Structures fondamentales . EDP Sciences. С. 241–282. ISBN 2-86883-583-X.
- ^ Крыговский, TM; Szatyowicz, H .; Захара, Дж. Э. (2005). «Как водородная связь изменяет молекулярную структуру и делокализацию π-электронов в кольце производных пиридина / пиридиния, участвующих в комплексообразовании водородной связи». J. Org. Chem . 70 (22): 8859–8865. DOI : 10.1021 / jo051354h . PMID 16238319 .
- ^ Джоуль , стр. 7
- ^ Weissberger, A .; Клингберг, А .; Барнс, РА; Броды, Ф .; Руби, PR (1960). Пиридин и его производные . 1 . Нью-Йорк: Interscience.
- ^ Андерсон, Томас (1849). «О составе и свойствах пиколина - новой органической основы из каменноугольной смолы» . Труды королевских обществ Эдинбургского университета . 16 (2): 123–136. DOI : 10.1017 / S0080456800024984 .
- ^ a b Андерсон, Т. (1849). "Producte der trocknen Destillation thierischer Materien" [Продукты сухой перегонки животных материалов]. Annalen der Chemie und Pharmacie (на немецком языке). 70 : 32–38. DOI : 10.1002 / jlac.18490700105 .
- ^ Андерсон, Томас (1851). «О продуктах разрушающей перегонки веществ животного происхождения. Часть II» . Труды Королевского общества Эдинбурга . 20 (2): 247–260. DOI : 10.1017 / S0080456800033160 . С п. 253: «Пиридин. Первое из этих оснований, которому я дал название пиридин,…»
- ^ Андерсон, Т. (1851). "Ueber die Producte der trocknen Destillation thierischer Materien" [О продуктах сухой перегонки животного вещества]. Annalen der Chemie und Pharmacie (на немецком языке). 80 : 44–65. DOI : 10.1002 / jlac.18510800104 .
- ^ Кернер, W. (1869). «Synthèse d'une base isomère à la toluidine» [Синтез основания, [то есть] изомерного толуидину]. Giornale di Scienze Naturali ed Economiche (журнал естественных наук и экономики (Палермо, Италия)) (на французском языке). 5 : 111–114.
- ↑ Дьюар, Джеймс (27 января 1871 г.). «О продуктах окисления пиколина» . Химические новости . 23 : 38–41.
- ^ Рок, Алан Дж. (1988). «Кернер, Дьюар и структура пиридина» . Вестник истории химии . 2 : 4.
- ^ Ладенбург, Альберт . Лекции по истории развития химии со времен Лавуазье. (PDF) . С. 283–287.
- ^ Bansal, Радж К. (1999). Гетероциклическая химия . п. 216. ISBN. 81-224-1212-2.
- ^ См .:
- Ладенбург, А. (1884). «Синтез пиперидинов» [Синтез пиперидина]. Berichte der Deutschen Chemischen Gesellschaft (на немецком языке). 17 : 156. DOI : 10.1002 / cber.18840170143 .
- Ладенбург, А. (1884). "Synthese des Piperidins und seiner Homologen" [Синтез пиперидина и его гомологов]. Berichte der Deutschen Chemischen Gesellschaft (на немецком языке). 17 : 388–391. DOI : 10.1002 / cber.188401701110 .
- ^ Рамзи, Уильям (1876). «О пиколине и его производных» . Философский журнал . 5-я серия. 2 (11): 269–281. DOI : 10.1080 / 14786447608639105 .
- ^ "A. Henninger, aus Paris. 12. апреля 1877 г.". Berichte der Deutschen Chemischen Gesellschaft (Переписка). 10 : 727–737. 1877. DOI : 10.1002 / cber.187701001202 .
- ^ Hantzsch, A. (1881). «Продукты конденсации альдегидаммония и кетонартиген Verbindungen» [Продукты конденсации альдегид-аммиака и соединений кетонового типа]. Berichte der Deutschen Chemischen Gesellschaft . 14 (2): 1637–1638. DOI : 10.1002 / cber.18810140214 .
- ^ Knoevenagel, E .; Фрис, А. (1898). "Synthesen in der Pyridinreihe. Ueber eine Erweiterung der Hantzsch'schen Dihydropyridinsynthese" [Синтезы в ряду пиридина. О расширении синтеза дигидропиридина Ганча. Berichte der Deutschen Chemischen Gesellschaft . 31 : 761–767. DOI : 10.1002 / cber.189803101157 .
- ^ a b Чичибабин, AE (1924). "Uber Kondensation der Aldehyde mit Ammoniak zu Pyridinebasen" [О конденсации альдегидов с аммиаком с образованием пиридинов]. Journal für Praktische Chemie . 107 : 122. DOI : 10.1002 / prac.19241070110 .
- ^ Лопух, Джорджия, изд. (1995). Справочник ароматических ингредиентов Фенароли . 2 (3-е изд.). Бока-Ратон: CRC Press. ISBN 0-8493-2710-5.
- ^ Täufel, A .; Ternes, W .; Tunger, L .; Зобель, М. (2005). Lebensmittel-Lexikon (4-е изд.). Behr. п. 450. ISBN 3-89947-165-2.
- ^ Тан, Цзянь; Цзинь, Ци Чжан; Шен, Го Хуэй; Хо, Чи Тан; Чанг, Стивен С. (1983). «Выделение и идентификация летучих соединений из жареной курицы». Журнал сельскохозяйственной и пищевой химии . 31 (6): 1287. DOI : 10.1021 / jf00120a035 .
- ^ Shibamoto, Такаюки; Камия, Йоко; Михара, Сатору (1981). «Выделение и идентификация летучих соединений в приготовленном мясе: сукияки». Журнал сельскохозяйственной и пищевой химии . 29 : 57–63. DOI : 10.1021 / jf00103a015 .
- ^ Aeschbacher, HU; Wolleb, U; Лелигер, Дж; Spadone, JC; Лиардон, Р. (1989). «Вклад компонентов кофейного аромата в мутагенность кофе». Пищевая и химическая токсикология . 27 (4): 227–232. DOI : 10.1016 / 0278-6915 (89) 90160-9 . PMID 2659457 .
- ^ Баттери, Рон Дж .; Зейферт, Ричард М .; Guadagni, Dante G .; Линг, Луиза С. (1971). «Характеристика летучих пиразиновых и пиридиновых компонентов картофельных чипсов». Журнал сельскохозяйственной и пищевой химии . Вашингтон, округ Колумбия: ACS. 19 (5): 969–971. DOI : 10.1021 / jf60177a020 .
- ^ Хо, Чи Тан; Ли, Кен Н .; Цзинь, Ци Чжан (1983). «Выделение и идентификация летучих ароматических соединений в жареном беконе». Журнал сельскохозяйственной и пищевой химии . 31 (2): 336. DOI : 10.1021 / jf00116a038 .
- ^ Дюмон, Жан-Пьер; Адда, Жак (1978). «Наличие сесквитерпена в летучих веществах горного сыра». Журнал сельскохозяйственной и пищевой химии . 26 (2): 364. DOI : 10.1021 / jf60216a037 .
- ^ Labows, Джон Н., младший; Уоррен, Крейг Б. (1981). «Одоранты как химические вестники». В Moskowitz, Говард Р. (ред.). Качество запаха и химическая структура . Вашингтон, округ Колумбия: Американское химическое общество. С. 195–210. DOI : 10.1021 / Б.К.-1981-0148.fw001 . ISBN 9780841206076.
- ^ Vitzthum, Отто G .; Веркхофф, Питер; Хуберт, Питер (1975). «Новые летучие составляющие аромата черного чая». Журнал сельскохозяйственной и пищевой химии . 23 (5): 999. DOI : 10.1021 / jf60201a032 .
- ^ Kostelc, JG; Preti, G .; Нельсон, PR; Браунер, Л .; Баэни, П. (1984). «Оральные запахи при раннем экспериментальном гингивите». Журнал исследований пародонтологии . 19 (3): 303–312. DOI : 10.1111 / j.1600-0765.1984.tb00821.x . PMID 6235346 .
- ^ Täufel, A .; Ternes, W .; Tunger, L .; Зобель, М. (2005). Lebensmittel-Lexikon (4-е изд.). Behr. п. 226. ISBN. 3-89947-165-2.
- ^ Gossauer, A. (2006). Struktur und Reaktivität der Biomoleküle . Вайнхайм: Wiley-VCH. п. 488. ISBN 3-906390-29-2.
- ^ «Развитие пиридина в Китае» . АгроХимЭкс . 11 мая 2010 года в архив с оригинала на 20 сентября 2018 года . Проверено 7 января 2011 года .
- ^ "О Вертеллусе" . vertellus.com . Архивировано из оригинального 18 -го сентября 2012 года . Проверено 7 января 2011 года .
- ^ а б Франк, RL; Семь, RP (1949). «Пиридины. IV. Исследование синтеза чичибабина». Журнал Американского химического общества . 71 (8): 2629–2635. DOI : 10.1021 / ja01176a008 .
- ^ Патент DE 1917037 , ICI, выданные 1968
- ^ JP патент 7039545 , Nippon Kayaku, выданные 1967
- ^ BE патент 758201 , Koei Chemicals, выпущенный в 1969 году
- ^ Менш, Ф. (1969). Erdöl Kohle Erdgas Petrochemie. 2: 67–71
- Перейти ↑ Behr, A. (2008). Однородный Angewandte Katalyse . Вайнхайм: Wiley-VCH. п. 722. ISBN 978-3-527-31666-3.
- ^ Kroehnke, Fritz (1976). «Специфический синтез пиридинов и олигопиридинов». Синтез . 1976 (1): 1–24. DOI : 10,1055 / с-1976-23941 ..
- ^ Скелл, PS; Сандлер, RS (1958). «Реакции 1,1-дигалоциклопропанов с электрофильными реагентами. Синтетический путь введения атома углерода между атомами двойной связи». Журнал Американского химического общества . 80 (8): 2024 DOI : 10.1021 / ja01541a070 .
- ^ Джонс, RL; Рис, CW (1969). «Механизм расширения гетероциклического кольца. Часть III. Взаимодействие пирролов с дихлоркарбеном». Журнал химического общества C: Organic (18): 2249. DOI : 10.1039 / J39690002249 .
- ^ Gambacorta, A .; Nicoletti, R .; Cerrini, S .; Fedeli, W .; Гавуццо, Э. (1978). «Улавливание и определение структуры промежуточного продукта в реакции между 2-метил-5- трет- бутилпирролом и дихлоркарбеном». Буквы тетраэдра . 19 (27): 2439. DOI : 10.1016 / S0040-4039 (01) 94795-1 .
- ^ Gattermann, L .; Скита, А. (1916). "Eine Synthese von Pyridin-Derivaten" [Синтез производных пиридина]. Chemische Berichte . 49 (1): 494–501. DOI : 10.1002 / cber.19160490155 .
- ^ "Гаттерманн – Скита" . Институт химии, Скопье. Архивировано из оригинального 16 -го июня 2006 года.
- ^ Скотт (1967). «Метод разложения радиоактивной никотиновой кислоты» . Биохимический журнал . 102 (1): 87–93. DOI : 10.1042 / bj1020087 . PMC 1270213 . PMID 6030305 .
- ^ Тарр, JB; Ардитти, Дж. (1982). «Биосинтез ниацина в проростках Zea mays » . Физиология растений . 69 (3): 553–556. DOI : 10.1104 / pp.69.3.553 . PMC 426252 . PMID 16662247 .
- Перейти ↑ Campaigne, E. (1986). «Адриен Альберт и рационализация гетероциклической химии». J. Chem. Educ . 63 (10): 860. Bibcode : 1986JChEd..63..860C . DOI : 10.1021 / ed063p860 .
- ^ Бакке, Ян М .; Хегбом, Ингрид (1994). «Пятиокись азота-диоксид серы, новая система нитрат-иона» . Acta Chemica Scandinavica . 48 : 181–182. DOI : 10.3891 / acta.chem.scand.48-0181 .
- ↑ Оно, Нобору; Мурашима, Такаши; Ниси, Кейджи; Накамото, Кен-Ичи; Като, Ацуши; Тамай, Рюдзи; Уно, Хидэмицу (2002). «Получение новых гетероизоиндолов из нитропиридинов и нитропиридонов». Гетероциклы . 58 : 301. DOI : 10,3987 / COM-02-S (M) 22 .
- ^ Даффи, Джозеф L .; Лаали, Кеннет К. (1991). «Апротическое нитрование ( НЕТ+
2BF-
4) 2-галоген- и 2,6-дигалогенпиридинов и химия переноса-нитрования их катионов N- нитропиридиния ». Журнал органической химии . 56 (9): 3006. doi : 10.1021 / jo00009a015 . - ^ Джоуль , стр. 126
- ^ Мёллер, Эрнст Фридрих; Биркофер, Леонхард (1942). «Konstitutionsspezifität дер Nicotinsäure ALS Wuchsstoff Bei Proteus обыкновенная унд Streptobacterium Plantarum » [Конституционное специфичность никотиновой кислоты в качестве фактора роста в Proteus обыкновенная и Streptobacterium Plantarum ]. Berichte der Deutschen Chemischen Gesellschaft (серии A и B) . 75 (9): 1108. DOI : 10.1002 / cber.19420750912 .
- ^ Мошер, HS; Тернер, Л .; Карлсмит, А. (1953). «Пиридин- N- оксид». Орг. Synth . 33 : 79. DOI : 10,15227 / orgsyn.033.0079 .
- ^ Луи-Шарль Кампо и Кейт Фагну (2011). «Синтез 2-арилпиридинов путем катализируемого палладием прямого арилирования пиридиновых N-оксидов» . Орг. Synth . 88 : 22. DOI : 10,15227 / orgsyn.088.0022 .CS1 maint: использует параметр авторов ( ссылка )
- ^ Джоуль , стр. 133
- ^ Шрив, Р. Норрис; Riechers, EH; Рубенкоениг, Гарри; Гудман, AH (1940). «Аминирование в гетероциклическом ряду амидом натрия». Промышленная и инженерная химия . 32 (2): 173. DOI : 10.1021 / ie50362a008 .
- ^ Барсук, G; Зассе, W (1963). «Действие металлических катализаторов на пиридины». Успехи химии гетероциклов . Успехи химии гетероциклов. 2 . С. 179–202. DOI : 10.1016 / S0065-2725 (08) 60749-7 . ISBN 9780120206025. PMID 14279523 .
- ^ Асс, ФВН (1966). «2,2'-бипиридин» (PDF) . Органический синтез . 46 : 5–8. DOI : 10.1002 / 0471264180.os046.02 . ISBN 0471264229. Архивировано из оригинального (PDF) 21 января 2012 года.
- ^ Eller, K .; Henkes, E .; Россбахер, Р .; Хок, Х. "Амины, алифатические". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH.
- ^ a b Кокс, JD; Пилчер, Г. (1970). Термохимия органических и металлоорганических соединений . Нью-Йорк: Academic Press. С. 1–636. ISBN 0-12-194350-X.
- ^ Таннер, Деннис Д .; Ян, Чи Мин (1993). «О структуре и механизме образования реагента Лэнсбери, тетракис ( N- дигидропиридил) алюмината лития ». Журнал органической химии . 58 (7): 1840. DOI : 10.1021 / jo00059a041 .
- ^ Де Конинг, А .; Будзелаар, PHM; Boersma, J .; Ван Дер Керк, GJM (1980). «Специфическое и селективное восстановление ароматических гетероциклов азота бис-пиридиновыми комплексами бис (1,4-дигидро-1-пиридил) цинка и бис (1,4-дигидро-1-пиридил) магния». Журнал металлоорганической химии . 199 (2): 153. DOI : 10.1016 / S0022-328X (00) 83849-8 .
- ^ Ферлес, М. (1959). Сборник чехословацких химических сообщений. 24: 1029–1033.
- Перейти ↑ Laurence, C. and Gal, JF. Шкалы основности и сродства Льюиса, данные и измерения, (Wiley 2010), стр. 50-51, IBSN 978-0-470-74957-9
- ^ Крамер, RE; Бопп, Т. Т. (1977). «Графическое отображение энтальпий образования аддуктов для кислот и оснований Льюиса». Журнал химического образования . 54 : 612–613. DOI : 10.1021 / ed054p612 .На графиках, представленных в этом документе, использовались более старые параметры. Улучшенные параметры E&C перечислены в модели ECW .
- ^ Накамото, К. (1997). Инфракрасные и рамановские спектры неорганических и координационных соединений . Часть А (5-е изд.). Вайли. ISBN 0-471-16394-5.
- ^ Накамото, К. (31 июля 1997 года). Инфракрасные и рамановские спектры неорганических и координационных соединений . Часть B (5-е изд.). п. 24. ISBN 0-471-16392-9.
- ^ Крэбтри, Роберт (1979). «Соединения иридия в катализе». Счета химических исследований . 12 (9): 331–337. DOI : 10.1021 / ar50141a005 .
- ^ Elschenbroich, C. (2008). Металлоорганическая химия (6-е изд.). Vieweg & Teubner. С. 524–525. ISBN 978-3-8351-0167-8.
- ^ «Экологические и санитарные критерии параквата и диквата» . Женева: Всемирная организация здравоохранения. 1984 г.
- Перейти ↑ Sherman, AR (2004). «Пиридин». В пакете, Л. (ред.). Энциклопедия реагентов для органического синтеза . e-EROS (Энциклопедия реагентов для органического синтеза) . Нью-Йорк: J. Wiley & Sons. DOI : 10.1002 / 047084289X.rp280 . ISBN 0471936235.
- ^ "Wasserbestimmung mit Karl-Fischer-Titration" [Анализ воды с титрованием по Карлу Фишеру] (PDF) . Йенский университет. Архивировано из оригинального (PDF) 19 июля 2011 года.
- ^ Tojo, G .; Фернандес, М. (2006). Окисление спиртов до альдегидов и кетонов: руководство по современной общепринятой практике . Нью-Йорк: Спрингер. стр. 28, 29, 86. ISBN 0-387-23607-4.
- ^ "Пиридин MSDS" (PDF) . Альфа Эзар . Проверено 3 июня 2010 года .
- ^ "База данных (EPA)" . США Агентство по охране окружающей среды .
- ^ Aylward, G (2008). SI Химические данные (6-е изд.). ISBN 978-0-470-81638-7.
- ^ Международное агентство по изучению рака (IARC) (22 августа 2000 г.). «Резюме и оценка пиридина» . Обобщения и оценки МАИР . IPCS INCHEM . Проверено 17 января 2007 года .
- ^ a b Bonnard, N .; Brondeau, MT; Miraval, S .; Pillière, F .; Protois, JC; Шнайдер, О. (2011). «Пиридин» (PDF) . Fiche Toxicologique (на французском языке). INRS.
- ^ Рабочая группа МАИР по оценке канцерогенных рисков для людей (2019). Некоторые химические вещества, вызывающие опухоли мочевыводящих путей у грызунов (PDF) . Международное агентство по изучению рака . Лион, Франция. С. 173–198. ISBN 978-92-832-0186-1. OCLC 1086392170 .
- ^ Хлам, Джорджия; Форд, CS (1980). «Обзор органических выбросов от выбранных процессов сжигания». Chemosphere . 9 (4): 187. Bibcode : 1980Chmsp ... 9..187J . DOI : 10.1016 / 0045-6535 (80) 90079-X .
- ^ Хоторн, Стивен Б .; Сиверс, Роберт Э. (1984). «Выбросы органических загрязнителей воздуха из сточных вод сланцевого масла». Наука об окружающей среде и технологии . 18 (6): 483–90. Bibcode : 1984EnST ... 18..483H . DOI : 10.1021 / es00124a016 . PMID 22247953 .
- ^ Stuermer, Дэниел Х .; Ng, Douglas J .; Моррис, Кларенс Дж. (1982). «Органические загрязнители в подземных водах рядом с участком подземной газификации угля на северо-востоке Вайоминга». Наука об окружающей среде и технологии . 16 (9): 582–7. Bibcode : 1982EnST ... 16..582S . DOI : 10.1021 / es00103a009 . PMID 22284199 .
- ^ Национальное обследование профессионального воздействия 1981–83 . Цинциннати, Огайо: Департамент здравоохранения и социальных служб, Служба общественного здравоохранения, Центры по контролю заболеваний, Национальный институт профессиональной безопасности и здоровья.
- ^ 83 FR 50490
- ^ «FDA удаляет 7 синтетических ароматизирующих веществ из списка пищевых добавок» . 5 октября 2018 . Проверено 8 октября 2018 года .
- ^ Sims, GK; О'Лафлин, EJ (1989). «Разложение пиридинов в окружающей среде». CRC Critical Reviews в области экологического контроля . 19 (4): 309–340. DOI : 10.1080 / 10643388909388372 .
- ^ Sims, GK; Соммерс, Л. Е. (1986). «Биодеградация производных пиридина в почвенных суспензиях». Экологическая токсикология и химия . 5 (6): 503–509. DOI : 10.1002 / etc.5620050601 .
- ^ Sims, GK; О'Лафлин, EJ (1992). «Продукция рибофлавина при росте Micrococcus luteus на пиридине» . Прикладная и экологическая микробиология . 58 (10): 3423–3425. DOI : 10,1128 / AEM.58.10.3423-3425.1992 . PMC 183117 . PMID 16348793 .
- ^ Bi, E .; Schmidt, TC; Хадерлейн, С.Б. (2006). «Сорбция гетероциклических органических соединений на эталонных почвах: колоночные исследования для идентификации процесса». Environ Sci Technol . 40 (19): 5962–5970. Bibcode : 2006EnST ... 40.5962B . DOI : 10.1021 / es060470e . PMID 17051786 .
- ^ О'Лафлин, Э. Дж; Traina, SJ; Симс, ГК (2000). «Влияние сорбции на биодеградацию 2-метилпиридина в водных суспензиях эталонных глинистых минералов». Экологическая токсикология и химия . 19 (9): 2168–2174. DOI : 10.1002 / etc.5620190904 .
- ^ Пауэлл, WH (1983). «Пересмотр расширенной системы номенклатуры Ганча-Видмана для гетеро-моноциклов» (PDF) . Чистая и прикладная химия . 55 (2): 409–416. DOI : 10,1351 / pac198855020409 . S2CID 4686578 .
- ^ Hellwinkel, D. (1998). Die systematische Nomenklatur der Organischen Chemie (4-е изд.). Берлин: Springer. п. 45. ISBN 3-540-63221-2.
Библиография
- Джоуль, JA; Миллс, К. (2010). Гетероциклическая химия (5-е изд.). Чичестер: издательство Blackwell Publishing. ISBN 978-1-4051-3300-5.
- Лиде, Д.Р., изд. (2009). Справочник по химии и физике (90-е изд.). Бока-Ратон: CRC Press. ISBN 978-1-4200-9084-0.
внешние ссылки
| Викискладе есть медиафайлы по теме пиридина . |
- Синтез и свойства пиридинов на chemsynthesis.com
- Международная карта химической безопасности 0323
- Карманный справочник NIOSH по химической опасности
- Синтез пиридинов (обзор новейших методов)
- Пиридины
- Аминовые растворители
- Дурно пахнущие химикаты
- Ароматические основы
- Простые ароматические кольца
- Функциональные группы
- Ароматические растворители