 | |
 | |
| Клинические данные | |
|---|---|
| Пути администрирования | Буккальная ( sublabial ), сублингвальна , интраназально , ингаляция , внутривенная , внутримышечная , ректальная |
| Код УВД |
|
| Легальное положение | |
| Легальное положение | |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| ЧЭМБЛ | |
| CompTox Dashboard ( EPA ) | |
| Химические и физические данные | |
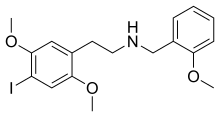
| Формула | C 18 H 22 I N O 3 |
| Молярная масса | 427,282 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
| | |
| Часть серии по |
| Психоделия |
|---|
25I-NBOMe ( 2C-I-NBOMe , Cimbi-5 , также сокращенно « 25I ») представляет собой синтетический галлюциноген, который используется в биохимических исследованиях для картирования использования мозгом рецептора серотонина типа 2A ; его также иногда используют в развлекательных целях. Производное замещенного семейства фенэтиламина 2C-I , это наиболее известный член семейства 25-NB . Он был открыт в 2003 году химиком Ральфом Хаймом из Свободного университета Берлина , который опубликовал свои открытия в своей докторской диссертации. [2] Соединение было впоследствии исследовано командой в Университет Пердью под руководством Дэвида Николса . [3]
Углерода-11 помечены версии 25I-NBOME, [11C] Cimbi-5, был синтезирован и подтверждено в качестве РФП для позитронно - эмиссионной томографии (ПЭТ) в Копенгаген. [4] [5] Являясь первым полноправным агонистом рецептора 5-HT 2A, радиолиганд ПЭТ, [11C] -CIMBI-5 является перспективным в качестве более функционального маркера этих рецепторов, особенно в их состояниях высокого сродства. [4]
Уличные прозвища и прозвища в СМИ для этого препарата: «N-Bomb», «Solaris», «Smiles» и «Wizard». [6] [7] [8]
Рекреационное использование [ править ]
Хотя 25I-NBOMe был обнаружен в 2003 году, он не стал популярным рекреационным наркотиком до 2010 года, когда впервые был продан поставщиками, специализирующимися на поставках дизайнерских наркотиков . [9] В сленговом контексте название соединения часто сокращается до «25I» или просто называется «N-Bomb». [10] Согласно опросу 2014 года, 25I-NBOMe был наиболее часто используемым из серии NBOMe. [11] К 2013 году сообщения о случаях интоксикации 25I-NBOMe с аналитическим подтверждением наличия препарата в организме и без него становились все более распространенными в медицинской литературе. [12]
Ходят слухи, что 25I-NBOMe неактивен при пероральном приеме; однако очевидные передозировки произошли при пероральном приеме. Общие пути введения включают сублингвальный , буккальный и интраназальный. [11] Для сублингвального и буккального введения 25I-NBOMe часто наносят на листы промокательной бумаги, небольшие части ( вкладки ) которой удерживаются во рту, чтобы обеспечить всасывание через слизистую оболочку полости рта. [13] [14] Имеются сообщения о внутривенном введении раствора 25I-NBOMe и курении препарата в порошкообразной форме. [15] [16]
Из-за своей эффективности и гораздо более низкой стоимости, чем так называемые классические или традиционные психоделики, блоттеры 25I-NBOMe иногда ошибочно принимают за ЛСД- блоттеры или ошибочно принимают за них. [17] Даже небольшие количества 25I-NBOMe могут производить большое количество промокательных машин. Продавцы будут импортировать 25I-NBOMe оптом (например, 1-килограммовые контейнеры) и перепродавать отдельные дозы с получением значительной прибыли. [14]
Дозировка [ править ]
25I-NBOMe является сильнодействующим веществом, действующим в дозах менее миллиграмма. Обычная доза гидрохлоридной соли составляет 600–1200 мкг . Консультативный совет Великобритании по злоупотреблению наркотиками заявляет, что обычная доза составляет от 50 до 100 мкг [14], хотя другие источники указывают, что эти цифры неверны; Эровид предварительно предполагает, что пороговая доза для людей составляет 50–250 мкг, при легкой дозе 200–600 мкг, обычной дозе 500–800 мкг и высокой дозе 700–1500 мкг. [18] На этом уровне активности невозможно точно измерить разовую дозу порошка 25I-NBOMe без аналитических весов , и попытка сделать это может подвергнуть пользователя значительному риску передозировки. [14]
Эффекты [ править ]
Эффект 25I-NBOMe обычно длится 6–10 часов при приеме сублингвально или буккально (между десной и щекой). [16] При вдыхании (вдыхании) эффекты обычно длятся 4–6 часов. [16]
25I-NBOMe имеет аналогичные эффекты с ЛСД, хотя пользователи сообщают о более негативных эффектах, когда они находятся под воздействием, и о большем риске причинения вреда после использования по сравнению с классическими психоделиками. [11]
Сообщения о случаях семи британских мужчин, которые обратились в отделение неотложной помощи после аналитически подтвержденной интоксикации 25I-NBOMe, предполагают следующие потенциальные побочные эффекты: тахикардия (n = 7), гипертония (4), возбуждение (6), агрессия, зрительные и слуховые галлюцинации (6), судороги (3), гиперпирексия (3), клонус (2), повышенное количество лейкоцитов (2), повышенная креатинкиназа (7), метаболический ацидоз (3) и острое повреждение почек (1) ». [15]
25I-NBOMe можно употреблять в жидкой, порошковой или бумажной форме, его можно нюхать, вводить путем инъекций, смешивать с пищей или курить, но наиболее распространено сублингвальное введение. [19]
Токсичность [ править ]
Рекреационное использование 25I-NBOMe несет в себе значительный риск как фармакологической, так и поведенческой токсичности. [12] [15] 25I-NBOMe - относительно новое вещество, и о его фармакологических рисках или взаимодействии с другими веществами известно мало. LD 50 еще не было определено. [20] Это очень мощный агонист серотонина и, из-за его психоделических эффектов и неоднозначного юридического статуса, дизайнерский наркотик, о котором сообщалось о приеме в рекреационных целях, начиная с 2010 года. Сообщения о смертельных случаях и серьезных травмах связаны с использованием 25I-NBOMe. , побуждая некоторые правительства контролировать владение, производство и продажу. Сайт Erowidзаявляет, что 25I-NBOMe является чрезвычайно сильнодействующим веществом, и его нельзя нюхать, и что препарат «по всей видимости, привел к нескольким смертельным случаям за последний год». [17] Сообщалось также о нескольких несмертельных передозировках, требующих длительной госпитализации. [14] [12] [15]
По состоянию на август 2015 года, 25I-NBOMe, как сообщается, привел как минимум к 19 смертельным случаям от передозировки в Соединенных Штатах. [10] [21] В июне 2012 года двое подростков в Гранд-Форксе, Северная Дакота и Ист-Гранд-Форкс, Миннесота, совершили смертельную передозировку вещества, предположительно 25I-NBOMe, что привело к длительным приговорам для двух вовлеченных сторон и федеральному обвинительному заключению. против онлайн-продавца из Техаса. [22] 21-летний мужчина из Литл-Рока, штат Арканзас.умер в октябре 2012 года после приема жидкой капли препарата в нос на музыкальном фестивале. Сообщается, что он заранее употреблял алкогольные напитки с кофеином в течение «нескольких часов». Неясно, какие еще лекарства он мог принимать, поскольку вскрытие обычно не проверяет наличие исследовательских химикатов. [23] В январе 2013 года 18-летний парень из Скоттсдейла, штат Аризона, умер после употребления 25I-NBOMe, продаваемого как LSD; токсикологический скрининг не выявил других лекарств в организме человека. Препарат является предполагаемой причиной смерти в другом инциденте в Скоттсдейле, штат Аризона, в апреле 2013 года. [14] Он также упоминается в смерти 21-летней женщины в августе 2013 года [24] и смерти 17 -летней женщины. лет в Миннесоте в январе 2014, [25]а также смерть 15-летнего подростка в Вашингтоне в сентябре 2014 г. [26]
25I-NBOMe был причастен к множеству смертей в Австралии. В марте 2012 года мужчина в Австралии скончался от травм, полученных в результате столкновения с деревьями и столбами электропередач в состоянии алкогольного опьянения 25I-NBOMe. [27]
25I-NBOMe был связан с серьезным заболеванием 20 января 2016 года в Корке , Ирландия , в результате которого были госпитализированы шесть подростков, один из которых позже скончался. Согласно сообщениям, по крайней мере у одного из подростков произошла остановка сердца , а также сильное внутреннее кровотечение. [28]
25I-NBOMe предположительно проявляет функциональную селективность в отношении рецептора 5HT 2A, аналогичную другим фенэтиламиновым галлюциногенам, активируя сигнальный каскад фосфолипазы A2 [29], который отвечает за высвобождение тромбоксана A2 , запускающего агрегацию тромбоцитов. Чрезмерные концентрации TXA2 могут привести к тромбозу , который в сочетании с сосудосуживающим действием 25I-NBOMe является основным фактором риска сердечной ишемии , опасного состояния, симптомы которого присутствуют в нескольких токсикологических отчетах. [20]
Фармакология [ править ]
| Рецептор | K i (нМ) | ± |
|---|---|---|
| 5-HT 2A | 0,044 | |
| 5-HT 2B | 231 | 73 |
| 5-HT 2C | 2 | |
| 5-HT 6 | 73 | 12 |
| μ-опиоид | 82 | 14 |
| κ-опиоид | 288 | 50 |
| H 1 | 189 | 35 год |
25I-NBOME действует как очень мощный полный агонист для человеческого 5-HT 2A - рецептора , [30] [32] с константой диссоциации ( K я ) от 0,044 нМ, что делает его некоторые шестнадцать раз потенции 2C-I сам по себе в этот рецептор. Радиоактивный изотоп форма 25I-NBOME может быть использована для картирования распределения 5-HT 2A рецепторов в головном мозге. [31]
25I-NBOMe вызывает у мышей реакцию подергивания головы, которая полностью блокируется селективным антагонистом 5-HT 2A , что позволяет предположить, что его психоделические эффекты опосредуются 5-HT 2A . Это исследование показало, что 25I-NBOMe примерно в 14 раз сильнее, чем 2C-I in vivo . [33]
В то время как исследования in vitro показали, что эффективность N- бензильных производных 2C-I была значительно выше, чем у 2C-I, N- бензильные производные родственного соединения DOI были неактивными. [34]
25I-NBOMe также слабее взаимодействует с множеством других рецепторов. Значения K i для взаимодействия со следующими мишенями были более 500 нМ: 5-HT 1A , D 3 , H 2 , 5-HT 1D , α 1A адренергический , δ опиоид , переносчик захвата серотонина , 5-HT 5A , 5-HT 1B , D 2 , 5-HT 7 , D 1 , 5-HT 3 , 5-HT 1E, D 5 , мускариновый M 1 -M 5 , H 3 и переносчик захвата дофамина . [31]
Химия [ править ]
Как и другие молекулы 2C- X -NBOMe, 25I-NBOMe является производным семейства 2C фенэтиламинов, описанных химиком Александром Шульгиным в его книге PiHKAL . [14] [12] В частности, 25I-NBOMe представляет собой N- бензильное производное молекулы фенэтиламина 2C-I , образованное добавлением 2-метоксибензила (BnOMe) к азоту (N) основной цепи фенэтиламина. Эта замена значительно увеличивает эффективность молекулы. [14]
Аналоги [ править ]
Аналоги и производные из 2C-I :
25I-NB *:
- 25I-NBF
- 25И-НБМД
- 25I-NB34MD
- 25I-NBOH
- 25I-NBOMe (NBOMe-2CI)
- 25I-NB3OMe
- 25I-NB4OMe
Синтез [ править ]
25I-NBOMe обычно синтезируется из 2C-I и 2-метоксибензальдегида путем восстановительного алкилирования . Это можно сделать поэтапно, сначала получая имин, а затем восстанавливая образовавшийся имин боргидридом натрия , или путем прямой реакции с триацетоксиборгидридом натрия . [2]
Общество и культура [ править ]
Правовой статус [ править ]
Австралия [ править ]
25I-NBOMe был прямо включен в закон о наркотиках Квинсленда в апреле 2012 года и в Новом Южном Уэльсе в октябре 2013 года, как и некоторые родственные соединения, такие как 25B-NBOMe. Федеральное правительство Австралии не имеет специального законодательства относительно любого из N-бензилфенэтиламинов. [35]
Канада [ править ]
По состоянию на 31 октября 2016 г .; 25I-NBOMe - это контролируемое вещество (Список III) в Канаде. [36]
Китай [ править ]
По состоянию на октябрь 2015 года 25I-NBOMe является контролируемым веществом в Китае. [37]
Европейский Союз [ править ]
В сентябре 2014 года Европейский Союз ввел запрет на использование 25I-NBOMe во всех странах-членах. [38]
Израиль [ править ]
Израиль запретил 25I-NBOMe в 2013 году. [39]
Россия [ править ]
Россия была первой страной, которая приняла специальные правила в отношении серии NBOMe. Все препараты из серии NBOMe, включая 25I-NBOMe, стали незаконными в России в октябре 2011 года. [39]
Соединенное Королевство [ править ]
Это вещество относится к классу А в Соединенном Королевстве в результате всеобъемлющего положения о N- бензилфенэтиламине в Законе о злоупотреблении наркотиками 1971 года . [40]
Соединенные Штаты [ править ]
15 ноября 2013 года DEA добавило 25I-NBOMe (а также 25C- и 25B-NBOMe) в Список I, используя свои полномочия по экстренному планированию, сделав эти соединения NBOMe «временно» в Списке I на 2 года. [21] В ноябре 2015 года временное расписание было продлено еще на год [41], в то время как было согласовано постоянное расписание. [42] 25I-NBOMe, 25B-NBOMe и 25C-NBOMe в настоящее время являются веществами Списка 1 в соответствии с 21 CFR 1308.11 (d) [43]
Румыния [ править ]
В 2011 году Румыния запретила все психоактивные вещества. [44]
Сербия [ править ]
25I-NBOMe был внесен в список запрещенных веществ в марте 2015 года. [45]
Швеция [ править ]
Риксдаг добавил 25I-NBOMe в Закон о наказаниях за наркотические средства в соответствии с шведским приложением I ( «вещества, растительные материалы и грибы, которые обычно не используются в медицинских целях» ) с 1 августа 2013 года, опубликованное Агентством медицинских продуктов (MPA) в постановлении LVFS. 2013: 15 указаны как 25I-NBOMe и 2- (4-йодо-2,5-диметоксифенил) -N- (2-метоксибензил) этанамин . [46]
Тайвань [ править ]
Согласно европейскому правилу 2014 года, 25I-NBOMe был отнесен к 4 классу запрещенных веществ. [47]
Бразилия [ править ]
Все препараты из семейства NBOMe, включая 25I-NBOMe, являются незаконными.
Ссылки [ править ]
- ^ Министерство внутренних дел Великобритании (2014). «Закон о злоупотреблении наркотиками 1971 года (кетамин и др.) (Поправка) 2014 года» . Правительство Великобритании.
- ↑ a b Heim R (25 марта 2003 г.). «Synthese und Pharmakologie Potenter 5-HT 2A -Rezeptoragonisten mit N-2-Methoxybenzyl-Partialstruktur. Entwicklung eines neuen Struktur-Wirkungskonzepts» (на немецком языке). dis.fu-berlin.de . Проверено 10 мая 2013 .
- Перейти ↑ Braden MR (2007). «К биофизическому пониманию действия галлюциногена» . Диссертация . Университет Пердью.
- ^ а б Эттруп А., Палнер М., Жиллингс Н., Сантини М.А., Хансен М., Корнум Б.Р. и др. (Ноябрь 2010 г.). «Радиосинтез и оценка 11C-CIMBI-5 как радиолиганда агониста рецептора 5-HT2A для ПЭТ» . Журнал ядерной медицины . 51 (11): 1763–70. DOI : 10,2967 / jnumed.109.074021 . PMID 20956470 .
- ↑ Hansen M (16 декабря 2010 г.). «Дизайн и синтез селективных агонистов рецепторов серотонина для позитронно-эмиссионной томографии головного мозга». Кандидат наук. Диссертация . Det Farmaceutiske Fakultet, København. CiteSeerX 10.1.1.690.4529 .
- ^ "Erowid 25I-NBOMe Vault" .
- ^ Vanderbilt University Medical Center (9 апреля 2015). «Ядовитый центр предостерегает от дизайнерского препарата« N-bomb » » . ScienceDaily.
- ^ Mackin, Тереза (9 октября 2012). Опасный синтетический наркотик продвигается по стране. Архивировано 31 октября 2012 года на Wayback Machine WISH-TV.
- ^ Морганы J (2017-02-08). «Все, что мы знаем о NBOMe и почему он убивает людей» . Vice . Проверено 23 июля 2019 .
- ^ a b Hastings D (6 мая 2013 г.). «Новый наркотик N-бомба попадает на улицу, наводя ужас на родителей, беспокоя полицейских» . Нью-Йорк Дейли Ньюс . Дата обращения 7 мая 2013 .
- ^ a b c Lawn W, Barratt M, Williams M, Horne A, Winstock A (август 2014 г.). «Серия галлюциногенных наркотиков NBOMe: модели использования, характеристики потребителей и самооценка эффектов в большой международной выборке». Журнал психофармакологии . 28 (8): 780–8. DOI : 10.1177 / 0269881114523866 . PMID 24569095 . S2CID 35219099 .
- ^ a b c d Rose SR, Poklis JL, Poklis A (март 2013 г.). «Случай интоксикации 25I-NBOMe (25-I): новый мощный дизайнерский препарат, агонист 5-HT2A» . Клиническая токсикология . 51 (3): 174–7. DOI : 10.3109 / 15563650.2013.772191 . PMC 4002208 . PMID 23473462 .
- ^ Poklis JL, Раз С.А., Элфорд К.Н., Poklis A, Мир MR (октябрь 2015). «Анализ производных 25I-NBOMe, 25B-NBOMe, 25C-NBOMe и других диметоксифенил-N - [(2-метоксифенил) метил] этанамина на промокательной бумаге» . Журнал аналитической токсикологии . 39 (8): 617–23. DOI : 10.1093 / JAT / bkv073 . PMC 4570937 . PMID 26378135 .
- ^ a b c d e f g h Иверсен Л. (4 июня 2013 г.). «Приказ временного класса на препараты бензофуры и НБОМе» . Консультативный совет по злоупотреблению наркотиками . Gov.Uk.
- ^ а б в г Хилл С.Л., Дорис Т., Гурунг С., Катебе С., Ломас А., Данн М. и др. (Июль 2013). «Тяжелая клиническая токсичность, связанная с аналитически подтвержденным рекреационным использованием 25I-NBOMe: серия случаев». Клиническая токсикология . 51 (6): 487–92. DOI : 10.3109 / 15563650.2013.802795 . PMID 23731373 . S2CID 41259282 .
- ^ a b c «Эффекты 2C-I-NBOMe (25I)» . Эровид.
- ^ а б "25И-НБОМе" . Эровид.
- ^ "Доза 2C-I-NBOMe (25I)" . Эровид.
- ^ Области-Холмблад L (2016-12-11). «Использование n-бомбы может убить вас ~ Наркомания сейчас» . Наркомания сейчас | Источник новостей о злоупотреблении психоактивными веществами, наркомании и выздоровлении . Проверено 4 сентября 2020 .
- ^ a b "Смертельные случаи / смерти" . Эровид.
- ^ a b «Еще три синтетических наркотика стали незаконными как минимум на два года» . Управление по борьбе с наркотиками США (DEA). 15 ноября 2013 г.
- ^ Malisow C (13 марта 2013). «Во все тяжкие: продажи наркотиков в цифровом формате, смерти от аналоговых наркотиков» . Хьюстон Пресс.
- ↑ Мартин Н. (1 ноября 2012 г.). «21-летний мужчина умирает после одной капли нового синтетического наркотика на фестивале Voodoo Fest» . NOLA.com.
- ^ "Дело о смертельной передозировке продолжается" . Hibbing Daily Tribune. 5 марта 2015.
- ↑ Giles K (28 апреля 2015 г.). «После смерти друга от передозировки подростки получают отсрочку» . Звездная трибуна.
- Перейти ↑ Lowe LM, Peterson BL, Couper FJ (октябрь 2015 г.). «Обзор случая первой аналитически подтвержденной смерти, связанной с 25I-NBOMe, в штате Вашингтон» . Журнал аналитической токсикологии . 39 (8): 668–71. DOI : 10.1093 / JAT / bkv092 . PMID 26378143 .
- ↑ Rice S (12 сентября 2012 г.). «Новый галлюциногенный препарат 25B-NBOMe и 25I-NBOMe привел к странной смерти южно-австралийского мужчины» . News.com.au . Австралия.
- ^ Feehan C (21 января 2016). «Мощный препарат N-Bomb, ответственный за волну смертей во всем мире - привел к госпитализации шести в Корке» . Ирландский независимый .
- Перейти ↑ Moya PR, Berg KA, Gutiérrez-Hernandez MA, Sáez-Briones P, Reyes-Parada M, Cassels BK, Clarke WP (июнь 2007). «Функциональная селективность галлюциногенных производных фенэтиламина и фенилизопропиламина на человеческих рецепторах 5-гидрокситриптамина (5-HT) 2A и 5-HT2C». Журнал фармакологии и экспериментальной терапии . 321 (3): 1054–61. CiteSeerX 10.1.1.690.3752 . DOI : 10,1124 / jpet.106.117507 . PMID 17337633 . S2CID 11651502 .
- ^ a b Эттруп А., Хансен М., Сантини М.А., Пейн Дж., Гиллингс Н., Палнер М. и др. (Апрель 2011 г.). «Радиосинтез и оценка in vivo ряда замещенных 11C-фенэтиламинов как 5-HT (2A) агонистов ПЭТ-трассеров». Европейский журнал ядерной медицины и молекулярной визуализации . 38 (4): 681–93. DOI : 10.1007 / s00259-010-1686-8 . PMID 21174090 . S2CID 12467684 .
- ^ a b c Николс DE, Frescas SP, Chemel BR, Rehder KS, Zhong D, Lewin AH (июнь 2008 г.). «Меченный тритием N- (2-метоксибензил) -2,5-диметокси-4-йодфенэтиламин (INBMeO) с высокой удельной активностью: высокоаффинный радиолиганд-селективный агонист рецептора 5-HT2A» . Биоорганическая и медицинская химия . 16 (11): 6116–23. DOI : 10.1016 / j.bmc.2008.04.050 . PMC 2719953 . PMID 18468904 .
- Перейти ↑ Silva ME, Heim R, Strasser A, Elz S, Dove S (январь 2011 г.). «Теоретические исследования взаимодействия частичных агонистов с рецептором 5-HT2A». Журнал компьютерного молекулярного дизайна . 25 (1): 51–66. Bibcode : 2011JCAMD..25 ... 51S . CiteSeerX 10.1.1.688.2670 . DOI : 10.1007 / s10822-010-9400-2 . PMID 21088982 . S2CID 3103050 .
- ↑ Halberstadt AL, Geyer MA (февраль 2014 г.). «Влияние галлюциногена 2,5-диметокси-4-йодфенэтиламина (2C-I) и суперпотентных производных N-бензила на реакцию подергивания головы» . Нейрофармакология . 77 : 200–7. DOI : 10.1016 / j.neuropharm.2013.08.025 . PMC 3866097 . PMID 24012658 .
- ↑ Braden MR, Parrish JC, Naylor JC, Nichols DE (декабрь 2006 г.). «Молекулярное взаимодействие остатков серотонинового 5-HT2A рецептора Phe339 (6.51) и Phe340 (6.52) с суперпотентными агонистами N-бензилфенэтиламина». Молекулярная фармакология . 70 (6): 1956–64. DOI : 10,1124 / mol.106.028720 . PMID 17000863 . S2CID 15840304 .
- ^ «Стандарт ядов, октябрь 2015» . Правительство Австралии. Октябрь 2015 г.
- ^ «Положения, вносящие поправки в Положения о пищевых продуктах и лекарствах (Часть J - 2C-фенэтиламины)» . Canada Gazette.
- ^ «关于 印发 《非 药用 类 麻醉 药子 和 精神 药子 列 管 办法》 的 通知» (на китайском языке). Управление по санитарному надзору за качеством пищевых продуктов и медикаментов Китая. 27 сентября 2015. Архивировано из оригинала на 1 октября 2015 года . Проверено 1 октября 2015 года .
- ^ «Исполнительное решение Совета (2014/688 / EU)» . Официальный журнал Европейского Союза. 1 октября 2014 г.
- ^ a b «Правовой статус 2C-I-NBOMe» . Эровид.
- ^ «Закон о злоупотреблении наркотиками 1971 года (кетамин и т. Д.) (Поправка) Приказ 2014» . www.legislation.gov.uk .
- ^ Управление по борьбе с наркотиками (ноябрь 2015 г.). «Списки контролируемых веществ: продление временного включения трех синтетических фенэтиламинов в Список I. Окончательный приказ» (PDF) . Федеральный регистр . 80 (219): 70657–9. PMID 26567439 .
- ^ «Списки контролируемых веществ: Помещение трех синтетических фенэтиламинов в Список I» . Архивировано из оригинального 13 мая 2017 года . Проверено 15 мая 2017 года .
- ^ «ЧАСТЬ 1308 eCFR - РАСПИСАНИЕ КОНТРОЛИРУЕМЫХ ВЕЩЕСТВ, Приложение I.»
- ^ "Legea 194/2011 privind combaterea operatiunilor cu produse soceptibile de avea efecte psihoactive, altele decat cele prevazute de acte normative in vigoare, republicata 2014" . Drept OnLine.
- ^ "Министарство здрава Републикe Србије" .
- ^ "Föreskrifter om ändring i Läkemedelsverkets föreskrifter (LVFS 2011: 10) om förteckningar över narkotika" [Правила, вносящие поправки в правила Агентства по медицинским продуктам (LVFS 2011: 10) в отношении списков лекарств] (PDF) . Läkemedelsverkets (Агентство медицинских продуктов) (на шведском языке). 11 июля 2013 г. Архивировано из оригинального (PDF) 28 сентября 2013 г.
- ^ "衛生 福利 部 子 藥物 管理 署" .