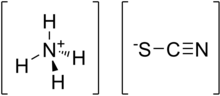 | |||
| Идентификаторы | |||
|---|---|---|---|
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.015.614 | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| NH 4 SCN | |||
| Молярная масса | 76,122 г / моль | ||
| Внешность | Бесцветное гигроскопичное кристаллическое твердое вещество | ||
| Плотность | 1,305 г / см 3 | ||
| Температура плавления | 149,5 ° С (301,1 ° F, 422,6 К) | ||
| Точка кипения | 170 ° С (338 ° F, 443 К) (разлагается) | ||
| 128 г / 100 мл (0 ° С) | |||
| Растворимость | растворим в жидком аммиаке , спирте , ацетоне | ||
| -48,1 · 10 −6 см 3 / моль | |||
| Опасности | |||
| Паспорт безопасности | Внешний паспорт безопасности материала | ||
| NFPA 704 (огненный алмаз) | |||
| Родственные соединения | |||
Другие анионы | Цианат аммония Цианид аммония | ||
Другие катионы | Тиоцианат натрия Тиоцианат калия | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Тиоцианат аммония представляет собой неорганическое соединение с формулой NH 4 SCN. Это соль из аммония катиона и тиоцианата аниона .
Использует [ редактировать ]
Тиоцианат аммония используется в производстве гербицидов , тиомочевины и прозрачных искусственных смол ; в спичках ; как стабилизатор в фотографии; в различных антикоррозионных составах; как адъювант при крашении текстиля и печати; как индикатор на нефтяных месторождениях; при отделении гафния от циркония и титриметрическом анализе.
В мае 1945 года генерал ВВС США Виктор Э. Бетрандиас выдвинул своему начальнику генералу Арнольду предложение использовать тиоцианат аммония для сокращения посевов риса в Японии в рамках бомбардировок их страны . [1]
Тиоцианат аммония также можно использовать для определения содержания железа в безалкогольных напитках колориметрическим методом.
Тиоцианат аммония может также использоваться для отделения хинидина от жидкостей после выделения хинина из нейтрального водного раствора сульфата. Соль добавляется к горячему раствору, и образующееся смолистое твердое вещество отделяется от жидкости. Затем твердое вещество нагревают с обратным холодильником с метанолом, который растворяет большую часть примесей, оставляя тиоцианат хинидина в виде твердого кристаллического вещества с чистотой 90-95%. После разделения (обычно центрифугированием) твердое вещество может быть подвергнуто дальнейшей очистке до фармацевтического качества. (Хинидин используется для лечения сердечной аритмии и поэтому имеет большую ценность.)
Подготовка [ править ]
Тиоцианат аммония получают реакцией сероуглерода с водным аммиаком . В этой реакции образуется дитиокарбамат аммония , который при нагревании разлагается на тиоцианат аммония и сероводород :
- CS 2 + 2 NH 3 (водн.) → NH 2 C (= S) SNH 4 → NH 4 SCN + H 2 S
Реакции [ править ]
Тиоцианат аммония устойчив на воздухе; однако при нагревании он изомеризуется в тиомочевину :
Равновесные смеси при 150 ° C и 180 ° C содержат 30,3% и 25,3% (по массе) тиомочевины соответственно. При нагревании до 200 ° C сухой порошок разлагается на аммиак, сероводород и сероуглерод , оставляя остаток тиоцианата гуанидиния .
NH 4 SCN является слабокислым из-за иона аммония; он реагирует с гидроксидами щелочных металлов, такими как гидроксид натрия или гидроксид калия, с образованием тиоцианата натрия или тиоцианата калия вместе с водой и аммиаком. Тиоцианат-анион, в частности, реагирует с солями трехвалентного железа с образованием темно-красного тиоцианатного комплекса трехвалентного железа:
- 6 SCN - + Fe 3+ → [Fe (SCN) 6 ] 3–
Тиоцианат аммония реагирует с несколькими ионами металлов, включая медь, серебро, цинк, свинец и ртуть, образуя их тиоцианатные осадки, которые можно экстрагировать в органические растворители.
Ссылки [ править ]
- ^ Джон Дэвид Чаппелл (1997). Перед бомбой: как Америка подошла к концу Тихоокеанской войны . Университетское издательство Кентукки. С. 91–92. ISBN 978-0-8131-7052-7.
- А.Ф. Уэллс, Структурная неорганическая химия , 5-е изд., Oxford University Press, Оксфорд, Великобритания, 1984. ISBN 978-0198553700


