Антиоксиданты - это соединения , подавляющие окисление . Окисление - это химическая реакция, которая может производить свободные радикалы , что приводит к цепным реакциям, которые могут повредить клетки организмов. Антиоксиданты, такие как тиолы или аскорбиновая кислота (витамин С), прекращают эти цепные реакции. Чтобы сбалансировать окислительный стресс , растения и животные поддерживают сложные системы перекрывающихся антиоксидантов, таких как глутатион и ферменты (например, каталаза и супероксиддисмутаза).), Произведенные внутри страны , или пищевые антиоксиданты витамина С и витамином Е .
Термин «антиоксидант» в основном используется для двух совершенно разных групп веществ: промышленных химикатов , которые добавляют в продукты для предотвращения окисления, и природных соединений, присутствующих в пищевых продуктах и тканях . Первые, промышленные антиоксиданты, имеют разнообразное применение: действуют в качестве консервантов в пищевых продуктах и косметике и в качестве ингибиторов окисления в резине, синтетических пластмассах и топливе. [1]
Не было доказано, что антиоксидантные пищевые добавки улучшают здоровье людей или эффективны в предотвращении заболеваний. [2] Добавки бета-каротина , витамина А и витамина Е не оказывают положительного влияния на уровень смертности [3] [4] или риск рака . [5] [ необходимо обновить ] [6] Кроме того, добавки селена или витамина Е не снижают риск сердечно-сосудистых заболеваний . [7] [8]
Воздействие на здоровье [ править ]
Отношение к диете [ править ]
Хотя для хорошего здоровья требуются определенные уровни витаминов- антиоксидантов в рационе, все еще ведутся серьезные споры о том, обладают ли богатые антиоксидантами продукты или добавки противозачаточной активностью. Более того, если они действительно полезны, неизвестно, какие антиоксиданты полезны для здоровья в рационе и в каких количествах сверх обычного рациона. [9] [10] [11] Некоторые авторы оспаривают гипотезу о том, что витамины-антиоксиданты могут предотвращать хронические заболевания, [9] [12], а другие заявляют, что гипотеза недоказана и ошибочна. [13] Полифенолы , обладающие антиоксидантными свойствами in vitro , обладают неизвестной антиоксидантной активностью in vivo.из-за обширного метаболизма после переваривания и небольшого количества клинических доказательств эффективности. [14]
Взаимодействия [ править ]
Обычные фармацевтические препараты (и добавки) с антиоксидантными свойствами могут влиять на эффективность некоторых противоопухолевых препаратов и лучевой терапии . [15]
Побочные эффекты [ править ]
Относительно сильные восстанавливающие кислоты могут иметь антинутриентный эффект, связываясь с пищевыми минералами, такими как железо и цинк, в желудочно-кишечном тракте и предотвращая их всасывание. [16] Примерами являются щавелевая кислота , дубильные вещества и фитиновая кислота , которых много в растительных диетах. [17] Дефицит кальция и железа не редкость в рационах питания в развивающихся странах, где едят меньше мяса и где высокое потребление фитиновой кислоты из бобов и пресного цельного зерна.хлеб. Однако проращивание, замачивание или микробная ферментация - это все домашние стратегии, которые снижают содержание фитатов и полифенолов в неочищенных злаках. Сообщалось об увеличении абсорбции Fe, Zn и Ca у взрослых, которых кормили дефитинизированными злаками, по сравнению со злаками, содержащими их природный фитат. [18]
| Еда | Уменьшение присутствия кислоты |
|---|---|
| Какао-бобы и шоколад, шпинат , репа и ревень [19] | Щавелевая кислота |
| Цельнозерновые , кукуруза, бобовые [20] | Фитиновая кислота |
| Чай, фасоль , капуста [19] [21] | Танины |
Высокие дозы некоторых антиоксидантов могут иметь долгосрочные вредные последствия. Бета-каротин и ретинол Испытание эффективности (CARET) исследование больных раком легкого обнаружили , что курильщики данные добавки , содержащие бета-каротин и витамин А увеличились показатели рака легких. [22] Последующие исследования подтвердили эти побочные эффекты. [23] Эти вредные эффекты могут также наблюдаться у некурящих, поскольку один метаанализ, включающий данные примерно 230 000 пациентов, показал, что добавление β-каротина, витамина A или витамина E связано с повышенной смертностью, но не выявило значительного эффекта от витамин С. [24]Никакого риска для здоровья не наблюдалось, когда все рандомизированные контролируемые исследования были изучены вместе, но рост смертности был обнаружен, когда отдельно рассматривались только исследования высокого качества и с низким риском смещения. [25] Поскольку большинство этих исследований с низким уровнем систематической ошибки касалось пожилых людей или людей с заболеваниями, эти результаты могут не применяться к населению в целом. [26] Этот метаанализ был позже повторен и расширен теми же авторами, подтвердив предыдущие результаты. [25] Эти две публикации согласуются с некоторыми предыдущими метаанализами, которые также предположили, что добавление витамина E увеличивает смертность, [27] и что антиоксидантные добавки увеличивают риск рака толстой кишки.. [28] Бета-каротин может также вызвать рак легких . [28] [29] В целом, большое количество клинических испытаний антиоксидантных добавок позволяет предположить, что либо эти продукты не влияют на здоровье, либо вызывают небольшое увеличение смертности среди пожилых или уязвимых групп населения. [9] [10] [24]
Окислительная проблема в биологии [ править ]
Парадокс в метаболизме заключается в том, в то время как подавляющее большинство сложной жизни на Земле требует кислорода для своего существования кислорода является очень реактивным элементом , который повреждает живые организмы, производя активные формы кислорода . [30] Следовательно, организмы содержат сложную сеть антиоксидантных метаболитов и ферментов, которые работают вместе, чтобы предотвратить окислительное повреждение клеточных компонентов, таких как ДНК , белки и липиды . [31] [32]В общем, антиоксидантные системы либо предотвращают образование этих реактивных частиц, либо удаляют их до того, как они могут повредить жизненно важные компоненты клетки. [30] [31] Однако активные формы кислорода также выполняют полезные клеточные функции, такие как передача сигналов окислительно-восстановительного потенциала . Таким образом, функция антиоксидантных систем заключается не в полном удалении окислителей, а в поддержании их на оптимальном уровне. [33]
Активные формы кислорода, продуцируемые в клетках, включают перекись водорода (H 2 O 2 ), хлорноватистую кислоту (HClO) и свободные радикалы, такие как гидроксильный радикал (· OH) и супероксид-анион (O 2 - ). [34] Гидроксильный радикал особенно нестабилен и будет реагировать быстро и неспецифично с большинством биологических молекул. Этот вид образуется из перекиси водорода в окислительно - восстановительных реакциях, катализируемых металлами, таких как реакция Фентона . [35] Эти окислители могут повредить клетки, запуская цепные химические реакции, такие какперекисное окисление липидов или окисление ДНК или белков. [31] Повреждение ДНК может вызвать мутации и, возможно, рак, если его не исправить с помощью механизмов репарации ДНК , [36] [37], в то время как повреждение белков вызывает ингибирование ферментов, денатурацию и деградацию белков . [38]
Использование кислорода в процессе выработки метаболической энергии приводит к образованию активных форм кислорода. [39] В этом процессе супероксид-анион образуется как побочный продукт нескольких этапов в цепи переноса электронов . [40] Особенно важным является восстановление кофермента Q в комплексе III , поскольку в качестве промежуточного соединения (Q · - ) образуется высокореактивный свободный радикал . Этот нестабильный промежуточный продукт может привести к "утечке" электронов, когда электроны прыгают прямо на кислород и образуют супероксид-анион, вместо того, чтобы проходить через нормальную серию хорошо контролируемых реакций цепи переноса электронов. [41]Перекись также производятся от окисления восстановленных флавопротеидов , такие как сложный I . [42] Однако, хотя эти ферменты могут производить окислители, относительная важность цепи переноса электронов для других процессов, которые генерируют пероксид, неясна. [43] [44] В растениях, водорослях и цианобактериях активные формы кислорода также образуются во время фотосинтеза , [45] особенно в условиях высокой интенсивности света . [46] Этот эффект частично компенсируется участием каротиноидов в фотоингибировании., Так и в морских водорослей и цианобактерий, путем большого количества иодида и селена , [47] , который включает в себя эти антиоксиданты , реагирующие с чрезмерной восстановленных форм фотосинтетических реакционных центров , чтобы предотвратить образование активных форм кислорода. [48] [49]
Примеры биоактивных антиоксидантных соединений [ править ]
Антиоксиданты подразделяются на два широких подразделения, в зависимости от того, растворимы ли они в воде ( гидрофильные ) или в липидах ( липофильные ). Как правило, водорастворимые антиоксиданты реагируют с окислителями в цитозоле клетки и плазме крови , в то время как жирорастворимые антиоксиданты защищают клеточные мембраны от перекисного окисления липидов . [31] Эти соединения могут быть синтезированы в организме или получены с пищей. [32] Различные антиоксиданты присутствуют в жидкостях и тканях организма в широком диапазоне концентраций , например, глутатион или убихинон.в основном присутствуют в клетках, тогда как другие, такие как мочевая кислота , распределяются более равномерно (см. таблицу ниже). Некоторые антиоксиданты обнаруживаются только в нескольких организмах, и эти соединения могут иметь важное значение для патогенов и могут быть факторами вирулентности . [50]
Относительная важность и взаимодействие между этими различными антиоксидантами - очень сложный вопрос, поскольку различные антиоксидантные соединения и антиоксидантные ферментные системы оказывают синергетическое и взаимозависимое действие друг на друга. [51] [52] Таким образом, действие одного антиоксиданта может зависеть от правильного функционирования других членов антиоксидантной системы. [32] Степень защиты, обеспечиваемая любым антиоксидантом, также будет зависеть от его концентрации, его реакционной способности по отношению к конкретным рассматриваемым реактивным формам кислорода и состояния антиоксидантов, с которыми он взаимодействует. [32]
Некоторые соединения способствуют антиоксидантной защите, хелатируя переходные металлы и предотвращая их катализирование образования свободных радикалов в клетке. Особенно важна способность связывать железо, что является функцией железосвязывающих белков, таких как трансферрин и ферритин . [44] Селен и цинк обычно называют антиоксидантными питательными веществами , но эти химические элементы сами по себе не обладают антиоксидантным действием и вместо этого необходимы для активности некоторых антиоксидантных ферментов, как обсуждается ниже.
| Антиоксидант | Растворимость | Концентрация в сыворотке крови человека ( мкМ ) | Концентрация в ткани печени ( мкмоль / кг ) |
|---|---|---|---|
| Аскорбиновая кислота ( витамин С ) | Вода | 50–60 [53] | 260 (человек) [54] |
| Глутатион | Вода | 4 [55] | 6 400 (человек) [54] |
| Липоевая кислота | Вода | 0,1–0,7 [56] | 4–5 (крыса) [57] |
| Мочевая кислота | Вода | 200–400 [58] | 1,600 (человек) [54] |
| Каротины | Липид | β-каротин : 0,5–1 [59] ретинол (витамин А): 1–3 [60] | 5 (человек, общие каротиноиды) [61] |
| α-токоферол (витамин Е) | Липид | 10–40 [60] | 50 (человек) [54] |
| Убихинол (коэнзим Q) | Липид | 5 [62] | 200 (человек) [63] |
Мочевая кислота [ править ]
Мочевая кислота является антиоксидантом с самой высокой концентрацией в крови человека. Мочевая кислота (UA) представляет собой оксипурин-антиоксидант, вырабатываемый из ксантина ферментом ксантиноксидазой , и является промежуточным продуктом метаболизма пуринов . [64] Почти у всех наземных животных уратоксидаза дополнительно катализирует окисление мочевой кислоты до аллантоина , [65] но у людей и большинства высших приматов ген уратоксидазы нефункционален, поэтому дальнейшее расщепление UA не происходит. [65] [66] Эволюционные причины потери превращения уратов в аллантоин остаются предметом активных предположений. [67] [68]Антиоксидантное действие мочевой кислоты привело исследователей к предположению, что эта мутация была полезна для первых приматов и людей. [68] [69] Исследования высотной акклиматизации подтверждают гипотезу о том, что ураты действуют как антиоксидант, уменьшая окислительный стресс, вызванный высокогорной гипоксией. [70]
Мочевая кислота имеет самую высокую концентрацию среди всех антиоксидантов крови [58] и обеспечивает более половины общей антиоксидантной способности сыворотки крови человека. [71] Антиоксидантная активность мочевой кислоты также сложна, учитывая, что она не вступает в реакцию с некоторыми окислителями, такими как супероксид , но действует против пероксинитрита , [72] пероксидов и хлорноватистой кислоты . [64] Обеспокоенность повышенным вкладом UA в подагру следует рассматривать как один из многих факторов риска. [73] Сам по себе связанный с UA риск подагры на высоких уровнях (415–530 мкмоль / л) составляет всего 0,5% в год с повышением до 4,5% в год в UA.уровни перенасыщения (535+ мкмоль / л). [74] Многие из этих вышеупомянутых исследований определили антиоксидантное действие УК в пределах нормальных физиологических уровней, [70] [72], а некоторые обнаружили антиоксидантную активность на уровне до 285 мкмоль / л. [75]
Витамин С [ править ]
Аскорбиновая кислота или витамин С представляет собой катализатор окисления-восстановления моносахаридов ( окислительно- восстановительный ), обнаруживаемый как у животных, так и у растений. [76] Поскольку один из ферментов, необходимых для производства аскорбиновой кислоты, был утерян в результате мутации во время эволюции приматов , люди должны получать его из своего рациона; поэтому это диетический витамин. [76] [77] Большинство других животных способны вырабатывать это соединение в своем организме и не нуждаются в нем в своем рационе. [78] Аскорбиновая кислота необходима для превращения проколлагена в коллаген путем окисления остатки пролина до гидроксипролина . [76] В других клетках он поддерживается в восстановленной форме за счет реакции с глутатионом, которая может катализироваться протеиндисульфидизомеразой и глутаредоксинами . [79] [80] Аскорбиновая кислота является окислительно-восстановительным катализатором, который может восстанавливать и тем самым нейтрализовать химически активные формы кислорода, такие как перекись водорода. [76] [81] Помимо своего прямого антиоксидантного действия, аскорбиновая кислота также является субстратом для окислительно-восстановительного фермента аскорбатпероксидазы , функции, которая используется для устойчивости растений к стрессу. [82]Аскорбиновая кислота присутствует в больших количествах во всех частях растений и может достигать 20 миллимолярных концентраций в хлоропластах . [83]
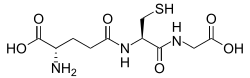
Глутатион [ править ]
Глутатион - это цистеин- содержащий пептид, который встречается в большинстве форм аэробной жизни. [84] Он не требуется в диете и вместо этого синтезируется в клетках из составляющих его аминокислот . [85] Глутатион обладает антиоксидантными свойствами, поскольку тиоловая группа в его цистеиновой части является восстанавливающим агентом и может обратимо окисляться и восстанавливаться. В клетках глутатион поддерживается в восстановленной форме ферментом глутатионредуктазой и, в свою очередь, снижает другие метаболиты и ферментные системы, такие как аскорбат в цикле глутатион-аскорбат , глутатионпероксидазы.и глутаредоксины , а также непосредственно реагирующие с окислителями. [79] Благодаря высокой концентрации и центральной роли в поддержании окислительно-восстановительного состояния клетки, глутатион является одним из важнейших клеточных антиоксидантов. [84] В некоторых организмов глутатион заменены другими тиолов, такими как mycothiol в актиномицетов , bacillithiol в некоторых грам-положительных бактерий , [86] [87] или путем trypanothione в кинетопластиды . [88] [89]
Витамин Е [ править ]
Витамин Е - это собирательное название набора из восьми родственных токоферолов и токотриенолов , жирорастворимых витаминов с антиоксидантными свойствами. [90] [91] Из них α-токоферол наиболее изучен, так как он имеет наивысшую биодоступность , при этом организм преимущественно абсорбирует и метаболизирует эту форму. [92]
Было заявлено, что форма α-токоферола является наиболее важным жирорастворимым антиоксидантом и что она защищает мембраны от окисления, реагируя с липидными радикалами, образующимися в цепной реакции перекисного окисления липидов. [90] [93] Это удаляет промежуточные продукты свободных радикалов и предотвращает продолжение реакции распространения. В результате этой реакции образуются окисленные α-токофероксильные радикалы, которые могут быть возвращены в активную восстановленную форму путем восстановления другими антиоксидантами, такими как аскорбат, ретинол или убихинол. [94] Это согласуется с результатами, показывающими, что α-токоферол, но не водорастворимые антиоксиданты, эффективно защищает клетки с дефицитом глутатионпероксидазы 4 ( GPX4 ) от гибели клеток. [95] GPx4 - единственный известный фермент, который эффективно восстанавливает гидропероксиды липидов в биологических мембранах.
Однако роль и важность различных форм витамина Е в настоящее время неясны [96] [97], и даже было высказано предположение, что наиболее важная функция α-токоферола - это сигнальная молекула , при этом эта молекула не имеет существенного значения. роль в метаболизме антиоксидантов. [98] [99] Функции других форм витамина Е еще менее изучены, хотя γ-токоферол является нуклеофилом, который может реагировать с электрофильными мутагенами, [92] и токотриенолы могут играть важную роль в защите нейронов от повреждений. [100]
Прооксидантная активность [ править ]
Антиоксиданты, являющиеся восстановителями, также могут действовать как прооксиданты. Например, витамин C обладает антиоксидантной активностью, когда восстанавливает окисляющие вещества, такие как перекись водорода; [101] однако он также будет восстанавливать ионы металлов, которые генерируют свободные радикалы в результате реакции Фентона . [35] [102]
- 2 Fe 3+ + аскорбат → 2 Fe 2+ + дегидроаскорбат
- 2 Fe 2+ + 2 H 2 O 2 → 2 Fe 3+ + 2 OH · + 2 OH -
Относительная важность антиоксидантной и прооксидантной активности антиоксидантов является областью текущих исследований, но витамин С, который проявляет свое действие как витамин путем окисления полипептидов, по-видимому, оказывает в организме человека в основном антиоксидантное действие. [102] Однако меньше данных доступно для других пищевых антиоксидантов, таких как витамин E, [103] или полифенолы . [104] [105] Аналогичным образом, патогенез заболеваний, связанных с гиперурикемией, вероятно, связан с прямыми и косвенными прооксидантными свойствами мочевой кислоты. [ необходима цитата ]
То есть, как это ни парадоксально, агенты, которые обычно считаются антиоксидантами, могут действовать как условные прооксиданты и фактически увеличивать окислительный стресс. Помимо аскорбата, важные с медицинской точки зрения условные прооксиданты включают мочевую кислоту и сульфгидриламинокислоты, такие как гомоцистеин . Как правило, в качестве катализатора используется какой-либо металл переходного ряда, например медь или железо. Потенциальная роль прооксидантной роли мочевой кислоты в (например) атеросклерозе и ишемическом инсульте рассмотрена выше. Другой пример - постулируемая роль гомоцистеина в развитии атеросклероза. [ необходима цитата ]
Ферментные системы [ править ]
Как и в случае с химическими антиоксидантами, клетки защищены от окислительного стресса взаимодействующей сетью антиоксидантных ферментов. [30] [31] Здесь супероксид, высвобождаемый в результате таких процессов, как окислительное фосфорилирование , сначала превращается в перекись водорода, а затем восстанавливается с образованием воды. Этот путь детоксикации является результатом действия множества ферментов: супероксиддисмутазы катализируют первую стадию, а затем каталазы и различные пероксидазы удаляют перекись водорода. Как и в случае антиоксидантных метаболитов, вклад этих ферментов в антиоксидантную защиту может быть трудно отделить друг от друга, но поколение трансгенных мышей, лишенных только одного антиоксидантного фермента, может быть информативным. [106]
Супероксиддисмутаза, каталаза и пероксиредоксины [ править ]
Супероксиддисмутазы (SOD) - это класс близкородственных ферментов, которые катализируют распад супероксид-аниона на кислород и перекись водорода. [107] [108] Ферменты СОД присутствуют почти во всех аэробных клетках и во внеклеточных жидкостях. [109] Ферменты супероксиддисмутазы содержат кофакторы ионов металлов, которые, в зависимости от изофермента, могут быть медью, цинком, марганцем или железом. У человека СОД медь / цинк присутствует в цитозоле , тогда как СОД марганца присутствует в митохондриях . [108] Существует также третья форма СОД во внеклеточной жидкости , которая содержит медь и цинк в своих активных центрах. [110]Митохондриальный изофермент кажется наиболее биологически важным из этих трех, поскольку мыши, лишенные этого фермента, умирают вскоре после рождения. [111] Напротив, мыши, у которых отсутствует SOD медь / цинк (Sod1), жизнеспособны, но имеют многочисленные патологии и сокращенную продолжительность жизни (см. Статью о супероксиде ), в то время как мыши без внеклеточной SOD имеют минимальные дефекты (чувствительные к гипероксии ). [106] [112] У растений изоферменты СОД присутствуют в цитозоле и митохондриях, а железная СОД, обнаруженная в хлоропластах , отсутствует у позвоночных и дрожжей . [113]
Каталазы - это ферменты, которые катализируют превращение перекиси водорода в воду и кислород с использованием кофактора железа или марганца. [114] [115] Этот белок находится в пероксисомах большинства эукариотических клеток. [116] Каталаза - необычный фермент, поскольку, хотя перекись водорода является ее единственным субстратом, она действует по механизму пинг-понга . Здесь его кофактор окисляется одной молекулой перекиси водорода, а затем регенерируется путем переноса связанного кислорода на вторую молекулу субстрата. [117] Несмотря на очевидную важность удаления перекиси водорода, люди с генетическим дефицитом каталазы - « акаталаземия » - или мышигенно-инженерные, полностью лишенные каталазы, мало страдают от побочных эффектов. [118] [119]
Пероксиредоксины - это пероксидазы, которые катализируют восстановление пероксида водорода, органических гидропероксидов , а также пероксинитрита . [121] Они делятся на три класса: типичные пероксиредоксины 2-цистеина; атипичные пероксиредоксины 2-цистеина; и пероксиредоксины 1-цистеина. [122] Эти ферменты имеют один и тот же основной каталитический механизм, в котором окислительно-восстановительный цистеин (перекисный цистеин) в активном центре окисляется до сульфеновой кислоты под действием пероксидного субстрата. [123] Чрезмерное окисление цистеинового остатка в пероксиредоксинах инактивирует эти ферменты, но это может быть отменено действием сульфиредоксина .[124] Пероксиредоксины, по-видимому, играют важную роль в метаболизме антиоксидантов, поскольку мыши, лишенные пероксиредоксина 1 или 2, сокращают продолжительность жизни и страдают гемолитической анемией , в то время как растения используют пероксиредоксины для удаления перекиси водорода, образующейся в хлоропластах. [125] [126] [127]
Системы тиоредоксина и глутатиона [ править ]
Тиоредоксин система содержит 12-K Da белка тиоредоксин и его компаньон тиоредоксин - редуктазы . [128] Белки, относящиеся к тиоредоксину, присутствуют во всех секвенированных организмах. Растения, такие как Arabidopsis thaliana , имеют особенно большое разнообразие изоформ. [129] Активный центр тиоредоксина состоит из двух соседних цистеинов как часть высококонсервативного мотива CXXC , который может циклически перемещаться между активной формой дитиола (восстановленной) и окисленным дисульфидом.форма. В активном состоянии тиоредоксин действует как эффективный восстанавливающий агент, улавливая активные формы кислорода и поддерживая другие белки в их восстановленном состоянии. [130] После окисления активный тиоредоксин регенерируется под действием тиоредоксинредуктазы с использованием НАДФН в качестве донора электронов . [131]
Система глутатиона включает глутатион, глутатионредуктазу , глутатионпероксидазы и S -трансферазы глутатиона . [84] Эта система обнаружена у животных, растений и микроорганизмов. [84] [132] Глутатионпероксидаза представляет собой фермент , содержащий четыре селен - кофакторов , который катализирует распад перекиси водорода и органических гидропероксидов. У животных существует по крайней мере четыре различных изофермента глутатионпероксидазы . [133]Глутатионпероксидаза 1 является наиболее распространенным и очень эффективным поглотителем перекиси водорода, в то время как глутатионпероксидаза 4 наиболее активна с гидропероксидами липидов. Удивительно, но глутатионпероксидаза 1 не является незаменимой, поскольку мыши, лишенные этого фермента, имеют нормальную продолжительность жизни [134], но они гиперчувствительны к индуцированному окислительному стрессу. [135] Кроме того, S- трансферазы глутатиона проявляют высокую активность в отношении перекисей липидов. [136] Эти ферменты находятся на особенно высоком уровне в печени и также участвуют в детоксикационном метаболизме. [137]
Использование в технологии [ править ]
Консерванты [ править ]
Антиоксиданты используются в качестве пищевых добавок, чтобы защитить пищу от порчи . Воздействие кислорода и солнечного света - два основных фактора окисления пищи, поэтому пищу можно сохранить, храня ее в темноте и запечатывая в контейнерах или даже покрывая воском, как в случае с огурцами. Однако, поскольку кислород также важен для дыхания растений , хранение растительных материалов в анаэробных условиях приводит к неприятным запахам и непривлекательным цветам. [138] Следовательно, упаковка свежих фруктов и овощей содержит ~ 8% кислорода в атмосфере. Антиоксиданты являются особенно важным классом консервантов, поскольку в отличие от бактериальных или грибковыхпорча, реакции окисления все еще протекают относительно быстро в замороженных или охлажденных пищевых продуктах. [139] Эти консерванты включают природные антиоксиданты, такие как аскорбиновая кислота (AA, E300) и токоферолы (E306), а также синтетические антиоксиданты, такие как пропилгаллат (PG, E310), третичный бутилгидрохинон (TBHQ), бутилированный гидроксианизол (BHA, E320). ) и бутилированный гидрокситолуол (BHT, E321). [140] [141]
Наиболее распространенными молекулами, подвергающимися окислению, являются ненасыщенные жиры; окисление делает их прогорклыми . [142] Поскольку окисленные липиды часто обесцвечиваются и обычно имеют неприятный привкус, например металлический или сернистый привкус, важно избегать окисления в богатой жирами пище. Таким образом, эти продукты редко сохраняются путем сушки; вместо этого они сохраняются путем копчения , соления или ферментации . Даже менее жирные продукты, такие как фрукты, перед сушкой на воздухе опрыскиваются серосодержащими антиоксидантами. Окисление часто катализируется металлами, поэтому жиры, такие как масло, никогда не следует оборачивать алюминиевой фольгой.или хранятся в металлических контейнерах. Некоторые жирные продукты, такие как оливковое масло, частично защищены от окисления благодаря естественному содержанию антиоксидантов, но остаются чувствительными к фотоокислению. [143] Антиоксидантные консерванты также добавляют в косметику на жировой основе, такую как губная помада и увлажняющие средства, чтобы предотвратить прогорклость. [ необходима цитата ]
Промышленное использование [ править ]
Антиоксиданты часто добавляют в промышленные продукты. Общее использование в качестве стабилизаторов в топливах и смазочных материалах для предотвращения окисления, а в бензинах для предотвращения полимеризации , что приводит к образованию двигателя обрастания остатков. [144] В 2014 году мировой рынок природных и синтетических антиоксидантов составлял 2,25 миллиарда долларов США с прогнозом роста до 3,25 миллиарда долларов к 2020 году. [145]
Стабилизаторы антиоксидантных полимеров широко используются для предотвращения разрушения полимеров, таких как каучуки, пластмассы и клеи, которое вызывает потерю прочности и гибкости этих материалов. [146] Полимеры, содержащие двойные связи в основных цепях, такие как натуральный каучук и полибутадиен , особенно подвержены окислению и озонолизу . Их можно защитить антиозонантами . Твердые полимерные продукты начинают трескаться на открытых поверхностях по мере разрушения материала и разрыва цепей. Режим крекинга варьируется между кислородом и озоном.нападение, первое вызывает эффект «сумасшедшего мощения», в то время как воздействие озона вызывает более глубокие трещины, расположенные под прямым углом к деформации растяжения в изделии. Окисление и УФ-деградация также часто связаны, в основном потому, что УФ-излучение создает свободные радикалы за счет разрыва связи. Затем свободные радикалы реагируют с кислородом с образованием пероксирадикалов, которые вызывают еще большее повреждение, часто в цепной реакции . Другие полимеры, подверженные окислению, включают полипропилен и полиэтилен . Первый более чувствителен из-за наличия вторичных атомов углерода.присутствует в каждом повторяющемся блоке. Атака происходит в этот момент, потому что образующийся свободный радикал более стабилен, чем радикал, образованный на первичном атоме углерода . Окисление полиэтилена обычно происходит в слабых звеньях цепи, таких как точки разветвления полиэтилена низкой плотности . [ необходима цитата ]
| Присадка к топливу | Компоненты [147] | Приложения [147] |
|---|---|---|
| АО-22 | N, N'-ди-2-бутил-1,4-фенилендиамин | Турбинные масла, трансформаторные масла , гидравлические жидкости , воски и смазки |
| АО-24 | N, N'-ди-2-бутил-1,4-фенилендиамин | Низкотемпературные масла |
| АО-29 | 2,6-ди-трет-бутил-4-метилфенол | Турбинные масла, трансформаторные масла, гидравлические жидкости, воски, консистентные смазки и бензины |
| АО-30 | 2,4-диметил-6-трет-бутилфенол | Топливо для реактивных двигателей и бензины, включая авиационные бензины |
| АО-31 | 2,4-диметил-6-трет-бутилфенол | Топливо для реактивных двигателей и бензины, включая авиационные бензины |
| АО-32 | 2,4-диметил-6-трет-бутилфенол и 2,6-ди-трет-бутил-4-метилфенол | Топливо для реактивных двигателей и бензины, включая авиационные бензины |
| АО-37 | 2,6-ди-трет-бутилфенол | Реактивное топливо и бензины, широко одобренные для использования в авиационных топливах |
Уровни в еде [ править ]
Витамины-антиоксиданты содержатся в овощах, фруктах, яйцах, бобовых и орехах. Витамины A, C и E могут быть разрушены при длительном хранении или продолжительном приготовлении пищи. [148] Влияние приготовления пищи и обработки пищевых продуктов является сложным, поскольку эти процессы могут также увеличить биодоступность антиоксидантов, таких как некоторые каротиноиды в овощах. [149] Обработанная пища содержит меньше витаминов-антиоксидантов, чем свежие и сырые продукты, поскольку при приготовлении пища подвергается воздействию тепла и кислорода. [150]
| Витамины-антиоксиданты | Пища с высоким содержанием витаминов-антиоксидантов [21] [151] [152] |
|---|---|
| Витамин С (аскорбиновая кислота) | Свежие или замороженные фрукты и овощи |
| Витамин Е (токоферолы, токотриенолы) | Растительные масла , орехи и семена |
| Каротиноиды ( каротины как провитамин А ) | Фрукты, овощи и яйца |
Другие антиоксиданты не поступают с пищей, а вырабатываются в организме. Например, убихинол (коэнзим Q) плохо всасывается в кишечнике и вырабатывается мевалонатным путем . [63] Другой пример - глутатион , который состоит из аминокислот. Поскольку любой глутатион в кишечнике расщепляется на свободный цистеин, глицин и глутаминовую кислоту перед всасыванием, даже большое пероральное употребление мало влияет на концентрацию глутатиона в организме. [153] [154] Хотя большое количество серосодержащих аминокислот, таких как ацетилцистеин, может увеличить глутатион, [155]Нет никаких доказательств того, что потребление большого количества этих предшественников глутатиона полезно для здоровых взрослых. [156]
Измерение и признание ORAC недействительным [ править ]
Измерение содержания полифенолов и каротиноидов в пище - непростой процесс, поскольку антиоксиданты в совокупности представляют собой разнообразную группу соединений с разной реакционной способностью по отношению к различным реактивным формам кислорода. В исследованиях в области пищевых продуктов in vitro способность поглощать кислородные радикалы (ORAC) когда-то была отраслевым стандартом для оценки антиоксидантной силы цельных продуктов, соков и пищевых добавок, в основном по наличию полифенолов . [157] [158] Предыдущие измерения и рейтинги Министерства сельского хозяйства США были отозваны в 2012 году как биологически не относящиеся к здоровью человека, ссылаясь на отсутствие физиологических доказательств того, что полифенолы обладают антиоксидантными свойствами.in vivo . [159] Следовательно, с 2010 года метод ORAC, полученный только в результате экспериментов in vitro , больше не считается актуальным для диет или биологии человека. [159]
Альтернативные измерения содержания антиоксидантов в пищевых продуктах in vitro - также основанные на присутствии полифенолов - включают реагент Фолин-Чокальтеу и анализ эквивалентной антиоксидантной способности Trolox . [160]
История [ править ]
В рамках адаптации к морской жизни наземные растения начали вырабатывать неморские антиоксиданты, такие как аскорбиновая кислота ( витамин С ), полифенолы и токоферолы . Эволюция покрытосеменных растений между 50 и 200 миллионами лет назад привела к развитию многих антиоксидантных пигментов - особенно в юрский период - в качестве химической защиты от активных форм кислорода, которые являются побочными продуктами фотосинтеза . [161]Первоначально термин «антиоксидант» относился к химическому веществу, предотвращающему потребление кислорода. В конце 19 - начале 20 веков обширные исследования были сосредоточены на использовании антиоксидантов в важных промышленных процессах, таких как предотвращение коррозии металлов , вулканизация резины и полимеризация топлива при загрязнении двигателей внутреннего сгорания . [162]
Ранние исследования роли антиоксидантов в биологии были сосредоточены на их использовании для предотвращения окисления ненасыщенных жиров , которое является причиной прогорклости . [163] Антиоксидантную активность можно было измерить, просто поместив жир в закрытый контейнер с кислородом и измерив скорость потребления кислорода. Однако именно идентификация витаминов C и E как антиоксидантов произвела революцию в этой области и привела к осознанию важности антиоксидантов в биохимии живых организмов . [164] [165] Возможные механизмы действияантиоксидантов были впервые исследованы, когда было признано, что вещество с антиоксидантной активностью, вероятно, само по себе легко окисляется. [166] Исследования того, как витамин E предотвращает процесс перекисного окисления липидов, привели к идентификации антиоксидантов как восстановителей, предотвращающих окислительные реакции, часто за счет удаления активных форм кислорода до того, как они могут повредить клетки. [167]
Ссылки [ править ]
- ^ Dabelstein W, Reglitzky A, Schütze A, Reders K (2007). «Автомобильное топливо». Энциклопедия промышленной химии Ульмана . DOI : 10.1002 / 14356007.a16_719.pub2 . ISBN 978-3-527-30673-2.
- ^ «Антиоксиданты: в глубине» . NCCIH. Июнь 2010 Архивировано из оригинала 25 августа 2018 года . Проверено 20 июня 2018 .
- ^ Bjelakovic G, D Николова, Глууд C (2013). «Мета-регрессионные анализы, мета-анализы и последовательные исследования воздействия добавок с бета-каротином, витамином А и витамином Е по отдельности или в различных комбинациях на общую смертность: есть ли у нас доказательства отсутствия вреда? " . PLOS ONE . 8 (9): e74558. Bibcode : 2013PLoSO ... 874558B . DOI : 10.1371 / journal.pone.0074558 . PMC 3765487 . PMID 24040282 .
- ^ Авенир Е.Л., Шмитт Ф., Mendiondo М.С., Маркум JL, Kryscio RJ (июль 2011). «Витамин Е и смертность от всех причин: метаанализ» . Современная наука о старении . 4 (2): 158–70. DOI : 10.2174 / 1874609811104020158 . PMC 4030744 . PMID 21235492 .
- ^ Кортес-Jofre М, Руед JR, Корсине-Муньос G, Фонсек-Кортес С, Caraballoso М, Bonfill COSP Х (2012). «Препараты для профилактики рака легких у здоровых людей». Кокрановская база данных систематических обзоров . 10 : CD002141. DOI : 10.1002 / 14651858.CD002141.pub2 . PMID 23076895 .
- ↑ Jiang L, Yang KH, Tian JH, Guan QL, Yao N, Cao N, Mi DH, Wu J, Ma B, Yang SH (2010). «Эффективность антиоксидантных витаминов и добавок селена в профилактике рака простаты: метаанализ рандомизированных контролируемых исследований». Питание и рак . 62 (6): 719–27. DOI : 10.1080 / 01635581.2010.494335 . PMID 20661819 . S2CID 13611123 .
- Перейти ↑ Rees K, Hartley L, Day C, Flowers N, Clarke A, Stranges S (2013). «Добавки селена для первичной профилактики сердечно-сосудистых заболеваний» (PDF) . Кокрановская база данных систематических обзоров . 1 (1): CD009671. DOI : 10.1002 / 14651858.CD009671.pub2 . PMC 7433291 . PMID 23440843 . Архивировано из оригинального (PDF) 12 августа 2017 года . Проверено 23 июля 2018 года .
- ^ Shekelle П.Г., Мортон СК, Jungvig ЛК, Udani Дж, Спар М, Вт Ср, J Suttorp М, Коултер я, Ньюберри SJ, Харди М (апрель 2004 г.). «Эффект дополнительного витамина Е для профилактики и лечения сердечно-сосудистых заболеваний» . Журнал общей внутренней медицины . 19 (4): 380–9. DOI : 10.1111 / j.1525-1497.2004.30090.x . PMC 1492195 . PMID 15061748 .
- ^ a b c Stanner SA, Hughes J, Kelly CN, Buttriss J (май 2004 г.). «Обзор эпидемиологических доказательств« антиоксидантной гипотезы » » . Питание общественного здравоохранения . 7 (3): 407–22. DOI : 10,1079 / PHN2003543 . PMID 15153272 .
- ^ a b Шенкин А. (февраль 2006 г.). «Ключевая роль микронутриентов». Клиническое питание . 25 (1): 1–13. DOI : 10.1016 / j.clnu.2005.11.006 . PMID 16376462 .
- ^ Woodside СП, McCall D, McGartland C, Янг (ноябрь 2005). «Микроэлементы: потребление с пищей против использования добавок» . Труды общества питания . 64 (4): 543–53. DOI : 10,1079 / PNS2005464 . PMID 16313697 .
- ^ Продовольствие, питание, физическая активность и профилактика рака: глобальная перспектива . Всемирный фонд исследования рака (2007 г.). ISBN 978-0-9722522-2-5 .
- ^ Радуйся Н, Кортес М, Селезень Е.Н., Spallholz JE (июль 2008 г.). «Химиопрофилактика рака: радикальная перспектива». Свободная радикальная биология и медицина . 45 (2): 97–110. DOI : 10.1016 / j.freeradbiomed.2008.04.004 . PMID 18454943 .
- ^ «Флавоноиды» . Институт Линуса Полинга, Государственный университет Орегона, Корваллис. 2016 . Дата обращения 24 июля 2016 .
- ^ Lemmo W (сентябрь 2014). «Возможные взаимодействия отпускаемых по рецепту и без рецепта лекарств, обладающих антиоксидантными свойствами, с лучевой и химиотерапией» . Международный журнал рака . 137 (11): 2525–33. DOI : 10.1002 / ijc.29208 . PMID 25220632 . S2CID 205951215 .
- ^ Hurrell РФ (сентябрь 2003). «Влияние источников растительного белка на биодоступность микроэлементов и минералов» . Журнал питания . 133 (9): 2973S – 7S. DOI : 10.1093 / JN / 133.9.2973S . PMID 12949395 .
- ↑ Хант-младший (сентябрь 2003 г.). «Биодоступность железа, цинка и других микроэлементов из вегетарианских диет» . Американский журнал клинического питания . 78 (3 доп.): 633S – 639S. DOI : 10.1093 / ajcn / 78.3.633S . PMID 12936958 .
- ^ Gibson RS, Perlas L, Хотз C (май 2006). «Повышение биодоступности питательных веществ в растительной пище на бытовом уровне» . Труды общества питания . 65 (2): 160–8. DOI : 10,1079 / PNS2006489 . PMID 16672077 .
- ^ a b Mosha TC, Gaga HE, Pace RD, Laswai HS, Mtebe K (июнь 1995 г.). «Влияние бланширования на содержание антипитательных факторов в избранных овощах». Растительные продукты для питания человека . 47 (4): 361–7. DOI : 10.1007 / BF01088275 . PMID 8577655 . S2CID 1118651 .
- ↑ Sandberg AS (декабрь 2002 г.). «Биодоступность минералов в бобовых культурах» . Британский журнал питания . 88 Suppl 3 (Suppl 3): S281–5. DOI : 10.1079 / BJN / 2002718 . PMID 12498628 .
- ^ а б Бичер GR (октябрь 2003 г.). «Обзор диетических флавоноидов: номенклатура, встречаемость и потребление» . Журнал питания . 133 (10): 3248S – 3254S. DOI : 10.1093 / JN / 133.10.3248S . PMID 14519822 .
- ^ Omenn GS, Goodman GE, Thornquist MD, Balmes J, Cullen MR, Glass A, Keogh JP, Meyskens FL, Valanis B, Williams JH, Barnhart S, Cherniack MG, Brodkin CA, Hammar S (ноябрь 1996). «Факторы риска рака легких и воздействия вмешательства в CARET, испытании эффективности бета-каротина и ретинола» (PDF) . Журнал Национального института рака . 88 (21): 1550–9. DOI : 10.1093 / JNCI / 88.21.1550 . PMID 8901853 .
- ^ Albanes D (июнь 1999). «Бета-каротин и рак легких: тематическое исследование» . Американский журнал клинического питания . 69 (6): 1345S – 50S. DOI : 10.1093 / ajcn / 69.6.1345S . PMID 10359235 .
- ^ a b Белакович Г., Николова Д., Глууд Л.Л., Симонетти Р.Г., Глууд С. (февраль 2007 г.). «Смертность в рандомизированных исследованиях антиоксидантных добавок для первичной и вторичной профилактики: систематический обзор и метаанализ». JAMA . 297 (8): 842–57. DOI : 10,1001 / jama.297.8.842 . PMID 17327526 .
- ^ a b Белакович Г., Николова Д., Глууд Л.Л., Симонетти Р.Г., Глууд С. (14 марта 2012 г.). «Антиоксидантные добавки для предотвращения смертности здоровых участников и пациентов с различными заболеваниями». Кокрановская база данных систематических обзоров . 3 (3): CD007176. DOI : 10.1002 / 14651858.CD007176.pub2 . hdl : 10138/136201 . PMID 22419320 .
- ^ Исследование, цитирующее риски антиоксидантных витаминов, основанное на ошибочной методологии, эксперты утверждают, что выпуск новостей из Университета штата Орегон, опубликованный на ScienceDaily. Проверено 19 апреля 2007 г.
- ^ Миллер ЭР, Пастора-Barriuso R, Далаль D, Riemersma Р.А., Аппель LJ, Guallar Е (январь 2005 г.). «Мета-анализ: добавление высоких доз витамина Е может увеличить смертность от всех причин» . Анналы внутренней медицины . 142 (1): 37–46. DOI : 10.7326 / 0003-4819-142-1-200501040-00110 . PMID 15537682 .
- ^ a b Bjelakovic G, Nagorni A, Nikolova D, Simonetti RG, Bjelakovic M, Gluud C (июль 2006 г.). «Мета-анализ: антиоксидантные добавки для первичной и вторичной профилактики колоректальной аденомы». Пищевая фармакология и терапия . 24 (2): 281–91. DOI : 10.1111 / j.1365-2036.2006.02970.x . PMID 16842454 . S2CID 20452618 .
- ^ Кортес-Jofre, Марсел; Руэда, Хосе-Рамон; Асеньо-Лобос, Клаудиа; Мадрид, Ева; Bonfill Cosp, Ксавье (4 марта 2020 г.). «Препараты для профилактики рака легких у здоровых людей» . Кокрановская база данных систематических обзоров . 3 : CD002141. DOI : 10.1002 / 14651858.CD002141.pub3 . ISSN 1469-493X . PMC 7059884 . PMID 32130738 .
- ^ а б в Дэвис К.Дж. (1995). «Окислительный стресс: парадокс аэробной жизни». Симпозиум Биохимического общества . 61 : 1–31. DOI : 10,1042 / bss0610001 . PMID 8660387 .
- ^ a b c d e Sies H (март 1997 г.). «Окислительный стресс: оксиданты и антиоксиданты» . Экспериментальная физиология . 82 (2): 291–5. DOI : 10.1113 / expphysiol.1997.sp004024 . PMID 9129943 . S2CID 20240552 .
- ^ a b c d Вертуани С., Ангусти А., Манфредини С. (2004). «Сеть антиоксидантов и про-антиоксидантов: обзор». Текущий фармацевтический дизайн . 10 (14): 1677–94. DOI : 10,2174 / 1381612043384655 . PMID 15134565 .
- ^ Ри SG (июнь 2006). «Передача сигналов клетки. H2O2, необходимое зло для передачи сигналов клетки». Наука . 312 (5782): 1882–3. DOI : 10.1126 / science.1130481 . PMID 16809515 . S2CID 83598498 .
- ^ Валько М, Leibfritz Д, Moncol Дж, Кронин МТ, Мазур М, Телсер J (2007). «Свободные радикалы и антиоксиданты в нормальных физиологических функциях и болезнях человека». Международный журнал биохимии и клеточной биологии . 39 (1): 44–84. DOI : 10.1016 / j.biocel.2006.07.001 . PMID 16978905 .
- ^ a b Stohs SJ, Bagchi D (февраль 1995 г.). «Окислительные механизмы при токсичности ионов металлов» (PDF) . Свободная радикальная биология и медицина (Представленная рукопись). 18 (2): 321–36. CiteSeerX 10.1.1.461.6417 . DOI : 10.1016 / 0891-5849 (94) 00159-H . PMID 7744317 .
- ^ Nakabeppu Y, Sakumi K, Сакамото K, Tsuchimoto D, Тсузуки T, Nakatsu Y (апрель 2006). «Мутагенез и канцерогенез, вызванные окислением нуклеиновых кислот». Биологическая химия . 387 (4): 373–9. DOI : 10.1515 / BC.2006.050 . PMID 16606334 . S2CID 20217256 .
- ^ Валько М, Izakovic М, М Мазур, Rhodes CJ, Телсер J (ноябрь 2004 г.). «Роль кислородных радикалов в повреждении ДНК и заболеваемости раком». Молекулярная и клеточная биохимия . 266 (1–2): 37–56. DOI : 10,1023 / Б: MCBI.0000049134.69131.89 . PMID 15646026 . S2CID 207547763 .
- ^ Stadtman ER (август 1992). «Окисление белков и старение» . Наука . 257 (5074): 1220–4. Bibcode : 1992Sci ... 257.1220S . DOI : 10.1126 / science.1355616 . PMID 1355616 .
- ^ Raha S, Robinson BH (октябрь 2000). «Митохондрии, свободные радикалы кислорода, болезни и старение». Направления биохимических наук . 25 (10): 502–8. DOI : 10.1016 / S0968-0004 (00) 01674-1 . PMID 11050436 .
- ^ Lenaz G (2001). «Митохондриальная продукция активных форм кислорода: механизмы и последствия патологии человека» . IUBMB Life . 52 (3–5): 159–64. DOI : 10.1080 / 15216540152845957 . PMID 11798028 . S2CID 45366190 .
- Перейти ↑ Finkel T, Holbrook NJ (ноябрь 2000 г.). «Окислители, окислительный стресс и биология старения». Природа . 408 (6809): 239–47. Bibcode : 2000Natur.408..239F . DOI : 10.1038 / 35041687 . PMID 11089981 . S2CID 2502238 .
- Перейти ↑ Hirst J, King MS, Pryde KR (октябрь 2008 г.). «Производство активных форм кислорода комплексом I». Сделки Биохимического Общества . 36 (Pt 5): 976–80. DOI : 10.1042 / BST0360976 . PMID 18793173 .
- ^ Сивер LC, Имлей JA (ноябрь 2004). «Являются ли респираторные ферменты основным источником внутриклеточной перекиси водорода?» . Журнал биологической химии . 279 (47): 48742–50. DOI : 10.1074 / jbc.M408754200 . PMID 15361522 .
- ^ а б Имлай JA (2003). «Пути окислительного повреждения». Ежегодный обзор микробиологии . 57 : 395–418. DOI : 10.1146 / annurev.micro.57.030502.090938 . PMID 14527285 .
- ^ Demmig-Adams B, Адамс WW (декабрь 2002). «Антиоксиданты в фотосинтезе и питании человека». Наука . 298 (5601): 2149–53. Bibcode : 2002Sci ... 298.2149D . DOI : 10.1126 / science.1078002 . PMID 12481128 . S2CID 27486669 .
- ^ Krieger-Liszkay A (январь 2005). «Производство синглетного кислорода при фотосинтезе». Журнал экспериментальной ботаники . 56 (411): 337–46. CiteSeerX 10.1.1.327.9651 . DOI : 10.1093 / JXB / erh237 . PMID 15310815 .
- ^ Kupper FC, Карпентер LJ, Макфигганс GB, Палмер CJ, Уэйт TJ, Boneberg EM, Woitsch S, Weiller M, Abela R, Grolimund D, Potin P, Butler A, Luther GW, Kroneck PMH, Meyer-Klaucke W, Feiters MC (2008). «Накопление йодида обеспечивает водоросли неорганическим антиоксидантом, влияющим на химический состав атмосферы» . Труды Национальной академии наук . 105 (19): 6954–6958. Bibcode : 2008PNAS..105.6954K . DOI : 10.1073 / pnas.0709959105 . ISSN 0027-8424 . PMC 2383960 . PMID 18458346 .
- ↑ Szabó I, Bergantino E, Giacometti GM (июль 2005 г.). «Световой и кислородный фотосинтез: рассеяние энергии как механизм защиты от фотоокисления» . EMBO Reports . 6 (7): 629–34. DOI : 10.1038 / sj.embor.7400460 . PMC 1369118 . PMID 15995679 .
- ^ Kerfeld CA (октябрь 2004). «Водорастворимые каротиноидные белки цианобактерий» (PDF) . Архивы биохимии и биофизики (Представленная рукопись). 430 (1): 2–9. DOI : 10.1016 / j.abb.2004.03.018 . PMID 15325905 .
- ^ Миллер Р., Britigan В (январь 1997). «Роль оксидантов в патофизиологии микробов» . Обзоры клинической микробиологии . 10 (1): 1–18. DOI : 10,1128 / CMR.10.1.1 . PMC 172912 . PMID 8993856 .
- ^ Chaudière J, Ferrari-Iliou R (1999). «Внутриклеточные антиоксиданты: от химических механизмов к биохимическим». Пищевая и химическая токсикология . 37 (9–10): 949–62. DOI : 10.1016 / S0278-6915 (99) 00090-3 . PMID 10541450 .
- ^ Sies H (июль 1993). «Стратегии антиоксидантной защиты». Европейский журнал биохимии / FEBS . 215 (2): 213–9. DOI : 10.1111 / j.1432-1033.1993.tb18025.x . PMID 7688300 .
- ^ Khaw KT, Woodhouse P (июнь 1995 г.). «Взаимосвязь витамина С, инфекции, гемостатических факторов и сердечно-сосудистых заболеваний» . BMJ . 310 (6994): 1559–63. DOI : 10.1136 / bmj.310.6994.1559 . PMC 2549940 . PMID 7787643 .
- ^ a b c d Evelson P, Travacio M, Repetto M, Escobar J, Llesuy S, Lissi EA (апрель 2001 г.). «Оценка общего реактивного антиоксидантного потенциала (TRAP) гомогенатов тканей и их цитозолей». Архивы биохимии и биофизики . 388 (2): 261–6. DOI : 10,1006 / abbi.2001.2292 . PMID 11368163 .
- ↑ Моррисон Дж. А., Якобсен Д. В., Спречер Д. Л., Робинсон К., Хури П., Дэниелс С. Р. (ноябрь 1999 г.). «Глутатион в сыворотке у подростков мужского пола является предиктором ишемической болезни сердца у родителей» . Тираж . 100 (22): 2244–7. DOI : 10.1161 / 01.CIR.100.22.2244 . PMID 10577998 .
- ^ Teichert Дж, Прейс Р (ноябрь 1992 г.). «ВЭЖХ-методы определения липоевой кислоты и ее восстановленной формы в плазме крови человека». Международный журнал клинической фармакологии, терапии и токсикологии . 30 (11): 511–2. PMID 1490813 .
- ^ Акиба S, Matsugo S, упаковщик L, Кониши T (май 1998). «Анализ липоевой кислоты, связанной с белками, в тканях новым ферментативным методом». Аналитическая биохимия . 258 (2): 299–304. DOI : 10.1006 / abio.1998.2615 . PMID 9570844 .
- ^ a b Гланцунис Г.К., Цимояннис Э.С., Каппас А.М., Галарис Д.А. (2005). «Мочевая кислота и окислительный стресс». Текущий фармацевтический дизайн . 11 (32): 4145–51. DOI : 10,2174 / 138161205774913255 . PMID 16375736 .
- ^ Эль-Sohemy А, Baylin А, Kabagambe Е, Ascherio А, Spiegelman Д, Кампос Н (июль 2002 г.). «Индивидуальные концентрации каротиноидов в жировой ткани и плазме как биомаркеры диетического потребления» . Американский журнал клинического питания . 76 (1): 172–9. DOI : 10.1093 / ajcn / 76.1.172 . PMID 12081831 .
- ^ a b Соуэлл А. Л., Хафф Д. Л., Йегер П. Р., Кодилл С. П., Гюнтер Е. В. (март 1994 г.). «Ретинол, альфа-токоферол, лютеин / зеаксантин, бета-криптоксантин, ликопин, альфа-каротин, транс-бета-каротин и четыре ретиниловых эфира в сыворотке, определяемые одновременно с помощью обращенно-фазовой ВЭЖХ с многоволновым детектированием» . Клиническая химия . 40 (3): 411–6. DOI : 10.1093 / clinchem / 40.3.411 . PMID 8131277 . [ постоянная мертвая ссылка ]
- ↑ Stahl W, Schwarz W, Sundquist AR, Sies H (апрель 1992 г.). «цис-транс-изомеры ликопина и бета-каротина в сыворотке и тканях человека». Архивы биохимии и биофизики . 294 (1): 173–7. DOI : 10.1016 / 0003-9861 (92) 90153-N . PMID 1550343 .
- ^ Зита C, Overvad K, Мортенсен SA, Sindberg CD, Moesgaard S, Hunter DA (2003). «Концентрации коэнзима Q10 в сыворотке крови у здоровых мужчин, получавших 30 или 100 мг кофермента Q10 в течение двух месяцев в рандомизированном контролируемом исследовании». BioFactors . 18 (1–4): 185–93. DOI : 10.1002 / biof.5520180221 . PMID 14695934 . S2CID 19895215 .
- ^ Б Турунен М, Олссон Дж, Dallner G (январь 2004 г.). «Метаболизм и функция коэнзима Q». Biochimica et Biophysica Acta (BBA) - Биомембраны . 1660 (1–2): 171–99. DOI : 10.1016 / j.bbamem.2003.11.012 . PMID 14757233 .
- ^ a b Enomoto A, Endou H (сентябрь 2005 г.). «Роль переносчиков органических анионов (ОАТ) и переносчика уратов (URAT1) в патофизиологии болезней человека». Клиническая и экспериментальная нефрология . 9 (3): 195–205. DOI : 10.1007 / s10157-005-0368-5 . PMID 16189627 . S2CID 6145651 .
- ^ Б У XW, Ли CC, Muzny DM, Каски CT (декабрь 1989). «Уратоксидаза: первичная структура и эволюционные последствия» . Труды Национальной академии наук Соединенных Штатов Америки . 86 (23): 9412–6. Bibcode : 1989PNAS ... 86.9412W . DOI : 10.1073 / pnas.86.23.9412 . PMC 298506 . PMID 2594778 .
- ^ У XW, Muzny DM, Ли CC, Каски CT (январь 1992). «Два независимых мутационных события в потере уратоксидазы во время эволюции гоминоидов». Журнал молекулярной эволюции . 34 (1): 78–84. Bibcode : 1992JMolE..34 ... 78W . DOI : 10.1007 / BF00163854 . PMID 1556746 . S2CID 33424555 .
- ^ Альварес-Ларио В, Macarrón-Висенте J (ноябрь 2010 г.). «Мочевая кислота и эволюция» . Ревматология . 49 (11): 2010–5. DOI : 10.1093 / ревматологических / keq204 . PMID 20627967 .
- ^ а б Ватанабе С., Канг Д.Х., Фенг Л., Накагава Т., Канеллис Дж., Лан Х., Маццали М., Джонсон Р.Дж. (сентябрь 2002 г.). «Мочевая кислота, эволюция гоминоидов и патогенез солевой чувствительности» . Гипертония . 40 (3): 355–60. DOI : 10.1161 / 01.HYP.0000028589.66335.AA . PMID 12215479 .
- Перейти ↑ Johnson RJ, Andrews P, Benner SA, Oliver W (2010). «Премия Теодора Э. Вудворда. Эволюция ожирения: выводы из среднего миоцена» . Труды Американской клинической и климатологической ассоциации . 121 : 295–305, обсуждение 305–8. PMC 2917125 . PMID 20697570 .
- ^ a b Бэйли Дж. К., Бейтс М. Г., Томпсон А. А., Уоринг В. С., Партридж Р. В., Шнопп М. Ф., Симпсон А., Гулливер-Слоан Ф., Максвелл С. Р., Уэбб Д. Д. (май 2007 г.). «Производство эндогенных уратов увеличивает антиоксидантную способность плазмы у здоровых людей, живущих в низинах, находящихся на большой высоте». Сундук . 131 (5): 1473–8. DOI : 10.1378 / chest.06-2235 . PMID 17494796 .
- ↑ Becker BF (июнь 1993 г.). «К физиологической функции мочевой кислоты». Свободная радикальная биология и медицина . 14 (6): 615–31. DOI : 10.1016 / 0891-5849 (93) 90143-I . PMID 8325534 .
- ^ a b Sautin YY, Johnson RJ (июнь 2008 г.). «Мочевая кислота: парадокс оксидант-антиоксидант» . Нуклеозиды, нуклеотиды и нуклеиновые кислоты . 27 (6): 608–19. DOI : 10.1080 / 15257770802138558 . PMC 2895915 . PMID 18600514 .
- ^ Eggebeen AT (сентябрь 2007). «Подагра: обновление» . Американский семейный врач . 76 (6): 801–8. PMID 17910294 .
- ^ Кэмпион EW, Глинн RJ, DeLabry LO (март 1987). «Бессимптомная гиперурикемия. Риски и последствия в исследовании нормативного старения». Американский журнал медицины . 82 (3): 421–6. DOI : 10.1016 / 0002-9343 (87) 90441-4 . PMID 3826098 .
- ^ Назаревич RR, Циолковский W, Vaccaro PS, Ghafourifar P (декабрь 2007). «Влияние краткосрочной кетогенной диеты на окислительно-восстановительный статус крови человека». Исследования омоложения . 10 (4): 435–40. DOI : 10,1089 / rej.2007.0540 . PMID 17663642 .
- ^ a b c d «Витамин С» . Информационный центр по микронутриентам, Институт Линуса Полинга, Университет штата Орегон, Корваллис, Орегон. 1 июля 2018 . Проверено 19 июня 2019 .
- Перейти ↑ Smirnoff N (2001). «Биосинтез L-аскорбиновой кислоты». Кофактор биосинтеза . Витамины и гормоны. 61 . С. 241–66. DOI : 10.1016 / S0083-6729 (01) 61008-2 . ISBN 978-0-12-709861-6. PMID 11153268 .
- ^ Linster CL, Ван Schaftingen E (январь 2007). «Витамин С. Биосинтез, переработка и разложение у млекопитающих» . Журнал FEBS . 274 (1): 1–22. DOI : 10.1111 / j.1742-4658.2006.05607.x . PMID 17222174 . S2CID 21345196 .
- ^ a b Meister A (апрель 1994 г.). «Антиоксидантная система глутатион-аскорбиновая кислота у животных» . Журнал биологической химии . 269 (13): 9397–400. PMID 8144521 .
- ^ Уэллс WW, Сюй DP, Ян YF, Rocque PA (сентябрь 1990). «Тиолтрансфераза (глутаредоксин) млекопитающих и протеиндисульфидизомераза обладают активностью дегидроаскорбатредуктазы» . Журнал биологической химии . 265 (26): 15361–4. PMID 2394726 .
- ^ Padayatty SJ, Katz A, Ван Y, Эк P, Kwon O, Lee JH, Chen S, Corpe C, Датта A, Датта SK, Levine M (февраль 2003). «Витамин С как антиоксидант: оценка его роли в профилактике заболеваний» . Журнал Американского колледжа питания . 22 (1): 18–35. DOI : 10.1080 / 07315724.2003.10719272 . PMID 12569111 . S2CID 21196776 .
- ^ Shigeoka S, Ishikawa T, Tamoi M, Y Miyagawa, Takeda T, Yabuta Y, Yoshimura K (май 2002). «Регуляция и функция изоферментов аскорбатпероксидазы» . Журнал экспериментальной ботаники . 53 (372): 1305–19. DOI : 10.1093 / jexbot / 53.372.1305 . PMID 11997377 .
- Перейти ↑ Smirnoff N, Wheeler GL (2000). «Аскорбиновая кислота в растениях: биосинтез и функции». Критические обзоры в биохимии и молекулярной биологии . 35 (4): 291–314. DOI : 10.1080 / 10409230008984166 . PMID 11005203 . S2CID 85060539 .
- ^ a b c d Meister A, Андерсон ME (1983). «Глутатион». Ежегодный обзор биохимии . 52 : 711–60. DOI : 10.1146 / annurev.bi.52.070183.003431 . PMID 6137189 .
- Перейти ↑ Meister A (ноябрь 1988 г.). «Метаболизм глутатиона и его селективная модификация» . Журнал биологической химии . 263 (33): 17205–8. PMID 3053703 .
- ^ Габалла А, Ньютон GL, Antelmann H, Парсонаж D, Upton H, M Рават, Claiborne A, Фейи RC, Helmann JD (апрель 2010). «Биосинтез и функции бацилтиола, основного низкомолекулярного тиола в бациллах» . Труды Национальной академии наук Соединенных Штатов Америки . 107 (14): 6482–6. Bibcode : 2010PNAS..107.6482G . DOI : 10.1073 / pnas.1000928107 . PMC 2851989 . PMID 20308541 .
- ^ Newton GL, Рават M, La Clair JJ, Jothivasan В.К., Budiarto T, Гамильтон CJ, Claiborne A, Helmann JD, Фейи RC (сентябрь 2009). «Бацилтиол - это тиол-антиоксидант, производимый бациллами» . Природа Химическая биология . 5 (9): 625–627. DOI : 10.1038 / nchembio.189 . PMC 3510479 . PMID 19578333 .
- ^ Фейи RC (2001). «Новые тиолы прокариот». Ежегодный обзор микробиологии . 55 : 333–56. DOI : 10.1146 / annurev.micro.55.1.333 . PMID 11544359 .
- ^ Фэрлемб AH, Cerami A (1992). «Метаболизм и функции трипанотиона в кинетопластиде». Ежегодный обзор микробиологии . 46 : 695–729. DOI : 10.1146 / annurev.mi.46.100192.003403 . PMID 1444271 .
- ^ a b Эррера Э, Барбас С (март 2001 г.). «Витамин Е: действие, метаболизм и перспективы». Журнал физиологии и биохимии . 57 (2): 43–56. DOI : 10.1007 / BF03179812 . PMID 11579997 . S2CID 7272312 .
- Перейти ↑ Packer L, Weber SU, Rimbach G (февраль 2001 г.). «Молекулярные аспекты антиоксидантного действия альфа-токотриенола и клеточной сигнализации» . Журнал питания . 131 (2): 369С – 73С. DOI : 10.1093 / JN / 131.2.369S . PMID 11160563 .
- ^ a b Brigelius-Flohé R, Traber MG (июль 1999 г.). «Витамин Е: функции и обмен веществ». Журнал FASEB . 13 (10): 1145–55. CiteSeerX 10.1.1.337.5276 . DOI : 10.1096 / fasebj.13.10.1145 . PMID 10385606 . S2CID 7031925 .
- ^ Траберу М. Аткинсон J (июль 2007). «Витамин Е, антиоксидант и не более того» . Свободная радикальная биология и медицина . 43 (1): 4–15. DOI : 10.1016 / j.freeradbiomed.2007.03.024 . PMC 2040110 . PMID 17561088 .
- Перейти ↑ Wang X, Quinn PJ (июль 1999 г.). «Витамин Е и его функции в мембранах». Прогресс в исследованиях липидов . 38 (4): 309–36. DOI : 10.1016 / S0163-7827 (99) 00008-9 . PMID 10793887 .
- ↑ Seiler A, Schneider M, Förster H, Roth S, Wirth EK, Culmsee C, Plesnila N, Kremmer E, Rådmark O, Wurst W, Bornkamm GW, Schweizer U, Conrad M (сентябрь 2008 г.). «Глутатионпероксидаза 4 воспринимает и переводит окислительный стресс в зависимую от 12/15 липоксигеназ и опосредованную AIF гибель клеток». Клеточный метаболизм . 8 (3): 237–48. DOI : 10.1016 / j.cmet.2008.07.005 . PMID 18762024 .
- ^ Brigelius-Flohé R, Davies KJ (июль 2007). «Является ли витамин E антиоксидантом, регулятором передачи сигналов и экспрессии генов, или является« нездоровой »пищей? Комментарии к двум сопроводительным документам:« Молекулярный механизм действия альфа-токоферола »А. Аззи и« Витамин E, антиоксидант и не более того "М. Трабера и Дж. Аткинсона". Свободная радикальная биология и медицина . 43 (1): 2–3. DOI : 10.1016 / j.freeradbiomed.2007.05.016 . PMID 17561087 .
- ^ Аткинсон J, Epand РФ, Epand RM (март 2008). «Токоферолы и токотриенолы в мембранах: критический обзор». Свободная радикальная биология и медицина . 44 (5): 739–64. DOI : 10.1016 / j.freeradbiomed.2007.11.010 . PMID 18160049 .
- ^ Ацци A (июль 2007). «Молекулярный механизм действия альфа-токоферола». Свободная радикальная биология и медицина . 43 (1): 16–21. DOI : 10.1016 / j.freeradbiomed.2007.03.013 . PMID 17561089 .
- ^ Zingg JM, Azzi A (май 2004). «Неантиоксидантная активность витамина Е» . Современная лекарственная химия . 11 (9): 1113–33. DOI : 10.2174 / 0929867043365332 . PMID 15134510 . Архивировано из оригинала 6 октября 2011 года.
- ↑ Sen CK, Khanna S, Roy S (март 2006 г.). «Токотриенолы: витамин Е помимо токоферолов» . Науки о жизни . 78 (18): 2088–98. DOI : 10.1016 / j.lfs.2005.12.001 . PMC 1790869 . PMID 16458936 .
- ^ Дуарте TL, Lunec J (июль 2005 г.). «Обзор: когда антиоксидант не является антиоксидантом? Обзор новых действий и реакций витамина С». Свободно-радикальные исследования . 39 (7): 671–86. DOI : 10.1080 / 10715760500104025 . PMID 16036346 . S2CID 39962659 .
- ^ a b Carr A, Frei B (июнь 1999 г.). «Витамин C действует как прооксидант в физиологических условиях?». Журнал FASEB . 13 (9): 1007–24. DOI : 10.1096 / fasebj.13.9.1007 . PMID 10336883 . S2CID 15426564 .
- Перейти ↑ Schneider C (январь 2005 г.). «Химия и биология витамина Е». Молекулярное питание и пищевые исследования . 49 (1): 7–30. DOI : 10.1002 / mnfr.200400049 . PMID 15580660 .
- Перейти ↑ Halliwell B (август 2008 г.). «Полифенолы являются антиоксидантами или прооксидантами? Что мы узнаем из клеточных культур и исследований in vivo?». Архивы биохимии и биофизики . 476 (2): 107–112. DOI : 10.1016 / j.abb.2008.01.028 . PMID 18284912 .
- ^ Ristow M, Zarse K (июнь 2010). «Как повышенный окислительный стресс способствует долголетию и метаболическому здоровью: концепция митохондриального гормезиса (митохондриального гормезиса)». Экспериментальная геронтология . 45 (6): 410–418. DOI : 10.1016 / j.exger.2010.03.014 . PMID 20350594 . S2CID 207727334 .
- ^ Б Хо Ю.С., Magnenat JL, Гаргано M, Cao J (октябрь 1998). «Природа механизмов антиоксидантной защиты: урок трансгенных исследований» . Перспективы гигиены окружающей среды . 106 Дополнение 5 (Дополнение 5): 1219–28. DOI : 10.2307 / 3433989 . JSTOR 3433989 . PMC 1533365 . PMID 9788901 .
- ^ Zelko IN, Mariani TJ, Folz RJ (август 2002). «Мультигенное семейство супероксиддисмутазы: сравнение структур, эволюции и экспрессии генов CuZn-SOD (SOD1), Mn-SOD (SOD2) и EC-SOD (SOD3)». Свободная радикальная биология и медицина . 33 (3): 337–49. DOI : 10.1016 / S0891-5849 (02) 00905-X . PMID 12126755 .
- ^ a b Bannister JV, Bannister WH, Rotilio G (1987). «Аспекты структуры, функции и применения супероксиддисмутазы». CRC Critical Reviews в биохимии . 22 (2): 111–80. DOI : 10.3109 / 10409238709083738 . PMID 3315461 .
- ^ Джонсон F, Giulivi C (2005). «Супероксиддисмутазы и их влияние на здоровье человека». Молекулярные аспекты медицины . 26 (4–5): 340–52. DOI : 10.1016 / j.mam.2005.07.006 . PMID 16099495 .
- ^ Нозик-Grayck E, Suliman HB, Piantadosi CA (декабрь 2005). «Внеклеточная супероксиддисмутаза». Международный журнал биохимии и клеточной биологии . 37 (12): 2466–71. DOI : 10.1016 / j.biocel.2005.06.012 . PMID 16087389 .
- ^ Melov S, Schneider JA, день BJ, Hinerfeld D, Coskun P, Мирра SS, Крапо JD, Уоллес DC (февраль 1998). «Новый неврологический фенотип у мышей, лишенных митохондриальной супероксиддисмутазы марганца». Генетика природы . 18 (2): 159–63. DOI : 10.1038 / ng0298-159 . PMID 9462746 . S2CID 20843002 .
- ^ Реум AG, Эллиот JL, Хоффман EK, Kowall NW, Ферранте RJ, Siwek DF, Wilcox HM, Flood DG, Beal MF, Brown RH, Скотт RW, Снайдер WD (май 1996). «Моторные нейроны у мышей с дефицитом супероксиддисмутазы Cu / Zn развиваются нормально, но демонстрируют повышенную гибель клеток после повреждения аксонов». Генетика природы . 13 (1): 43–7. DOI : 10.1038 / ng0596-43 . PMID 8673102 . S2CID 13070253 .
- ^ Van Camp W, Inze D, Ван Монтегю M (1997). «Регуляция и функция супероксиддисмутаз табака». Свободная радикальная биология и медицина . 23 (3): 515–20. DOI : 10.1016 / S0891-5849 (97) 00112-3 . PMID 9214590 .
- ^ Chelikani P, Fita I, Лоуэн PC (январь 2004). «Разнообразие структур и свойств каталаз» (PDF) . Клеточные и молекулярные науки о жизни (Представленная рукопись). 61 (2): 192–208. DOI : 10.1007 / s00018-003-3206-5 . hdl : 10261/111097 . PMID 14745498 . S2CID 4411482 .
- ^ Zámocký M, F Koller (1999). «Понимание структуры и функции каталаз: ключи от молекулярной эволюции и мутагенеза in vitro» . Прогресс в биофизике и молекулярной биологии . 72 (1): 19–66. DOI : 10.1016 / S0079-6107 (98) 00058-3 . PMID 10446501 .
- ^ Дель - Рио LA, Sandalio LM, Palma JM, Bueno P, Corpas FJ (ноябрь 1992). «Метаболизм кислородных радикалов в пероксисомах и клеточные проявления». Свободная радикальная биология и медицина . 13 (5): 557–80. DOI : 10.1016 / 0891-5849 (92) 90150-F . PMID 1334030 .
- ^ Hiner А.Н., Ворон Е.Л., Thorneley RN, Гарсия-Cánovas F, Родригес-Лопес JN (июль 2002). «Механизмы образования соединения I в пероксидазах гема». Журнал неорганической биохимии . 91 (1): 27–34. DOI : 10.1016 / S0162-0134 (02) 00390-2 . PMID 12121759 .
- ^ Mueller S, Riedel HD, Stremmel W (декабрь 1997). «Прямые доказательства того, что каталаза является преобладающим ферментом, удаляющим H2O2, в эритроцитах человека» . Кровь . 90 (12): 4973–8. DOI : 10.1182 / blood.V90.12.4973 . PMID 9389716 .
- Перейти ↑ Ogata M (февраль 1991). «Акаталаземия». Генетика человека . 86 (4): 331–40. DOI : 10.1007 / BF00201829 . PMID 1999334 .
- ^ Парсонаж Г, Д Юнгблуд, Сарма G, Z Вуд, Карплус Р, Пул л (2005). «Анализ связи между ферментативной активностью и олигомерным состоянием в AhpC, бактериальном пероксиредоксине» . Биохимия . 44 (31): 10583–92. DOI : 10.1021 / bi050448i . PMC 3832347 . PMID 16060667 . PDB 1YEX
- ^ Ри SG, Чэ HZ, Ким K (июнь 2005). «Пероксиредоксины: исторический обзор и предварительный просмотр новых механизмов и новых концепций в передаче сигналов в клетке». Свободная радикальная биология и медицина . 38 (12): 1543–52. DOI : 10.1016 / j.freeradbiomed.2005.02.026 . PMID 15917183 .
- ^ Wood ZA, Шрёдер Е, Робин Харрис J, Poole LB (январь 2003). «Структура, механизм и регуляция пероксиредоксинов». Направления биохимических наук . 28 (1): 32–40. DOI : 10.1016 / S0968-0004 (02) 00003-8 . PMID 12517450 .
- ↑ Claiborne A, Yeh JI, Mallett TC, Luba J, Crane EJ, Charrier V, Parsonage D (ноябрь 1999 г.). «Белок-сульфеновые кислоты: разнообразные роли маловероятного игрока в ферментативном катализе и окислительно-восстановительном регулировании». Биохимия . 38 (47): 15407–16. DOI : 10.1021 / bi992025k . PMID 10569923 .
- ^ Jönsson TJ, Lowther WT (2007). «Белки восстановления пероксиредоксина». Системы пероксиредоксина . Субклеточная биохимия. 44 . С. 115–41. DOI : 10.1007 / 978-1-4020-6051-9_6 . ISBN 978-1-4020-6050-2. PMC 2391273 . PMID 18084892 .
- ^ Neumann CA, Krause DS, Carman CV, Das S, Dubey DP, Abraham JL, Bronson RT, Fujiwara Y, Orkin SH, Van Etten RA (июль 2003 г.). «Важная роль пероксиредоксина Prdx1 в антиоксидантной защите эритроцитов и подавлении опухоли» (PDF) . Природа . 424 (6948): 561–5. Bibcode : 2003Natur.424..561N . DOI : 10,1038 / природа01819 . PMID 12891360 . S2CID 3570549 .
- ↑ Lee TH, Kim SU, Yu SL, Kim SH, Park DS, Moon HB, Dho SH, Kwon KS, Kwon HJ, Han YH, Jeong S, Kang SW, Shin HS, Lee KK, Rhee SG, Yu DY (июнь 2003 г.). «Пероксиредоксин II необходим для поддержания продолжительности жизни эритроцитов у мышей» . Кровь . 101 (12): 5033–8. DOI : 10,1182 / кровь 2002-08-2548 . PMID 12586629 .
- ^ Dietz KJ, Jacob S, Oelze ML, Laxa M, Tognetti V, де Миранда SM, Байера M, Finkemeier I (2006). «Функция пероксиредоксинов в окислительно-восстановительном метаболизме органелл растений» . Журнал экспериментальной ботаники . 57 (8): 1697–709. DOI : 10.1093 / JXB / erj160 . PMID 16606633 .
- ^ Нордберг Дж, Arner Е.С. (декабрь 2001 г.). «Активные формы кислорода, антиоксиданты и тиоредоксиновая система млекопитающих». Свободная радикальная биология и медицина . 31 (11): 1287–312. DOI : 10.1016 / S0891-5849 (01) 00724-9 . PMID 11728801 .
- ^ Виейра Дос Сантос C, Rey P (июль 2006). «Тиоредоксины растений являются ключевыми участниками реакции на окислительный стресс». Тенденции в растениеводстве . 11 (7): 329–34. DOI : 10.1016 / j.tplants.2006.05.005 . PMID 16782394 .
- ^ Arner ES, Хольмгрен A (октябрь 2000). «Физиологические функции тиоредоксина и тиоредоксинредуктазы» . Европейский журнал биохимии / FEBS . 267 (20): 6102–9. DOI : 10.1046 / j.1432-1327.2000.01701.x . PMID 11012661 .
- ^ Mustacich D, Пауис G (февраль 2000). «Тиоредоксинредуктаза» . Биохимический журнал . 346 (1): 1–8. DOI : 10.1042 / 0264-6021: 3460001 . PMC 1220815 . PMID 10657232 .
- ^ Creissen G, Broadbent P, Stevens R, Wellburn AR, Mullineaux P (май 1996). «Манипуляция метаболизмом глутатиона в трансгенных растениях». Сделки Биохимического Общества . 24 (2): 465–9. DOI : 10,1042 / bst0240465 . PMID 8736785 .
- ^ Brigelius-Flohé R (ноябрь 1999). «Тканевые функции отдельных пероксидаз глутатиона». Свободная радикальная биология и медицина . 27 (9–10): 951–65. DOI : 10.1016 / S0891-5849 (99) 00173-2 . PMID 10569628 .
- ^ Хо Ю.С., Magnenat ДЛ, Бронсона РТ, Као - J, М Гаргано, Сугавара М., Funk компакт (июнь 1997). «Мыши с дефицитом клеточной глутатионпероксидазы развиваются нормально и не проявляют повышенной чувствительности к гипероксии» . Журнал биологической химии . 272 (26): 16644–51. DOI : 10.1074 / jbc.272.26.16644 . PMID 9195979 .
- ^ Де Хаан JB, Bladier C, P, Griffiths Kelner M, О'Ши RD, Cheung Н.С., Bronson РТ, Сильвестро МДж, Дикий S, Чжэн SS, Беар PM, Герцога PJ, Кольский I (август 1998 г.). «Мыши с гомозиготной нулевой мутацией по самой распространенной глутатионпероксидазе, Gpx1, демонстрируют повышенную чувствительность к параквату и перекиси водорода, вызывающим окислительный стресс» . Журнал биологической химии . 273 (35): 22528–36. DOI : 10.1074 / jbc.273.35.22528 . PMID 9712879 .
- ^ Sharma R, Yang Y, Sharma A, S Awasthi, Awasthi YC (апрель 2004). «Антиоксидантная роль глутатион-S-трансфераз: защита от токсичности оксидантов и регуляция стресс-опосредованного апоптоза». Антиоксиданты и редокс-сигналы . 6 (2): 289–300. DOI : 10.1089 / 152308604322899350 . PMID 15025930 .
- ^ Hayes JD, Фланеген JU, Jowsey ИК (2005). «Трансферазы глутатиона». Ежегодный обзор фармакологии и токсикологии . 45 : 51–88. DOI : 10.1146 / annurev.pharmtox.45.120403.095857 . PMID 15822171 .
- ^ Кадер AA, Zagory D, Кербелем EL (1989). «Упаковка фруктов и овощей в модифицированной атмосфере». Критические обзоры в области пищевой науки и питания . 28 (1): 1–30. DOI : 10.1080 / 10408398909527490 . PMID 2647417 .
- ^ Zallen Е.М., Хичкок MJ, Goertz GE (декабрь 1975). «Системы охлажденного питания. Влияние выдержки при охлаждении на качество говяжьего хлеба». Журнал Американской диетической ассоциации . 67 (6): 552–7. PMID 1184900 .
- ↑ Iverson F (июнь 1995 г.). «Фенольные антиоксиданты: исследования отделения здравоохранения по бутилированному гидроксианизолу». Письма о раке . 93 (1): 49–54. DOI : 10.1016 / 0304-3835 (95) 03787-W . PMID 7600543 .
- ^ "Индекс номера E" . Британский кулинарный гид. Архивировано 4 марта 2007 года . Проверено 5 марта 2007 года .
- ^ Robards K, Kerr AF, Patsalides E (февраль 1988). «Прогорклость и ее измерение в пищевых маслах и закусках. Обзор». Аналитик . 113 (2): 213–24. Bibcode : 1988Ana ... 113..213R . DOI : 10.1039 / an9881300213 . PMID 3288002 .
- ^ Del Carlo M, G Sacchetti, Ди Маттиа C, D Compagnone, Mastrocola D, L Liberatore, Cichelli A (июнь 2004). «Вклад фенольной фракции в антиоксидантную активность и окислительную стабильность оливкового масла». Журнал сельскохозяйственной и пищевой химии . 52 (13): 4072–9. DOI : 10.1021 / jf049806z . PMID 15212450 .
- ^ Boozer CE, GS Hammond, Hamilton CE, Сен JN (1955). «Окисление углеводородов воздухом.1II. Стехиометрия и судьба ингибиторов в бензоле и хлорбензоле». Журнал Американского химического общества . 77 (12): 3233–7. DOI : 10.1021 / ja01617a026 .
- ^ «Мировой рынок антиоксидантов (природных и синтетических) готов вырасти с 2,25 млрд долларов США в 2014 году до 3,25 млрд долларов США к 2020 году, при этом среднегодовой темп роста 5,5%» . GlobalNewswire, Эль-Сегундо, Калифорния. 19 января 2016 . Проверено 30 января 2017 года .
- ^ "Зачем использовать антиоксиданты?" . SpecialChem клеи. Архивировано из оригинального 11 февраля 2007 года . Проверено 27 февраля 2007 года .
- ^ a b «Топливные антиоксиданты» . Innospec Chemicals. Архивировано из оригинального 15 октября 2006 года . Проверено 27 февраля 2007 года .
- Перейти ↑ Rodriguez-Amaya DB (2003). «Пищевые каротиноиды: анализ, состав и изменения при хранении и переработке пищевых продуктов». Форум питания . 56 : 35–7. PMID 15806788 .
- ^ Maiani G, Castón MJ, Catasta G, Toti E, Cambrodón IG, Bysted A, Granado-Lorencio F, Olmedilla-Alonso B, Knuthsen P, Valoti M, Böhm V, Mayer-Miebach E, Behsnilian D, Schlemmer U (сентябрь 2009 г.). «Каротиноиды: актуальные знания об источниках пищи, потреблении, стабильности и биодоступности, а также их защитной роли в организме человека» . Молекулярное питание и пищевые исследования . 53 Дополнение 2: S194–218. DOI : 10.1002 / mnfr.200800053 . hdl : 10261/77697 . PMID 19035552 . Архивировано из оригинального 27 сентября 2018 года . Проверено 18 апреля 2017 года .
- ^ Генри CJ, Heppell N (февраль 2002). «Пищевые потери и выгоды во время обработки: будущие проблемы и проблемы» . Труды общества питания . 61 (1): 145–8. DOI : 10,1079 / PNS2001142 . PMID 12002789 .
- ^ «Антиоксиданты и профилактика рака: информационный бюллетень» . Национальный институт рака. Архивировано 4 марта 2007 года . Проверено 27 февраля 2007 года .
- ↑ Ortega R (декабрь 2006 г.). «Важность функциональных продуктов в средиземноморской диете» . Питание общественного здравоохранения . 9 (8A): 1136–40. DOI : 10.1017 / S1368980007668530 . PMID 17378953 .
- ^ WITSCHI А, Редди S, Stofer В, Лаутербург ВН (1992). «Системная доступность орального глутатиона». Европейский журнал клинической фармакологии . 43 (6): 667–9. DOI : 10.1007 / BF02284971 . PMID 1362956 . S2CID 27606314 .
- ↑ Flagg EW, Coates RJ, Eley JW, Jones DP, Gunter EW, Byers TE, Block GS, Greenberg RS (1994). «Диетическое потребление глутатиона людьми и взаимосвязь между потреблением и уровнем общего глутатиона в плазме». Питание и рак . 21 (1): 33–46. DOI : 10.1080 / 01635589409514302 . PMID 8183721 .
- ^ Додд S, декан O, Copolov DL, Malhi GS, Берк M (декабрь 2008). «N-ацетилцистеин для антиоксидантной терапии: фармакология и клиническое применение». Экспертное заключение по биологической терапии . 8 (12): 1955–62. DOI : 10.1517 / 14728220802517901 . PMID 18990082 . S2CID 74736842 .
- ^ Ван де Poll MC, Dejong CH, Soeters PB (июнь 2006 г.). «Адекватный диапазон серосодержащих аминокислот и биомаркеры их избытка: уроки энтерального и парентерального питания» . Журнал питания . 136 (6 доп.): 1694S – 1700S. DOI : 10.1093 / JN / 136.6.1694S . PMID 16702341 .
- Перейти ↑ Cao G, Alessio HM, Cutler RG (март 1993). «Анализ способности поглощать кислородные радикалы антиоксидантами» . Свободная радикальная биология и медицина . 14 (3): 303–11. DOI : 10.1016 / 0891-5849 (93) 90027-R . PMID 8458588 .
- ^ Ou B, Hampsch-Woodill М, До RL (октябрь 2001). «Разработка и проверка улучшенного анализа способности поглощения радикалов кислорода с использованием флуоресцеина в качестве флуоресцентного зонда». Журнал сельскохозяйственной и пищевой химии . 49 (10): 4619–26. DOI : 10.1021 / jf010586o . PMID 11599998 .
- ^ a b «Изъято: способность поглощать кислородные радикалы (ORAC) отобранных продуктов, выпуск 2 (2010)» . Министерство сельского хозяйства США, Служба сельскохозяйственных исследований. 16 мая 2012 . Проверено 13 июня 2012 года .
- ^ До RL, Wu X, Schaich K (май 2005). «Стандартизированные методы определения антиоксидантной способности и фенолов в пищевых продуктах и пищевых добавках» (PDF) . Журнал сельскохозяйственной и пищевой химии . 53 (10): 4290–302. DOI : 10.1021 / jf0502698 . PMID 15884874 . Архивировано из оригинального (PDF) 29 декабря 2016 года . Проверено 24 октября 2017 года .
- ^ Benzie IF (сентябрь 2003). «Эволюция диетических антиоксидантов». Сравнительная биохимия и физиология . 136 (1): 113–26. DOI : 10.1016 / S1095-6433 (02) 00368-9 . ЛВП : 10397/34754 . PMID 14527634 .
- ^ Мэттил HA (1947). «Антиоксиданты». Ежегодный обзор биохимии . 16 : 177–92. DOI : 10.1146 / annurev.bi.16.070147.001141 . PMID 20259061 .
- ^ Немецкий JB (1999). «Пищевая промышленность и окисление липидов». Влияние обработки на безопасность пищевых продуктов . Успехи экспериментальной медицины и биологии. 459 . С. 23–50. DOI : 10.1007 / 978-1-4615-4853-9_3 . ISBN 978-0-306-46051-7. PMID 10335367 .
- ^ Джейкоб Р.А. (1996). Три эр открытия витамина С . Субклеточная биохимия. 25 . С. 1–16. DOI : 10.1007 / 978-1-4613-0325-1_1 . ISBN 978-1-4613-7998-0. PMID 8821966 .
- Перейти ↑ Knight JA (1998). «Свободные радикалы: их история и текущее состояние при старении и болезнях». Летопись клинической и лабораторной науки . 28 (6): 331–46. PMID 9846200 .
- ^ Moureu С, Dufraisse С (1922). "Sur l'autoxydation: Les antioxygènes". Comptes Rendus des Séances et Mémoires de la Société de Biologie (на французском языке). 86 : 321–322.
- ↑ Wolf G (март 2005 г.). «Открытие антиоксидантной функции витамина Е: вклад Генри А. Маттилла» . Журнал питания . 135 (3): 363–6. DOI : 10.1093 / JN / 135.3.363 . PMID 15735064 .
Дальнейшее чтение [ править ]
- Холливелл, Барри. и Джон М.К. Гаттеридж, Свободные радикалы в биологии и медицине (Oxford University Press, 2007), ISBN 0-19-856869-X
- Лейн, Ник, Кислород: молекула, которая создала мир (Oxford University Press, 2003), ISBN 0-19-860783-0
- Покорный, Ян, Нелли Янислива и Майкл Х. Гордон, Антиоксиданты в продуктах питания: практическое применение (CRC Press, 2001), ISBN 0-8493-1222-1
Внешние ссылки [ править ]
- СМИ, связанные с антиоксидантами, на Викискладе?
![{\ displaystyle {\ ce {{\ underset {Oxygen} {O2}} -> {\ underset {Superoxide} {* O2 ^ {-}}} -> [{\ ce {Superoxide \ attop dismutase}}] {\ underset {Водород \ на перекиси} {H2O2}} -> [{\ ce {Peroxidases \ attop catalase}}] {\ underset {Water} {H2O}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8feecd26377be56b431d182ea9a398ab6b5d3b7f)