 | |
| Идентификаторы | |
|---|---|
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.013.764 |
| Номер ЕС |
|
| Номер E | E930 (глазури, ...) |
| 674257 | |
| КЕГГ | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1457 |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| CaO 2 | |
| Молярная масса | 72,0768 г / моль |
| Внешность | белый или желтоватый порошок |
| Запах | без запаха |
| Плотность | 2,91 г / см 3 |
| Температура плавления | ~ 355 ° С (671 ° F, 628 К) (разлагается) |
| разлагается | |
| Кислотность (p K a ) | 12,5 |
| -23,8 · 10 −6 см 3 / моль | |
Показатель преломления ( n D ) | 1,895 |
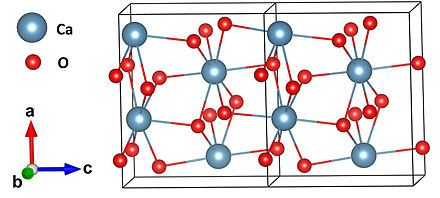
| Структура | |
| Орторомбический [1] | |
| Pna2 1 | |
| 8 [1] | |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Предупреждение |
Положения об опасности GHS | H272 , H315 , H319 , H335 |
Меры предосторожности GHS | Р210 , Р220 , P221 , P261 , P264 , P271 , P280 , P302 + 352 , Р304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P337 + 313 , P362 , P370 + 378 , P403 + 233 , P405 , P501 |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | > 5000 мг / кг (перорально, крысы) > 10000 мг / кг (кожные, крысы) |
| Родственные соединения | |
Другие анионы | Оксид кальция |
Другие катионы | Пероксид стронция Пероксид бария Пероксид натрия |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Пероксид кальция или диоксид кальция - это неорганическое соединение с формулой CaO 2 . Это пероксидная (O 2 2- ) соль Ca 2+ . Коммерческие образцы могут быть желтоватыми, но чистое соединение - белым. Практически не растворяется в воде . [2]
Структура и стабильность [ править ]
В твердом состоянии он относительно устойчив к разложению. Однако при контакте с водой он гидролизуется с выделением кислорода. При обработке кислотой образует перекись водорода .
Подготовка [ править ]
Перекись кальция получают путем объединения солей кальция и перекиси водорода :
- Са (ОН) 2 + Н 2 О 2 → СаО 2 + 2 Н 2 О
Октагидрат выпадает в осадок при реакции гидроксида кальция с разбавленной перекисью водорода . При нагревании он обезвоживается.
Приложения [ править ]
Он в основном используется в качестве окислителя для повышения извлечения драгоценных металлов из их руд. Во втором основном применении он используется как пищевая добавка под номером E E930, он используется в качестве отбеливающего и улучшающего агента для муки . [2]
В сельском хозяйстве используется для предпосевной обработки семян риса . Кроме того, пероксид кальция нашел применение в аквакультуре для насыщения кислородом и дезинфекции воды. В индустрии экологического восстановления используется для обработки почв. Перекись кальция используется аналогично перекиси магния в программах восстановления окружающей среды. Он используется для восстановления почвы и грунтовых вод, загрязненных нефтью, с помощью процесса усиленной биоремедиации на месте . Это второстепенный компонент некоторых средств для ухода за зубами.
Он также используется для отверждения полимеров на основе простого политиоэфира путем окисления концевых тиоловых групп до дисульфидных мостиков.
Ссылки [ править ]
- ^ а б Чжао, X .; Nguyen, MC; Ван, Чехия; Хо, К.М. (2013). «Структуры и стабильность пероксидов щелочноземельных металлов XO2 (X = Ca, Be, Mg) изучены с помощью генетического алгоритма» . RSC Advances . 3 (44): 22135. DOI : 10.1039 / C3RA43617A .
- ^ а б Харальд Якоб, Стефан Лейнингер, Томас Леманн, Сильвия Якоби, Свен Гутворт. «Пероксосоединения неорганические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a19_177.pub2 .CS1 maint: несколько имен: список авторов ( ссылка )