| Имена | |||
|---|---|---|---|
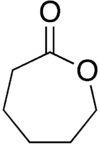
| Предпочтительное название IUPAC 2-оксепанон | |||
| Систематическое название ИЮПАК Гексано-6-лактон | |||
| Другие названия Капролактон ε-Капролактон Эпсилон-капролактон 6-Гексанолактон Гексан-6-олид 1-Окса-2-оксоциклогептан | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.007.217 | ||
| КЕГГ | |||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 6 Н 10 О 2 | |||
| Молярная масса | 114,14 г / моль | ||
| Плотность | 1,030 г / см 3 | ||
| Температура плавления | -1 ° С (30 ° F, 272 К) | ||
| Точка кипения | 241 ° С (466 ° F, 514 К) [2] | ||
| Смешиваемый [1] | |||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
ε-Капролактон или просто капролактон - это лактон (циклический сложный эфир ), имеющий семичленное кольцо. Его название происходит от капроновой кислоты . Эта бесцветная жидкость смешивается с большинством органических растворителей и водой. Когда-то он производился в больших масштабах как предшественник капролактама . [3]
Производство и использование [ править ]
Капролактон получают промышленным способом Байеру-Виллигеру из циклогексанона с надуксусной кислотой .
Капролактон - это мономер, используемый в производстве высокоспециализированных полимеров . Полимеризация с раскрытием кольца , например, дает поликапролактон . [3] Другой полимер - полиглекапрон , используемый в качестве шовного материала в хирургии. [4]
Реакции [ править ]
Хотя капролактон больше не был экономичным, его когда-то производили как предшественник капролактама. Капролактон обрабатывают аммиаком при повышенных температурах, чтобы получить лактам:
- (CH 2 ) 5 CO 2 + NH 3 → (CH 2 ) 5 C (O) NH + H 2 O
Карбонилирование капролактона дает после гидролиза пимелиновую кислоту . Лактоновое кольцо легко раскрывается нуклеофилами, включая спирты и воду, с образованием полилактонов и, в конечном итоге, 6-гидроксиадипиновой кислоты.
Родственные соединения [ править ]
Известно несколько других капролактонов. Эти изомеры включают α-, β-, γ- и δ-капролактоны. Все хиральны. ( R ) -γ-капролактон является компонентом цветочных ароматов и ароматов некоторых фруктов и овощей [5], а также вырабатывается жуком капра в виде феромона . [6] δ-капролактон содержится в нагретом молочном жире. [7]
Эфир капролактона используется в качестве связующего для ракетного топлива AP / AN / Al HTCE: эфир капролактона с концевыми гидроксильными группами [8]
Безопасность [ править ]
Капролактон быстро гидролизуется, и образующаяся гидроксикарбоновая кислота проявляет неисключительную токсичность, как и другие гидроксикарбоновые кислоты. [9] Известно, что он вызывает сильное раздражение глаз. Воздействие может привести к травме роговицы. [1]
Ссылки [ править ]
- ^ a b «Отчет о первоначальной оценке СВДС ε-капролактона» (PDF) . ОЭСР. Архивировано из оригинального (PDF) на 2011-08-15 . Проверено 12 октября 2017 .
- ^ "Технический паспорт продукта Capa Monomer" (PDF) . Perstorp. 2015-02-27. Архивировано из оригинального (PDF) 02.02.2017 . Проверено 11 октября 2017 .
- ^ а б Кёпник, Хорст; Шмидт, Манфред; Брюггинг, Вильгельм; Рютер, Йорн; Каминский, Уолтер (2002). «Полиэфиры». Энциклопедия промышленной химии Ульмана (6-е изд.). Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a21_227 .
- ^ "Сводный отчет сополимера гликолида E-капролактона" . CureHunter . Проверено 11 октября 2017 .
- ^ Мосандл, А .; Гюнтер, К. (1989). «Стереоизомерные ароматические соединения: структура и свойства гамма-лактонных энантиомеров». Журнал сельскохозяйственной и пищевой химии . 37 : 413–418. DOI : 10.1021 / jf00086a031 .
- ^ Нуньес, М. Тереза; Мартин, Виктор С. (1990). «Эффективное окисление фенильных групп до карбоновых кислот тетраоксидом рутения. Простой синтез (R) -гамма-капролактона, феромона Trogoderma granarium ». Журнал органической химии . 55 (6): 1928–1932. DOI : 10.1021 / jo00293a044 .
- ^ Парламент, Томас Х .; Nawar, Wassef W .; Фагерсон, Ирвинг С. (1965). «Дельта-капролактон в подогретом молочном жире» . Журнал молочной науки . 48 (5): 615–616. DOI : 10.3168 / jds.S0022-0302 (65) 88298-4 .
- ^ HTCE
- Перейти ↑ Miltenberger, Karlheinz (2002). «Гидроксикарбоновые кислоты алифатические». Энциклопедия промышленной химии Ульмана (6-е изд.). Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a13_507 .