 | |
 | |
| Имена | |
|---|---|
| Другие названия Диметилсульфат; Диметиловый эфир серной кислоты; Me 2 SO 4 ; ДМСО 4 ; Диметиловый эфир серной кислоты; Метилсульфат | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.000.963 |
| КЕГГ | |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| C 2 H 6 O 4 S | |
| Молярная масса | 126,13 г / моль |
| Появление | Бесцветная маслянистая жидкость |
| Запах | слабый, луковичный [1] |
| Плотность | 1,33 г / мл, жидкость |
| Температура плавления | -32 ° С (-26 ° F, 241 К) |
| Точка кипения | 188 ° С (370 ° F, 461 К) (разлагается) |
| Реагирует | |
| Растворимость | Метанол , дихлорметан , ацетон |
| Давление газа | 0,1 мм рт. Ст. (20 ° C) [1] |
| -62,2 · 10 −6 см 3 / моль | |
| Опасности | |
| Основные опасности | Чрезвычайно токсичен, опасность контакта, опасность вдыхания, коррозия, опасность для окружающей среды, канцерогенный, мутагенный |
| R-фразы (устаревшие) | R45 , R25 , R26 , R34 , R43 , R68 |
| S-фразы (устаревшие) | S53 , S45 , S30 , S60 , S61 |
| NFPA 704 (огненный алмаз) |  4 2 1 |
| точка возгорания | 83 ° С; 182 ° F; 356 К [1] |
| Смертельная доза или концентрация (LD, LC): | |
ЛК 50 ( средняя концентрация ) | 8,6 частей на миллион (крыса, 4 часа) 75 частей на миллион (морская свинка, 20 мин) 53 частей на миллион (мышь) 32 частей на миллион (морская свинка, 1 час) [2] |
LC Lo ( самый низкий опубликованный ) | 97 частей на миллион (человек, 10 мин) [2] |
| NIOSH (пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 1 ppm (5 мг / м 3 ) [кожа] [1] |
REL (рекомендуется) | Са TWA 0,1 ppm (0,5 мг / м 3 ) [кожа] [1] |
IDLH (Непосредственная опасность) | Ca [7 частей на миллион] [1] |
| Родственные соединения | |
Родственные соединения | Диэтилсульфат , метилтрифлат , диметилкарбонат |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
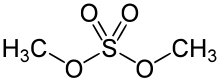
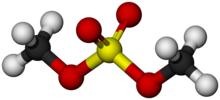
Диметилсульфат - это химическое соединение с формулой (CH 3 O) 2 SO 2 . В качестве диэфира из метанола и серной кислоты , его формула часто записывается в виде ( СН 3 ) 2 SO 4 или Me 2 SO 4 , где СН 3 или Ме метил . Me 2 SO 4 в основном используется в качестве метилирующего агента в органическом синтезе .
Me 2 SO 4 - это бесцветная маслянистая жидкость с легким запахом лука (хотя ее запах может свидетельствовать о значительном воздействии). Как и все сильные алкилирующие агенты , Me 2 SO 4 чрезвычайно токсичен . Его использование в качестве лабораторного реагента до некоторой степени было заменено метилтрифлатом CF 3 SO 3 CH 3 , метиловым эфиром трифторметансульфоновой кислоты .
История [ править ]
Диметилсульфат был обнаружен в начале 19 века в неочищенной форме. [3] П. Клаэссон позже подробно изучил его приготовление. [4] [5] Он использовался в химической войне в Первой мировой войне. [6] [7]
Производство [ править ]
Диметилсульфат могут быть синтезированы в лаборатории многими различными способами, [8] простейший быть этерификация серной кислоты с метанолом : [ разъяснение необходимости ]
- 2 СН 3 ОН + Н 2 SO 4 → (СН 3 ) 2 SO 4 + 2 Н 2 О
Другой возможный синтез включает дистилляцию метилгидросульфата: [5]
- 2 CH 3 HSO 4 → H 2 SO 4 + (CH 3 ) 2 SO 4
Метилнитрит и метилхлорсульфонат также приводят к диметилсульфату: [5]
- CH 3 ONO + (CH 3 ) OSO 2 Cl → (CH 3 ) 2 SO 4 + NOCl
Me 2 SO 4 коммерчески производится с 1920-х годов. Обычным процессом является непрерывная реакция диметилового эфира с триоксидом серы . [9]
- (СН 3 ) 2 О + SO 3 → (СН 3 ) 2 SO 4
Использует [ редактировать ]
Диметилсульфат является наиболее известным в качестве реагента для метилирования из фенолов , аминов и тиолов . Одна метильная группа передается быстрее, чем вторая. Предполагается, что перенос метила происходит посредством реакции S N 2. По сравнению с другими метилирующими агентами, промышленность предпочитает диметилсульфат из-за его низкой стоимости и высокой реакционной способности.
Метилирование кислородом [ править ]
Чаще всего Me 2 SO 4 используется для метилирования фенолов. Некоторые простые спирты также подходящим образом метилированы, как показано на примере превращения трет- бутанола в трет-бутилметиловый эфир :
- 2 (CH 3 ) 3 COH + (CH 3 O) 2 SO 2 → 2 (CH 3 ) 3 COCH 3 + H 2 SO 4
Соли алкоксидов быстро метилируются: [10]
- RO - Na + + (CH 3 O) 2 SO 2 → ROCH 3 + Na (CH 3 ) SO 4
Метилирование сахаров называется метилированием Хаворта . [11]
Метилирование аминным азотом [ править ]
Me 2 SO 4 используется для получения солей четвертичного аммония или третичных аминов :
- C 6 H 5 CH = NC 4 H 9 + (CH 3 O) 2 SO 2 → C 6 H 5 CH = N + (CH 3 ) C 4 H 9 + CH 3 OSO 3 -
Соединения четвертичного жирного аммония используются в качестве поверхностно-активного вещества или смягчителей тканей. Метилирование с образованием третичного амина проиллюстрировано следующим образом: [10]
- CH 3 (C 6 H 4 ) NH 2 + (CH 3 O) 2 SO 2 (в водном NaHCO 3 ) → CH 3 (C 6 H 4 ) N (CH 3 ) 2 + Na (CH 3 ) SO 4
Метилирование серы [ править ]
Подобно метилированию спиртов, соли меркаптида легко метилируются Me 2 SO 4 : [10]
- RS - Na + + (CH 3 O) 2 SO 2 → RSCH 3 + Na (CH 3 ) SO 4
Пример: [12]
- п-CH 3 C 6 H 4 SO 2 Na + (CH 3 O) 2 SO 2 → п-CH 3 C 6 H 4 SO 2 CH 3 + Na (CH 3 ) SO 4
Этот метод был использован для приготовления тиоэфиров:
- RC (O) SH + (CH 3 O) 2 SO 2 → RC (O) S (CH 3 ) + HOSO 3 CH 3
Реакции с нуклеиновыми кислотами [ править ]
Диметилсульфат (DMS) используется для определения вторичной структуры из РНК . При нейтральном pH DMS метилирует неспаренные остатки аденина и цитозина на их канонических лицевых сторонах Уотсона-Крика, но не может метилировать нуклеотиды, спаренные по основанию. Используя метод, известный как DMS-MaPseq , [13] РНК инкубируют с DMS для метилирования неспаренных оснований. Затем РНК подвергается обратной транскрипции; обратной транскриптазы часто добавляет неправильную базу ДНК , когда он сталкивается с денатурат РНК базы. Эти мутации могут быть обнаружены с помощью секвенирования , и предполагается, что РНК является одноцепочечной по основаниям с частотой мутаций выше фоновой.
Диметилсульфат может влиять на специфическое для оснований расщепление ДНК, воздействуя на имидазольные кольца, присутствующие в гуанине. [14] Диметилсульфат также метилирует аденин в одноцепочечных частях ДНК (например, в тех, где такие белки, как РНК-полимераза, постепенно плавятся и повторно отжигают ДНК). При повторном отжиге эти метильные группы мешают спариванию оснований аденин-гуанин. Затем нуклеазу S1 можно использовать для разрезания ДНК в одноцепочечных областях (в любом месте с метилированным аденином). Это важный метод анализа взаимодействий белок-ДНК.
Альтернативы [ править ]
Хотя диметилсульфат очень эффективен и доступен, его токсичность побудила использовать другие метилирующие реагенты. Метилиодид - это реагент, используемый для O-метилирования, как и диметилсульфат, но он менее опасен и более дорог. [12] Диметилкарбонат , который менее реакционноспособен, имеет гораздо более низкую токсичность по сравнению как с диметилсульфатом, так и с метилиодидом. [15] Высокое давление можно использовать для ускорения метилирования диметилкарбонатом. В целом токсичность метилирующих агентов коррелирует с их эффективностью в качестве реагентов для переноса метила.
Безопасность [ править ]
Диметилсульфат канцероген [9] и мутаген , очень ядовит , вызывает коррозию и опасен для окружающей среды . [16] Диметилсульфат всасывается через кожу, слизистые оболочки и желудочно-кишечный тракт и может вызвать замедленную реакцию дыхательных путей со смертельным исходом. Глазная реакция также обычна. Нет сильного запаха или немедленного раздражения, предупреждающих о смертельной концентрации в воздухе. ЛД50 (острый, перорально) составляет 205 мг / кг (крыса) и 140 мг / кг (мышь), и ЛК50 (острый) составляет 45 частей на миллион / 4 часа (крысы). [17] Давление пара 65 Па [18]достаточно велика, чтобы вызвать смертельную концентрацию в воздухе за счет испарения при 20 ° C. Отсроченная токсичность позволяет произойти потенциально смертельному воздействию до появления любых предупреждающих симптомов. [16] Симптомы могут проявляться через 6–24 часов. Концентрированные растворы оснований (аммиак, щелочи) можно использовать для гидролиза небольших разливов и остатков на загрязненном оборудовании, но реакция может стать бурной с большим количеством диметилсульфата (см. ICSC). Хотя соединение гидролизуется, нельзя предполагать, что обработка водой обеззараживает диметилсульфат.
Ссылки [ править ]
- ^ a b c d e f Карманный справочник NIOSH по химической опасности. «# 0229» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ a b «Диметилсульфат» . Немедленно опасная для жизни или здоровья концентрация (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Dumas, J .; Пелиго, Э. (1835). "Mémoire sur l'esprit de bois et sur les divers composés ethérés qui en proviennent" [Воспоминания о древесном спирте [то есть метаноле] и о различных эфирных соединениях, которые из него происходят]. Annales de Chimie et de Physique . 2-я серия (на французском языке). 58 : 5–74.
- ^ Клаэссон, Питер (1879). "Ueber die Neutralen und Sauren Sulfate des Methyl- und Aethylalkohols" [О нейтральных и кислых сульфатах метилового и этилового спирта]. Journal für praktische Chemie . 2-я серия (на немецком языке). 19 : 231–265. DOI : 10.1002 / prac.18790190123 .
- ^ a b c Suter, CM (1944). Органическая химия серы: соединения четырехвалентной серы . Джон Вили и сыновья. С. 49–53. LCCN 44001248 .
- ^ "Диметилсульфат 77-78-1" . EPA.
- ^ «Факты о ядах: низкое содержание химикатов: диметилсульфат» . Больница Канзасского университета.
- Перейти ↑ Shirley, DA (1966). Органическая химия . Холт, Райнхарт и Уинстон. п. 253. LCCN 64010030 .
- ^ a b "Диметилсульфат CAS № 77-78-1" (PDF) . 12-й отчет о канцерогенных веществах (RoC) . Министерство здравоохранения и социальных служб США . 2011 г.
- ^ a b c «Информация о продукте Dupont» . Архивировано из оригинала на 2008-11-19 . Проверено 8 мая 2006 .
- ^ WN Haworth (1915). «III. Новый метод получения алкилированных сахаров». Журнал Химического общества, Сделки . 107 : 8–16. DOI : 10.1039 / CT9150700008 .
- ^ a b Физер, LF; Физер, М. (1967). Реагенты для органического синтеза . Джон Вили и сыновья. п. 295 . ISBN 9780471258759.
- ^ Зубрадт, Меган; Гупта, Паромита; Персад, Ситара; Ламбовиц, Алан; Вайсман, Джонатан; Рускин, Сильви (2017). «DMS-MaPseq для полногеномного или целевого исследования структуры РНК in vivo» . Методы природы . 14 (1): 75–82. DOI : 10.1038 / nmeth.4057 . PMC 5508988 . PMID 27819661 .
- ^ Streitwieser, A .; Хиткок, Швейцария ; Kosower, EM (1992). Введение в органическую химию (4-е изд.). Макмиллан. п. 1169 . ISBN 978-0024181701.
- ^ Ши, WC; Dell, S .; Репик, О. (2001). «1,8-Диазабицикло [5.4.0] ундец-7-ен (DBU) и ускоренная микроволнами зеленая химия в метилировании фенолов, индолов и бензимидазолов диметилкарбонатом». Органические буквы . 3 (26): 4279–4281. DOI : 10.1021 / ol016949n . PMID 11784197 .
- ^ а б Риппи, JCR; Столлвуд, Мичиган (2005). «Девять случаев случайного воздействия диметилсульфата - потенциального химического оружия» . Журнал неотложной медицины . 22 (12): 878–879. DOI : 10.1136 / emj.2004.015800 . PMC 1726642 . PMID 16299199 .
- ^ "Паспорт безопасности материала - Диметилсульфат MSDS" . Научная лаборатория. Архивировано из оригинала на 2012-04-06 . Проверено 2 октября 2011 .
- ^ ICSC
Внешние ссылки [ править ]
- Страница веб-книги для C2H6SO4
- Международный химический