 | |
 | |
| Имена | |
|---|---|
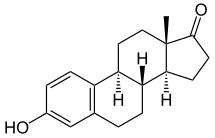
| Название ИЮПАК (8 R , 9 S , 13 S , 14 S ) -3-гидрокси-13-метил-7,8,9,11,12,14,15,16-октагидро- 6H -циклопента [ a ] фенантрен-17 -один | |
| Другие имена Эстрон; E1; 3-гидроксиэстра-1,3,5 (10) -триен-17-он | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.000.150 |
| КЕГГ | |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| С 18 Н 22 О 2 | |
| Молярная масса | 270,366 г / моль |
| Температура плавления | 254,5 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Эстрон ( E1 ), также называемый эстроном , является стероидом , слабым эстрогеном и второстепенным женским половым гормоном . [1] Это один из трех основных эндогенных эстрогенов, другие - эстрадиол и эстриол . [1] эстрона, а также другие эстрогены, которые синтезированы из холестерина и секретируется в основном из гонад , хотя они также могут быть образованы из надпочечниковых андрогенов в жировой ткани . [2]По сравнению с эстрадиолом и эстрон, и эстриол обладают гораздо более слабой активностью как эстрогены. [1] Эстрон может превращаться в эстрадиол и служит в основном в качестве предшественника или промежуточного звена метаболизма эстрадиола. [1] [3] Это предшественник и метаболит эстрадиола. [4] [1]
Помимо своей роли естественного гормона, эстрон использовался в качестве лекарства , например, в гормональной терапии менопаузы ; для получения информации об эстроне как лекарстве см. статью эстрон (лекарства) .
Биологическая активность [ править ]
Эстрон является эстроген, в частности , агонист из рецепторов эстрогена ERα и ERβ . [1] [5] Это гораздо менее мощный эстроген, чем эстрадиол, и поэтому он является относительно слабым эстрогеном. [1] [5] [6] При подкожном введении мышам эстрадиол примерно в 10 раз эффективнее эстрона и примерно в 100 раз сильнее эстриола . [7] Согласно одному исследованию, относительная аффинность связывания эстрона с человеческими ERα и ERβ составляла 4,0% и 3,5% от этих эстрадиолов, соответственно, иотносительные трансактивационные способности эстрона в ERα и ERβ составляли 2,6% и 4,3% от таковых у эстрадиола, соответственно. [5] Соответственно, эстрогенная активность эстрона, как сообщается, составляет примерно 4% от активности эстрадиола. [1] Помимо своей низкой эстрогенной активности, эстрон, в отличие от эстрадиола и эстриола, не накапливается в тканях-мишенях эстрогена. [1] Поскольку эстрон может превращаться в эстрадиол, большая часть или вся эстрогенная активность эстрона in vivo на самом деле связана с преобразованием в эстрадиол. [1] [8] Таким образом, эстрон считается предшественником или прогормоном эстрадиола.[3] В отличие от эстрадиола и эстриола, эстрон не является лигандом рецептора эстрогена, связанного с G-белком (сродство> 10 000 нМ). [9]
Клинические исследования подтвердили природу эстрона как относительно инертного предшественника эстрадиола. [1] [10] [11] [12] С перорального введения эстрадиола, соотношение уровней эстрадиола до уровней эстрона примерно в 5 раз выше , чем в среднем при нормальных физиологических условиях в пременопаузе женщин , а также с парентеральным (не пероральный) маршрутов эстрадиола. [1] Пероральное введение менопаузальных замещающих доз эстрадиола приводит к низким уровням эстрадиола в фолликулярной фазе , тогда как уровни эстрона напоминают высокие уровни, наблюдаемые во времяпервый триместр от беременности . [1] [13] [14] Несмотря на заметно повышенные уровни эстрона при пероральном приеме эстрадиола, но не при трансдермальном эстрадиоле, клинические исследования показали, что дозы перорального и трансдермального эстрадиола, позволяющие достичь схожих уровней эстрадиола, обладают эквивалентной и незначительно различающейся эффективностью. с точки зрения мер, включая подавление уровней лютеинизирующего гормона и фолликулостимулирующего гормона , ингибирование резорбции костей и облегчение симптомов менопаузы, таких как приливы . [1] [10] [11][12] [15] Кроме того, было обнаружено, что уровни эстрадиола коррелируют с этими эффектами, а уровни эстрона - нет. [10] [11] Эти данные подтверждают, что эстрон обладает очень низкой эстрогенной активностью, а также указывают на то, что эстрон не снижает эстрогенную активность эстрадиола. [1] [10] [11] [12] Это противоречит некоторым бесклеточной в пробирке исследования свидетельствуютчто высокие концентрации эстрона могли бы частично противодействуют действия эстрадиола. [16] [17] [18]
| Эстроген | ER RBA (%) | Масса матки (%) | Утеротрофия | Уровни ЛГ (%) | ГСПГ РБА (%) |
|---|---|---|---|---|---|
| Контроль | - | 100 | - | 100 | - |
| Эстрадиол | 100 | 506 ± 20 | +++ | 12–19 | 100 |
| Estrone | 11 ± 8 | 490 ± 22 | +++ | ? | 20 |
| Эстриол | 10 ± 4 | 468 ± 30 | +++ | 8–18 | 3 |
| Эстетрол | 0,5 ± 0,2 | ? | Неактивный | ? | 1 |
| 17α-эстрадиол | 4,2 ± 0,8 | ? | ? | ? | ? |
| 2-гидроксиэстрадиол | 24 ± 7 | 285 ± 8 | + b | 31–61 | 28 год |
| 2-метоксиэстрадиол | 0,05 ± 0,04 | 101 | Неактивный | ? | 130 |
| 4-гидроксиэстрадиол | 45 ± 12 | ? | ? | ? | ? |
| 4-метоксиэстрадиол | 1,3 ± 0,2 | 260 | ++ | ? | 9 |
| 4-фторэстрадиол а | 180 ± 43 | ? | +++ | ? | ? |
| 2-гидроксиэстрон | 1,9 ± 0,8 | 130 ± 9 | Неактивный | 110–142 | 8 |
| 2-метоксиэстрон | 0,01 ± 0,00 | 103 ± 7 | Неактивный | 95–100 | 120 |
| 4-гидроксиэстрон | 11 ± 4 | 351 | ++ | 21–50 | 35 год |
| 4-метоксиэстрон | 0,13 ± 0,04 | 338 | ++ | 65–92 | 12 |
| 16α-гидроксиэстрон | 2,8 ± 1,0 | 552 ± 42 | +++ | 7–24 | <0,5 |
| 2-гидроксиэстриол | 0,9 ± 0,3 | 302 | + b | ? | ? |
| 2-метоксиэстриол | 0,01 ± 0,00 | ? | Неактивный | ? | 4 |
| Примечания: значения являются средними ± стандартное отклонение или диапазон. ER RBA = относительное сродство связывания с рецепторами эстрогена цитозоля матки крысы . Масса матки = процентное изменение влажной массы матки крыс с удаленными яичниками через 72 часа при непрерывном введении 1 мкг / час с помощью подкожно имплантированных осмотических насосов . Уровни ЛГ = уровни лютеинизирующего гормона относительно исходного уровня у овариэктомированных крыс после 24-72 часов непрерывного введения через подкожный имплантат. Сноски: a = синтетический (т. Е. Не эндогенный ). b = Атипичный утеротрофический эффект, достигающий плато в течение 48 часов (утеротрофия эстрадиола линейно продолжается до 72 часов). Источники: см. Шаблон. | |||||
Биохимия [ править ]
Биосинтез [ править ]
Эстрон биосинтезируется из холестерина . Основной путь включает андростендион в качестве промежуточного продукта , при этом андростендион превращается в эстрон ферментом ароматазой . Эта реакция происходит как в гонадах, так и в некоторых других тканях , особенно в жировой ткани , и впоследствии из этих тканей секретируется эстрон . [2] Помимо ароматизации андростендиона, эстрон также обратимо образуется из эстрадиола ферментом 17β-гидроксистероиддегидрогеназой.(17β-HSD) в различных тканях, включая печень , матку и молочную железу . [1]
Распространение [ править ]
Эстрон связан примерно 16% до полового гормона-связывающего глобулина (SHBG) и 80% до альбумина в обращении , [1] с остатком ( от 2,0 до 4,0%) свободно или несвязанного циркулирующего. [20] Он имеет около 24% относительной аффинности связывания эстрадиола с SHBG. [1] Таким образом, эстрон относительно плохо связывается с SHBG. [21]
Метаболизм [ править ]
Эстрон является конъюгирует в эстроген конъюгат , такие как сульфат эстрона и эстрон глюкуронид по sulfotransferases и глюкуронидазам , а также может быть гидроксилированным с помощью цитохрома P450 ферментов в катехоле эстрогенов , таким как 2-гидроксиэстрон и 4-гидроксиэстрон или в эстриол . [1] Оба эти преобразования происходят преимущественно в печени . [1] Эстрон также может обратимо превращаться в эстрадиол с помощью 17β-HSD. [1]Период полувыведения эстрона из крови составляет от 10 до 70 минут и аналогичен периоду полувыведения эстрадиола. [22] [23]
Метаболические пути , из эстрадиола в организме человека |
Экскреция [ править ]
Эстрон выводится с мочой в виде конъюгатов эстрогена, таких как сульфат эстрона . [1] После внутривенной инъекции меченого эстрона женщинам почти 90% выводится с мочой и калом в течение 4–5 дней. [22] Энтерогепатическая рециркуляция вызывает задержку выведения эстрона. [22]
Уровни [ править ]
| Секс | Половой гормон | Репродуктивная фаза | Скорость производства крови | Скорость секреции гонад | Скорость метаболического клиренса | Референсный диапазон (уровни в сыворотке) | |
|---|---|---|---|---|---|---|---|
| Единицы СИ | Единицы, не относящиеся к системе СИ | ||||||
| Мужчины | Андростендион | - | 2,8 мг / день | 1,6 мг / день | 2200 л / сутки | 2,8-7,3 нмоль / л | 80–210 нг / дл |
| Тестостерон | - | 6,5 мг / день | 6,2 мг / день | 950 л / сутки | 6,9–34,7 нмоль / л | 200–1000 нг / дл | |
| Estrone | - | 150 мкг / день | 110 мкг / день | 2050 л / сутки | 37–250 пмоль / л | 10–70 пг / мл | |
| Эстрадиол | - | 60 мкг / день | 50 мкг / день | 1600 л / сутки | <37–210 пмоль / л | 10–57 пг / мл | |
| Эстрона сульфат | - | 80 мкг / день | Незначительный | 167 л / сутки | 600–2500 пмоль / л | 200–900 пг / мл | |
| Женщины | Андростендион | - | 3,2 мг / день | 2,8 мг / день | 2000 л / сутки | 3,1–12,2 нмоль / л | 89–350 нг / дл |
| Тестостерон | - | 190 мкг / день | 60 мкг / день | 500 л / сутки | 0,7–2,8 нмоль / л | 20–81 нг / дл | |
| Estrone | Фолликулярная фаза | 110 мкг / день | 80 мкг / день | 2200 л / сутки | 110–400 пмоль / л | 30–110 пг / мл | |
| Лютеиновой фазы | 260 мкг / день | 150 мкг / день | 2200 л / сутки | 310–660 пмоль / л | 80–180 пг / мл | ||
| Постменопауза | 40 мкг / день | Незначительный | 1610 л / сутки | 22–230 пмоль / л | 6–60 пг / мл | ||
| Эстрадиол | Фолликулярная фаза | 90 мкг / день | 80 мкг / день | 1200 л / сутки | <37–360 пмоль / л | 10–98 пг / мл | |
| Лютеиновой фазы | 250 мкг / день | 240 мкг / день | 1200 л / сутки | 699–1250 пмоль / л | 190–341 пг / мл | ||
| Постменопауза | 6 мкг / день | Незначительный | 910 л / сутки | <37–140 пмоль / л | 10–38 пг / мл | ||
| Эстрона сульфат | Фолликулярная фаза | 100 мкг / день | Незначительный | 146 л / сутки | 700–3600 пмоль / л | 250–1300 пг / мл | |
| Лютеиновой фазы | 180 мкг / день | Незначительный | 146 л / сутки | 1100–7300 пмоль / л | 400–2600 пг / мл | ||
| Прогестерон | Фолликулярная фаза | 2 мг / день | 1,7 мг / день | 2100 л / сутки | 0,3–3 нмоль / л | 0,1–0,9 нг / мл | |
| Лютеиновой фазы | 25 мг / день | 24 мг / день | 2100 л / сутки | 19–45 нмоль / л | 6–14 нг / мл | ||
Примечания и источники Примечания: « Концентрация стероида в кровотоке определяется скоростью, с которой он секретируется железами, скоростью метаболизма прекурсора или прегормонов в стероид и скоростью, с которой он извлекается тканями и метаболизируется. Скорость секреции стероида относится к общей секреции соединения из железы в единицу времени. Скорость секреции оценивалась путем отбора проб венозного стока из железы с течением времени и вычитания концентрации гормонов в артериальных и периферических венах. Скорость метаболического клиренса стероида определяется как объем крови , который был полностью очищен от гормона в единицу времени. в дебитстероидного гормона относится к поступлению в кровь соединения из всех возможных источников, включая секрецию желез и превращение прогормонов в интересующий стероид. В устойчивом состоянии количество гормона, поступающего в кровь из всех источников, будет равно скорости, с которой он очищается (скорость метаболического клиренса), умноженной на концентрацию в крови (скорость продуцирования = скорость метаболического клиренса × концентрация). Если метаболизм прогормонов вносит незначительный вклад в циркулирующий пул стероидов, то скорость продукции будет приблизительно соответствовать скорости секреции ». Источники: см. Шаблон. | |||||||
Химия [ править ]
Структуры основных эндогенных эстрогенов |
Эстрон, также известный как эстра-1,3,5 (10) -триен-3-ол-17-он, представляет собой природный стероид эстрана с двойными связями в положениях C1, C3 и C5, гидроксильной группой в положениях Положение C3 и кетонная группа в положении C17. Название эстрон был получен из химических терминов ESTR в (эстре-1,3,5 (10) -трийно) и кеты один .
Химическая формула эстрона представляет собой С 18 Н 22 О 2 и его молекулярная масса составляет 270,366 г / моль. Это белый твердый кристаллический порошок без запаха с температурой плавления 254,5 ° C (490 ° F) и удельным весом 1,23. [24] [25] Эстрон воспламеняется при высоких температурах, образуя оксид углерода (CO) и диоксид углерода (CO 2 ). [24]
Медицинское использование [ править ]
Эстрон был доступен в качестве впрыскиваемого эстрогена для использования в медицинских целях, например , в гормональной терапии для симптомов менопаузы , но это теперь уже в основном не продается. [26]
История [ править ]
Эстрон был первым открытым стероидным гормоном . [27] [28] Он был открыт в 1929 году независимо американскими учеными Эдвардом Дойзи и Эдгаром Алленом и немецким биохимиком Адольфом Бутенандтом , хотя Дойзи и Аллен выделили его за два месяца до Бутенандта. [27] [29] [30] Они выделяют и очищают эстрон в кристаллическом виде из мочи на беременных женщин. [29] [30] [31] Дойзи и Аллен назвали его theelin, в то время как Бутенандт назвал его прогиноном и впоследствии назвал его фолликулином в своей второй публикации по этому веществу. [30] [32] Позже Бутенандт был удостоен Нобелевской премии в 1939 году за выделение эстрона и его работы по половым гормонам в целом. [31] [33] Молекулярная формула эстрона была известна 1931, [34] и его химическая структура была определена с помощью Butenandt 1932. [30] [29] После выяснения его структуры, эстрон дополнительно упоминается как кетогидроксиэстрин илиoxohydroxyestrin , [35] [36] и имя эстрон , на основе его C17 кетона группы, были официально создан в 1932 году на первое заседании Международной конференции по стандартизации половых гормонов в Лондоне. [37] [38]
Частичный синтез эстрона из эргостерина был достигнут Рассел Earl Маркером в 1936 году, и был первым химическим синтезом эстрона. [39] [40] Альтернативный частичный синтез эстрона из холестерина с помощью дегидроэпиандростерона (ДГЭА) был разработан Гансом Херлоффом Инхоффеном и Вальтером Хольвегом в 1939 или 1940 годах [39], а полный синтез эстрона был достигнут Аннером и Мишером. в 1948 г. [38]
Ссылки [ править ]
- ^ a b c d e f g h i j k l m n o p q r s t u v Kuhl H (август 2005 г.). «Фармакология эстрогенов и прогестагенов: влияние различных путей введения» (PDF) . Климактерический . 8 Дополнение 1: 3–63. DOI : 10.1080 / 13697130500148875 . PMID 16112947 .
- ^ a b Хорнштейн Т., Шверин Дж. Л. (1 января 2012 г.). Биология женщины . Cengage Learning. С. 369–. ISBN 978-1-285-40102-7.
- ^ a b van Keep PA, Utian WH, Vermeulen A (6 декабря 2012 г.). Спорный климактерический период: доклады модераторов семинара, представленные на Третьем международном конгрессе по менопаузе, состоявшемся в Остенде, Бельгия, в июне 1981 г. под эгидой Международного общества менопаузы . Springer Science & Business Media. п. 92. ISBN 978-94-011-7253-0.
- ^ Chervenak J (октябрь 2009). «Биоидентичные гормоны для взрослеющих женщин». Maturitas . 64 (2): 86–9. DOI : 10.1016 / j.maturitas.2009.08.002 . PMID 19766414 .
- ^ a b c Escande A, Pillon A, Servant N, Cravedi JP, Larrea F, Muhn P, Nicolas JC, Cavaillès V, Balaguer P (май 2006 г.). «Оценка селективности лиганда с использованием линий репортерных клеток, стабильно экспрессирующих рецептор эстрогена альфа или бета». Биохимическая фармакология . 71 (10): 1459–69. DOI : 10.1016 / j.bcp.2006.02.002 . PMID 16554039 .
- ^ Руджеро RJ, Likis FE (2002). «Эстроген: физиология, фармакология и препараты для заместительной терапии». Журнал акушерства и женского здоровья . 47 (3): 130–8. DOI : 10.1016 / s1526-9523 (02) 00233-7 . PMID 12071379 .
- ^ A. Labhart (6 декабря 2012). Клиническая эндокринология: теория и практика . Springer Science & Business Media. С. 548–. ISBN 978-3-642-96158-8.
- ^ Фишман, Дж .; Мартуччи, CP (1980). «Новые концепции эстрогенной активности: роль метаболитов в выражении действия гормонов». У Н. Пасетто; Р. Паолетти; JL Амбрус (ред.). Менопауза и постменопауза . С. 43–52. DOI : 10.1007 / 978-94-011-7230-1_5 . ISBN 978-94-011-7232-5.
- ^ Prossnitz ER, Arterburn JB (июль 2015). "Международный союз фундаментальной и клинической фармакологии. XCVII. G-белковый рецептор эстрогена и его фармакологические модуляторы" . Pharmacol. Ред . 67 (3): 505–40. DOI : 10,1124 / pr.114.009712 . PMC 4485017 . PMID 26023144 .
- ^ a b c d Селби П., МакГарригл Х. Х., Павлин М. (март 1989 г.). «Сравнение эффектов перорального и трансдермального введения эстрадиола на метаболизм эстрогенов, синтез белка, высвобождение гонадотропина, метаболизм костей и климактерические симптомы у женщин в постменопаузе». Клиническая эндокринология . 30 (3): 241–9. DOI : 10.1111 / j.1365-2265.1989.tb02232.x . PMID 2512035 .
- ^ a b c d Powers MS, Schenkel L, Darley PE, Good WR, Balestra JC, Place VA (август 1985 г.). «Фармакокинетика и фармакодинамика трансдермальных лекарственных форм 17 бета-эстрадиола: сравнение с обычными пероральными эстрогенами, используемыми для заместительной гормональной терапии». Американский журнал акушерства и гинекологии . 152 (8): 1099–106. DOI : 10.1016 / 0002-9378 (85) 90569-1 . PMID 2992279 .
- ^ a b c Fåhraeus L, Larsson-Cohn U (декабрь 1982 г.). «Эстрогены, гонадотропины и SHBG при пероральном и кожном введении эстрадиола-17 бета женщинам в менопаузе». Acta Endocrinologica . 101 (4): 592–6. DOI : 10,1530 / acta.0.1010592 . PMID 6818806 .
- Перейти ↑ Wright JV (декабрь 2005 г.). «Биоидентичная замена стероидного гормона: избранные наблюдения из 23 лет клинической и лабораторной практики». Летопись Нью-Йоркской академии наук . 1057 (1): 506–24. Bibcode : 2005NYASA1057..506W . DOI : 10.1196 / annals.1356.039 . PMID 16399916 .
- Перейти ↑ Friel PN, Hinchcliffe C, Wright JV (март 2005 г.). «Замещение гормонов эстрадиолом: обычные пероральные дозы приводят к чрезмерному воздействию эстрона». Обзор альтернативной медицины . 10 (1): 36–41. PMID 15771561 .
- ^ De Lignieres B, Бадеван A, Thomas G, Thalabard JC, Мерсье-Bodard C, Conard J, Guyene TT, Майрон N, P Corvol, Гай-Гранд B (март 1986). «Биологические эффекты эстрадиола-17 бета у женщин в постменопаузе: пероральное или чрескожное введение». J. Clin. Эндокринол. Метаб . 62 (3): 536–41. DOI : 10,1210 / jcem-62-3-536 . PMID 3080464 .
- ^ Kloosterboer, HJ; Schoonen, WG; Верхёль, штат Джорджия (11 апреля 2008 г.). «Пролиферация клеток груди стероидными гормонами и их метаболитами» . В Паскуалини, Хорхе Р. (ред.). Рак груди: прогноз, лечение и профилактика . CRC Press. С. 343–366. ISBN 978-1-4200-5873-4.
- ^ Sasson S, Notides AC (июль 1983). «Взаимодействие эстриола и эстрона с рецептором эстрогена. II. Индуцированное эстриолом и эстроном ингибирование кооперативного связывания [3H] эстрадиола с рецептором эстрогена» . Журнал биологической химии . 258 (13): 8118–22. PMID 6863280 .
- ^ Lundström E, Conner P, Naessén S, Löfgren L, Carlström K, Söderqvist G (2015). «Эстрон - частичный антагонист эстрадиола в нормальной груди». Гинекологическая эндокринология . 31 (9): 747–9. DOI : 10.3109 / 09513590.2015.1062866 . PMID 26190536 .
- ^ Haggstrom МЫ, Ричфилд D (2014). «Схема путей стероидогенеза человека» . WikiJournal of Medicine . 1 (1). DOI : 10.15347 / wjm / 2014.005 . ISSN 2002-4436 .
- ^ Jameson JL, Де Гроот LJ (18 мая 2010). Эндокринология - электронная книга: взрослые и дети . Elsevier Health Sciences. С. 2813–. ISBN 978-1-4557-1126-0.
- ↑ HJ Buchsbaum (6 декабря 2012 г.). Менопауза . Springer Science & Business Media. С. 62, 64. ISBN 978-1-4612-5525-3.
- ^ a b c Дорфман, Ральф I. (1961). «Метаболизм стероидных гормонов»: 1223–1241. DOI : 10.1007 / 978-3-642-49761-2_39 . Цитировать журнал требует
|journal=( помощь ) - ^ Сандберг AA, Slaunwhite WR (август 1957). «Исследования фенольных стероидов на людях. II. Метаболическая судьба и гепато-билиарно-кишечная циркуляция C14-эстрона и C14-эстрадиола у женщин» . J. Clin. Инвестируйте . 36 (8): 1266–78. DOI : 10.1172 / JCI103524 . PMC 1072719 . PMID 13463090 .
- ^ a b "Паспорт безопасности материала Estrone" (PDF) . ScienceLab.com . Проверено 21 февраля 2013 года .
- ^ "Estrone -PubChem" . Национальный центр биотехнологической информации . Проверено 6 сентября 2009 года .
- ^ «Наркотики @ FDA: одобренные FDA лекарственные препараты» .
- ^ Б Верн Л. Bullough (19 мая 1995). Наука в спальне: история сексуальных исследований . Основные книги. С. 128–. ISBN 978-0-465-07259-0.
Когда Аллен и Дойзи услышали о [тесте Ашейма-Зондека для диагностики беременности], они поняли, что в моче есть богатый и легко обрабатываемый источник гормонов, из которого они могут получить мощный экстракт. [...] Исследование Аллена и Дойзи спонсировалось комитетом, в то время как исследование их главного конкурента Адольта Бутенандта (р. 1903) из Геттингенского университета спонсировалось немецкой фармацевтической фирмой. В 1929 году оба термина объявили о выделении чистого кристаллического женского полового гормона, эстрона, в 1929 году, хотя Дойзи и Аллен сделали это на два месяца раньше, чем Бутенандт27. К 1931 году эстрон коммерчески производился Парком Дэвисом в этой стране, и Шеринг-Кальбаум в Германии. Интересно, что когда Бутенандт (обладатель Нобелевской премии по химии в 1939 г.) выделил эстрон и проанализировал его структуру,он обнаружил, что это стероид, первый гормон, относящийся к этому молекулярному семейству.
- ^ Nielsch U, Фурманн U, Jaroch S (30 марта 2016). Новые подходы к открытию лекарств . Springer. С. 7–. ISBN 978-3-319-28914-4.
Первый стероидный гормон был выделен из мочи беременных женщин Адольфом Бутенандтом в 1929 году (эстрон; см. Рис. 1) (Butenandt 1931).
- ^ a b c Фриц Ф. Парл (2000). Эстрогены, рецепторы эстрогенов и рак груди . IOS Press. С. 4–5. ISBN 978-0-9673355-4-4.
[Дойзи] сосредоточил свое исследование на выделении женских половых гормонов из сотен галлонов мочи беременных людей, основываясь на открытии Ашеймом и Зондеком в 1927 году, что моча беременных женщин обладает эстрогенной активностью [9]. Летом 1929 года Дуази удалось изолировать эстрон (названный им theelin) одновременно с Адольфом Бутенандтом из Геттингенского университета в Германии, но независимо от него. Дуази представил свои результаты по кристаллизации эстрона на XIII Международном физиологическом конгрессе в Бостоне в августе 1929 г. [10].
- ^ a b c d Джеймс К. Лейлин (30 октября 1993 г.). Нобелевские лауреаты по химии, 1901–1992 . Фонд химического наследия. С. 255–. ISBN 978-0-8412-2690-6.
Адольт Фридрих Иоганн Бутенандт был удостоен Нобелевской премии по химии в 1939 году «за свои работы по половым гормонам»; [...] В 1929 году Бутенандт выделил эстрон [...] в чистой кристаллической форме. [...] И Бутенандт, и Эдвард Дойзи выделили эстрон одновременно, но независимо в 1929 году. [...] Бутенандт сделал большой шаг вперед в истории биохимии, когда выделил эстрон из мочи беременных женщин. [...] Он назвал его «прогинон» в своей первой публикации, а затем «фолликулин», [...] К 1932 году [...] он смог определить его химическую структуру, [...]
- ^ a b Артур Гринберг (14 мая 2014 г.). Химия: десятилетие за десятилетием . Издание информационной базы. С. 127–. ISBN 978-1-4381-0978-7.
Рациональные химические исследования половых гормонов человека начались в 1929 году, когда Адольф Бутенандт выделил чистый кристаллический эстрон, фолликулярный гормон, из мочи беременных женщин. [...] Бутенандт и Ружичка разделили Нобелевскую премию 1939 года по химии.
- ^ A. Labhart (6 декабря 2012). Клиническая эндокринология: теория и практика . Springer Science & Business Media. стр. 511–. ISBN 978-3-642-96158-8.
Э. Дойзи и А. Бутенандт почти одновременно сообщили о выделении эстроген-активного вещества в кристаллической форме из мочи беременных. Н.К. Адам предложил назвать это вещество эстроном из-за присутствия группы C-17-кетонов (1933).
- ↑ Том Рук (1 января 2012 г.). В поисках кортизона . Издательство МГУ. С. 54–. ISBN 978-1-60917-326-5.
В 1929 году Дойзи выделил и очистил первый эстроген, стероид под названием «эстрон»; Позже он получил Нобелевскую премию за эту работу.
- ^ Д. Линн Лорио (23 февраля 2016). Биографическая история эндокринологии . Вайли. С. 345–. ISBN 978-1-119-20247-9.
- ^ Кэмпбелл, AD (1933). «О плацентарных гормонах и нарушениях менструального цикла». Анналы внутренней медицины . 7 (3): 330. DOI : 10,7326 / 0003-4819-7-3-330 . ISSN 0003-4819 .
- ^ Fluhmann CF (ноябрь 1938). «Эстрогенные гормоны: их клиническое использование» . Калифорния и западная медицина . 49 (5): 362–6. PMC 1659459 . PMID 18744783 .
- ^ Fritz MA, Speroff L (28 марта 2012). Клиническая гинекологическая эндокринология и бесплодие . Липпинкотт Уильямс и Уилкинс. С. 750–. ISBN 978-1-4511-4847-3.
В 1926 году сэр Алан С. Паркс и К. У. Беллерби изобрели основное слово «эстрин» для обозначения гормона или гормонов, вызывающих течку у животных, время, когда самки млекопитающих плодовиты и восприимчивы к самцам. [...] Терминология была расширена за счет включения основных эстрогенов человека, эстрона, эстрадиола и эстриола, в 1932 году на первом заседании Международной конференции по стандартизации половых гормонов в Лондоне, [...]
- ^ a b Oettel M, Schillinger E (6 декабря 2012 г.). Эстрогены и антиэстрогены I: физиология и механизмы действия эстрогенов и антиэстрогенов . Springer Science & Business Media. С. 2–. ISBN 978-3-642-58616-3.
Структура эстрогенных гормонов была установлена Бутенандтом, Тайером, Маррианом и Хазлвудом в 1930 и 1931 годах (см. Butenandt 1980). Следуя предложению группы Марриан, эстрогенные гормоны получили тривиальные названия эстрадиол, эстрон и эстриол. На первом заседании Международной конференции по стандартизации половых гормонов в Лондоне (1932 г.) был разработан стандартный препарат эстрон. [...] Частичный синтез эстрадиола и эстрона из холестерина и дегидроэпиандростерона был осуществлен Инхоффеном и Хоулегом (Берлин, 1940); полный синтез был осуществлен Аннером и Мишером (Базель, 1948).
- ^ Б Элизабет Сигел Уоткинс (6 марта 2007). Эликсир эстрогена: история заместительной гормональной терапии в Америке . JHU Press. С. 21–. ISBN 978-0-8018-8602-7.
- ^ Грегори Пинкус; Тиманн Кеннет Вивиан Пинкус Грегори (2 декабря 2012 г.). Гормоны V1: физиология, химия и приложения . Эльзевир. С. 360–. ISBN 978-0-323-14206-9.

