| Имена | |||
|---|---|---|---|
| Имена ИЮПАК Гуанидин [1] Иминометандиамин | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| 506044 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100,003,656 | ||
| Номер ЕС |
| ||
| 100679 | |||
| MeSH | Гуанидин | ||
PubChem CID | |||
| UNII | |||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C H 5 N 3 | |||
| Молярная масса | 59,072 г · моль -1 | ||
| Температура плавления | 50 ° С (122 ° F, 323 К) | ||
| журнал P | −1,251 | ||
| Кислотность (p K a ) | 13,6 | ||
| Конъюгированная кислота | Гуанидиний | ||
| Термохимия | |||
Std энтальпия формации (Δ F H ⦵ 298 ) | −57 - −55 кДж моль −1 | ||
Стандартная энтальпия сгорания (Δ c H ⦵ 298 ) | −1.0511 - −1.0531 МДж моль −1 | ||
| Фармакология | |||
| Фармакокинетика : | |||
Биологический период полураспада | 7–8 часов | ||
| Опасности | |||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 475 мг / кг (перорально, крысы) [2] | ||
| Родственные соединения | |||
Родственные соединения |
| ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
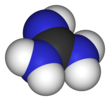
Гуанидин - это соединение формулы HNC (NH 2 ) 2 . Это бесцветное твердое вещество, растворяющееся в полярных растворителях. Это прочная основа, которая используется при производстве пластмасс и взрывчатых веществ . Он обнаруживается в моче как нормальный продукт метаболизма белков . Гуанидина фрагмент также появляется в больших органических молекул, в том числе и на боковой цепи аргинина .
Структура [ править ]
Гуанидин можно рассматривать как азотистый аналог угольной кислоты . То есть группа C = O в угольной кислоте заменяется группой C = NH, и каждый OH заменяется группой NH
2группа. [3] Изобутилен можно рассматривать как аналог углерода примерно таким же образом. Подробный кристаллографический анализ гуанидина был выяснен через 148 лет после его первого синтеза, несмотря на простоту молекулы. [4] В 2013 году положения атомов водорода и параметры их смещения были точно определены с помощью дифракции нейтронов на монокристалле. [5]
Производство [ править ]
Гуанидин может быть получен из природных источников, впервые он был выделен Адольфом Стрекером путем разложения гуанина . [6] Он был впервые синтезирован в 1861 году путем окислительного разложения ароматического природного продукта, гуанина , выделенного из перуанского гуано . [7]
Лабораторный метод получения гуанидина - щадящее (180-190 ° C) термическое разложение сухого тиоцианата аммония в безводных условиях:
Коммерческий путь включает двухстадийный процесс, начинающийся с реакции дициандиамида с солями аммония . Через посредство бигуанидин , это аммонолиз шаг дает соль катиона гуанидин (см ниже). На втором этапе соль обрабатывают основанием, например метоксидом натрия . [6]
Химия [ править ]
Катион гуанидиния [ править ]
При ap K b 0,4 гуанидин является сильным основанием. Большинство производных гуанидина фактически представляют собой соли, содержащие конъюгированную кислоту.
Сопряженная кислота называется гуанидина катион , ( C (NH
2)+
3). Этот плоский симметричный ион состоит из трех аминогрупп, каждая из которых связана с центральным атомом углерода ковалентной связью порядка 4/3. Это высокостабильный катион +1 в водном растворе благодаря эффективной резонансной стабилизации заряда и эффективной сольватации молекулами воды. В результате его p K a составляет 13,6 [8], что означает, что гуанидин является очень сильным основанием в воде; в нейтральной воде он существует почти исключительно в виде гуанидиния.
клюшка резонансный гибрид канонические формы
Тест на гуанидин [ править ]
Гуанидин может быть выборочно обнаружен с помощью натрий 1,2-нафтохинон-4-сульфоновой кислоты ( реагент Фолина ) и подкисленной мочевины. [9]
Использует [ редактировать ]
Промышленность [ править ]
Основной коммерческий интерес представляет собой нитрат [C ( NH
2) 3 ] НЕТ
3. Он используется в качестве топлива, например, в подушках безопасности .
Биохимия [ править ]
Гуанидин существует в протонированном виде, как гуанидин, в растворе при физиологическом pH.
Хлорид гуанидиния (также известный как гидрохлорид гуанидина) обладает хаотропными свойствами и используется для денатурирования белков. Хлорид гуанидиния, как известно, денатурирует белки с линейной зависимостью между концентрацией и свободной энергией разворачивания. В водных растворах, содержащих 6 М хлорида гуанидиния, почти все белки полностью теряют свою вторичную структуру и превращаются в случайно скрученные пептидные цепи. Тиоцианат гуанидиния также используется из-за его денатурирующего действия на различные биологические образцы.
Гуанидинийхлорид [10] используют в качестве адъюванта при лечении ботулизма , введенном в 1968, [11] , но теперь его роль считается спорной [12] - потому , что у некоторых пациентов не было никакого улучшения после введения этого препарата.
Другое [ править ]
Гидроксид гуанидиния является активным ингредиентом некоторых средств для расслабления волос, не содержащих щелок .
Производные гуанидина [ править ]
Гуанидины представляют собой группу органических соединений, имеющих общую функциональную группу с общей структурой (R
1р
2N) (R
3р
4N) C = N − R
5. Центральной связью в этой группе является имин , а группа структурно связана с амидинами и мочевинами. Примерами гуанидинов являются аргинин , триазабициклодецен , сакситоксин и креатин .
Галегин - это изоамиленгуанидин. [13]
См. Также [ править ]
- Категория: Гуанидины
- Тест Сакагути
- Y-ароматичность
- Амидин
Ссылки [ править ]
- ^ «Гуанидин - Резюме соединения» . PubChem Compound . США: Национальный центр биотехнологической информации. 16 сентября 2004 г. Опознание . Проверено 29 февраля 2012 года .
- ^ "Гуанидин гидрохлорид" . ChemIDplus . Национальная медицинская библиотека .
- ^ Goebel, M .; Клапоэтке, TM (2007). «Первая структурная характеристика гуанидина». Chem. Commun . 43 (30): 3180–2. DOI : 10.1039 / B705100J . PMID 17653381 .
- ^ Ямада, Т .; Лю, X .; Englert, U .; Yamane, H .; Дронсковски, Р. (2009). «Наконец-то достигнута твердотельная структура свободного основания гуанидина». Chem. Евро. Дж . 15 (23): 5651–5. DOI : 10.1002 / chem.200900508 . PMID 19388036 .
- ^ Савински, ПК; Meven, M .; Englert, U .; Дронсковски, Р. (2013). "Монокристаллическое нейтронографическое исследование гуанидина, CN 3 H 5 " . Cryst. Рост Des . 13 (4): 1730–5. DOI : 10.1021 / cg400054k .
- ^ a b Гютнер, Томас; Мерченк, Бернд; Шульц, Бернд. «Гуанидин и производные». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a12_545.pub2 .
- ^ Стрекер, А. (1861). "Untersuchungen über die chemischen Beziehungen zwischen Guanin, Xanthin, Theobromin, Caffeïn und Kreatinin" [Исследования химических отношений между гуанином, ксантином, теобромином, кофеином и креатинином]. Liebigs Ann. Chem . 118 (2): 151–177. DOI : 10.1002 / jlac.18611180203 .
- Перейти ↑ Perrin, DD (1972). Константы диссоциации органических оснований в водном растворе (Дополнение под ред.). Лондон: Баттервортс..
- ^ Салливан, MX (1935-10-01). «Колориметрический тест на гуанидин». Труды Общества экспериментальной биологии и медицины . 33 (1): 106–108. DOI : 10,3181 / 00379727-33-8270C . ISSN 0037-9727 . S2CID 88290359 .
- ^ Каплан, JE; Дэвис, LE; Нараян, В .; Koster, J .; Каценштейн, Д. (1979). «Ботулизм типа А и лечение гуанидином». Анналы неврологии . 6 (1): 69–71. DOI : 10.1002 / ana.410060117 . PMID 389150 . S2CID 42901888 .
- ^ Пуджиари, Марчелло; Черингтон, Майкл (1978). «Ботулизм и гуанидин: десять лет спустя». Варенье. Med. Доц . 240 (21): 2276–7. DOI : 10,1001 / jama.1978.03290210058027 . PMID 702753 .
- ^ Brook, Ицхак (2001). Детские анаэробные инфекции: диагностика и лечение (3-е изд.). Тейлор и Фрэнсис. п. 529. ISBN 0824741862.
- ^ Witters, Л. (2001). «Цветение французской сирени» . Журнал клинических исследований . 108 (8): 1105–7. DOI : 10.1172 / JCI14178 . PMC 209536 . PMID 11602616 .