 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Бромистый водород [ необходима цитата ] | |||
| Систематическое название ИЮПАК Броман [1] | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| 3587158 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.030.090 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
| MeSH | Бромистоводородная + кислота | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1048 | ||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| HBr | |||
| Молярная масса | 80,91 г / моль | ||
| Внешность | Бесцветный газ | ||
| Запах | Едкий | ||
| Плотность | 3,6452 кг / м 3 (0 ° C, 1013 мбар) [2] | ||
| Температура плавления | -86,9 ° С (-124,4 ° F, 186,2 К) | ||
| Точка кипения | -66,8 ° С (-88,2 ° F, 206,3 К) | ||
| 221 г / 100 мл (0 ° C) 204 г / 100 мл (15 ° C) 193 г / 100 мл (20 ° C) 130 г / 100 мл (100 ° C) | |||
| Растворимость | Растворим в спирте , органических растворителях | ||
| Давление газа | 2,308 МПа (при 21 ° C) | ||
| Кислотность (p K a ) | -8,8 (± 0,8); [3] ~ −9 [4] | ||
| Основность (p K b ) | ~ 23 | ||
| Конъюгированная кислота | Бромоний | ||
| Основание конъюгата | Бромид | ||
Показатель преломления ( n D ) | 1,325 [ необходима ссылка ] | ||
| Структура | |||
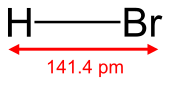
Молекулярная форма | Линейный | ||
Дипольный момент | 820 мД | ||
| Термохимия | |||
Теплоемкость ( C ) | 350,7 мДж / (К · г) | ||
Стандартная мольная энтропия ( S | 198,696–198,704 Дж / (К · моль) [5] | ||
Std энтальпия формации (Δ F H ⦵ 298 ) | −36,45 ...− 36,13 кДж / моль [5] | ||
| Опасности | |||
| Паспорт безопасности | hazar.com Physchem.ox.ac.uk | ||
| Пиктограммы GHS | |||
| Сигнальное слово GHS | Опасность | ||
Формулировки опасности GHS | H314 , H335 | ||
Меры предосторожности GHS | P261 , P280 , P305 + 351 + 338 , P310 | ||
| NFPA 704 (огненный алмаз) |  0 3 0 COR | ||
| Смертельная доза или концентрация (LD, LC): | |||
ЛК 50 ( средняя концентрация ) | 2858 частей на миллион (крыса, 1 час ) 814 частей на миллион (мышь, 1 час) [7] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 3 частей на миллион (10 мг / м 3 ) [6] | ||
REL (рекомендуется) | TWA 3 частей на миллион (10 мг / м 3 ) [6] | ||
IDLH (Непосредственная опасность) | 30 страниц в минуту [6] | ||
| Родственные соединения | |||
Родственные соединения | Фтористый водород Хлороводород Йодистый водород Астатид водорода | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Бромистый водород представляет собой гетероядерное двухатомное молекулярное соединение с формулой HBr, галогенид водорода, состоящий из водорода и брома. В чистом виде это бесцветный газ.
Бромистый водород хорошо растворяется в воде, образуя бромистоводородную кислоту , насыщенность которой составляет 68,85% HBr по массе при комнатной температуре. Водные растворы, которые содержат 47,6% HBr по массе, образуют постоянно кипящую азеотропную смесь, которая кипит при 124,3 ° C. При кипячении менее концентрированных растворов выделяется H 2 O до достижения состава смеси с постоянным кипением.
Как безводный, так и водный растворы HBr являются общими реагентами для получения бромидных соединений.
Использование HBr [ править ]
Бромистый водород и бромистоводородная кислота являются важными реагентами при производстве неорганических и органических соединений брома. [8] Свободно-радикальное присоединение HBr к алкенам дает алкилбромиды:
- RCH = CH 2 + HBr → R-CHBr-CH 3
Эти алкилирующие агенты являются предшественниками производных жирных аминов . Подобное присоединение свободных радикалов к аллилхлориду и стиролу дает 1-бром-3-хлорпропан и фенилэтилбромид соответственно.
Бромистый водород реагирует с дихлорметаном с образованием бромхлорметана и дибромметана , последовательно:
- HBr + CH 2 Cl 2 → HCl + CH 2 BrCl
- HBr + CH 2 BrCl → HCl + CH 2 Br 2
Аллилбромид получают обработкой аллилового спирта HBr:
- CH 2 = CHCH 2 OH + HBr → CH 2 = CHCH 2 Br + H 2 O
Другие реакции [ править ]
Хотя HBr не широко используется в промышленности, он добавляется к алкенам с образованием бромалканов, важного семейства броморганических соединений . Точно так же HBr присоединяется к галогеналкену с образованием геминального дигалогеналкана. (Этот тип сложения следует правилу Марковникова ):
- RC (Br) = CH 2 + HBr → RC (Br 2 ) -CH 3
HBr также присоединяется к алкинам с образованием бромалкенов. Стереохимия этого типа того, как правило , анти :
- RC≡CH + HBr → RC (Br) = CH 2
Также HBr используется для раскрытия эпоксидов и лактонов и в синтезе бромацеталей. Кроме того, HBr катализирует многие органические реакции. [9] [10] [11] [12]
Возможные приложения [ править ]
HBr был предложен для использования в проточных батареях для коммунальных предприятий. [13]
Промышленная подготовка [ править ]
Бромистый водород (вместе с бромистоводородной кислотой) получают путем объединения водорода и брома при температурах от 200 до 400 ° C. Реакция обычно катализируется платиной или асбестом . [10] [14]
Лабораторный синтез [ править ]
HBr можно синтезировать различными методами. Его можно приготовить в лаборатории путем дистилляции раствора бромида натрия или бромида калия с фосфорной или серной кислотой : [15]
- KBr + H 2 SO 4 → KHSO 4 + HBr
Концентрированная серная кислота менее эффективна, поскольку окисляет HBr до брома :
- 2 HBr + H 2 SO 4 → Br 2 + SO 2 + 2 H 2 O
Кислота может быть получена:
- реакция брома с водой и серой : [15]
- 2 Br 2 + S + 2 H 2 O → 4 HBr + SO 2
- бромирование тетралина : [15]
- C 10 H 12 + 4 Br 2 → C 10 H 8 Br 4 + 4 HBr
- восстановление брома фосфористой кислотой: [10]
- Br 2 + H 3 PO 3 + H 2 O → H 3 PO 4 + 2 HBr
Безводный бромистый водород также может быть получен в небольших масштабах термолизом трифенилфосфонийбромида в кипящем с обратным холодильником ксилоле . [9]
Бромистый водород, полученный указанными выше способами, может быть загрязнен Br 2 , который можно удалить, пропустив газ через раствор фенола при комнатной температуре в тетрахлорметане или другом подходящем растворителе (с получением 2,4,6-трибромфенола и образованием большего количества HBr в процесс) или через медную стружку или медную сетку при высокой температуре. [14]
Безопасность [ править ]
HBr вызывает сильную коррозию и раздражает при вдыхании.
Ссылки [ править ]
- ^ «Бромистоводородная кислота - Резюме соединений» . PubChem Compound . США: Национальный центр биотехнологической информации. 16 сентября 2004 г. Идентификационные и связанные записи . Проверено 10 ноября 2011 года .
- ^ Запись в базе данных веществ GESTIS Института безопасности и гигиены труда
- ^ Trummal, Александр; Липпинг, Лаури; Кальюранд, Ивари; Коппель, Ильмар А; Лейто, Иво (2016). «Кислотность сильных кислот в воде и диметилсульфоксиде». Журнал физической химии . 120 (20): 3663–9. Bibcode : 2016JPCA..120.3663T . DOI : 10.1021 / acs.jpca.6b02253 . PMID 27115918 .
- ^ Перрин, Д.Д. Константы диссоциации неорганических кислот и оснований в водном растворе. Баттервортс, Лондон, 1969 год.
- ^ a b Zumdahl, Стивен С. (2009). Химические принципы 6-е изд . Компания Houghton Mifflin. ISBN 978-0-618-94690-7.
- ^ a b c Карманный справочник NIOSH по химической опасности. «# 0331» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ «Бромоводород» . Немедленно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Дагани, MJ; Барда, HJ; Беня, TJ; Сандерс, округ Колумбия "Соединения брома". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a04_405 .CS1 maint: несколько имен: список авторов ( ссылка )
- ^ a b Hercouet, A .; ЛеКорре, М. (1988) Трифенилфосфония бромид: удобный и количественный источник газообразного бромистого водорода. Синтез, 157–158.
- ^ a b c Гринвуд, штат Нью-Йорк; Эрншоу, А. Химия элементов; Баттерворт-Хейнеман: Оксфорд, Великобритания; 1997; С. 809–812.
- ^ Carlin, William W. патент США 4147601 , 3 апреля 1979.
- ^ Воллхардт, КПК; Шор, Н. Е. Органическая химия: структура и функции; 4-е изд .; WH Freeman and Company: Нью-Йорк, штат Нью-Йорк; 2003 г.
- ^ https://www1.eere.energy.gov/hydrogenandfuelcells/pdfs/30535ag.pdf
- ^ а б Рухофф, младший; Бернетт, RE; Reid, EE " Органический синтез бромистого водорода (безводный)" , Vol. 15, стр. 35 (Сб. Т. 2, с. 338).
- ^ a b c М. Шмайссер «Хлор, бром, йод» в Справочнике по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, NY. Vol. 1. п. 282.
