 | |
 | |
| Имена | |
|---|---|
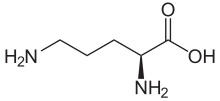
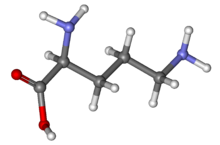
| Название ИЮПАК L- орнитин | |
| Другие названия (+) - ( S ) -2,5-Диаминовалериановая кислота (+) - ( S ) -2,5-Диаминопентановая кислота | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.665 |
| Номер ЕС |
|
| КЕГГ | |
| MeSH | Орнитин |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Свойства [1] | |
| C 5 H 12 N 2 O 2 | |
| Молярная масса | 132,16 г / моль |
| Температура плавления | 140 ° С (284 ° F, 413 К) |
| растворимый | |
| Растворимость | растворим в этаноле |
| Кислотность (p K a ) | 1,94 |
Хиральное вращение ([α] D ) | +11,5 (H 2 O, c = 6,5) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Орнитин - это непротеиногенная аминокислота, которая играет роль в цикле мочевины . Орнитин аномально накапливается в организме при дефиците орнитин-транскарбамилазы . Радикал является орнитил .
Роль в цикле мочевины [ править ]
Л -Ornithine является одним из продуктов действия фермента аргиназы на L - аргинин , создавая мочевины . Следовательно, орнитин является центральной частью цикла мочевины, что позволяет избавляться от избыточного азота . Орнитин перерабатывается и в некотором смысле является катализатором. Сначала аммиак превращается в карбамоилфосфат ( H
2NC (O) OPO2-
3). Орнитин превращается в производное мочевины по δ (концевому) азоту карбамоилфосфатсинтетазой. Другой азот добавляется из аспартата , образуя денитрогенизированный фумарат , и полученный аргинин ( соединение гуанидиния ) гидролизуется обратно до орнитина, образуя мочевину. Азот мочевины поступает из аммиака и аспартата, а азот в орнитине остается неизменным.
Орнитин - это не аминокислота, кодируемая ДНК , то есть не протеиногенная . Однако в непеченочных тканях млекопитающих цикл мочевины в основном используется в биосинтезе аргинина, поэтому в качестве промежуточного звена в метаболических процессах орнитин весьма важен. [2]
Другие реакции [ править ]
Орнитин под действием орнитиндекарбоксилазы (EC 4.1.1.17) является отправной точкой для синтеза полиаминов, таких как путресцин .
У бактерий, таких как E. coli , орнитин может быть синтезирован из L- глутамата . [3]
Исследование [ править ]
Усталость от упражнений [ править ]
Добавка L- орнитина уменьшала утомляемость субъектов в плацебо-контролируемом исследовании с использованием велоэргометра. Результаты показали, что L -орнитин обладает эффектом против утомления, повышая эффективность потребления энергии и способствуя выведению аммиака. [4] [5]
Дополнение по тяжелой атлетике [ править ]
Аминокислотные добавки, включая L -орнитин, часто продаются бодибилдерам и тяжелоатлетам с заявлениями о повышении уровня гормона роста человека (HGH), мышечной массы и силы. Короткое 4-дневное клиническое исследование 1993 г. показало, что комбинация L -орнитина с L- аргинином и L- лизином в дозе 2 г / сут каждый не увеличивала уровень гормона роста. [6] В обзоре 2002 года по теме был сделан вывод: «Использование определенных аминокислот для стимуляции высвобождения гормона роста спортсменами не рекомендуется». [7]
Цирроз [ править ]
L- орнитин L- аспартат (LOLA), стабильная соль орнитина и аспарагиновой кислоты, использовался для лечения цирроза печени . [8]
Ссылки [ править ]
- ^ Weast, Роберт С., изд. (1981). CRC Справочник по химии и физике (62-е изд.). Бока-Ратон, Флорида: CRC Press. п. С-408. ISBN 0-8493-0462-8.
- Перейти ↑ Weber AL, Miller SL (1981). «Причины появления двадцати кодированных аминокислот белка» (PDF) . Журнал молекулярной эволюции . 17 (5): 273–84. Bibcode : 1981JMolE..17..273W . DOI : 10.1007 / BF01795749 . PMID 7277510 . S2CID 27957755 .
- ^ «Биосинтез орнитина» . Школа биологических и химических наук Королевы Марии Лондонского университета. Архивировано из оригинала на 2012-04-14 . Проверено 17 августа 2007 . Цитировать журнал требует
|journal=( помощь ) - ^ Сугино Т, Т Ширай, Kajimoto Y, Kajimoto O (ноябрь 2008 г.). «Добавка L-орнитина снижает физическую усталость у здоровых добровольцев, регулируя метаболизм липидов и аминокислот». Исследования питания . 28 (11): 738–43. DOI : 10.1016 / j.nutres.2008.08.008 . PMID 19083482 .
- ^ Демура S, Ямада T, Yamaji S, M Komatsu, Моришита K (октябрь 2010). «Влияние приема внутрь гидрохлорида L-орнитина на производительность во время дополнительных исчерпывающих упражнений на велоэргометре и метаболизм аммиака во время и после тренировки» . Европейский журнал клинического питания . 64 (10): 1166–71. DOI : 10.1038 / ejcn.2010.149 . PMID 20717126 .
- ^ Fogelholm GM, Näveri HK, Kiilavuori KT, Härkönen MH (сентябрь 1993). «Добавки с низкими дозами аминокислот: не влияют на сывороточный гормон роста человека и инсулин у тяжелоатлетов-мужчин». Международный журнал спортивного питания . 3 (3): 290–7. DOI : 10.1123 / ijsn.3.3.290 . PMID 8220394 .
- ^ Chromiak JA, Антонио J (2002). «Использование спортсменами аминокислот в качестве высвобождающих гормон роста агентов». Питание . 18 (7–8): 657–61. DOI : 10.1016 / s0899-9007 (02) 00807-9 . PMID 12093449 .
- ^ Sikorska H, Cianciara J, Wiercińska-Drapało A (июнь 2010 г.). «[Физиологические функции L-орнитина и L-аспартата в организме и эффективность введения L-орнитин-L-аспартата в условиях относительного дефицита]» . Польски Меркуриуш Лекарски . 28 (168): 490–5. PMID 20642112 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме L-орнитина . |
- Масс-спектр орнитина