Тиоцианат ртути(II)
2_Xray.jpg/440px-Hg(SCN)2_Xray.jpg) | |
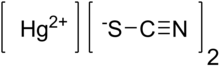 | |
| Имена | |
|---|---|
| Другие имена Тиоцианат ртути Сульфоцианат ртути | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| Информационная карта ECHA | 100.008.886 |
| Номер ЕС |
|
PubChem CID | |
| УНИИ | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| ртутного столба (SCN) 2 | |
| Молярная масса | 316,755 г/моль |
| вид | Белый моноклинный порошок |
| Запах | без запаха |
| Плотность | 3,71 г/см 3 , твердое |
| Температура плавления | 165 ° C (329 ° F, 438 K) (разлагается) |
| 0,069 г/100 мл | |
| Растворимость | Растворим в разбавленной соляной кислоте , KCN , аммиаке , слабо растворим в спирте , эфире |
| −96,5·10 −6 см 3 /моль | |
| Опасности | |
| Охрана труда и гигиена труда (OHS/OSH): | |
Основные опасности | высокотоксичный |
| Маркировка СГС : [1] | |
   | |
| Опасность | |
| Х300 , Х310 , Х330 , Х373 , Х410 | |
| P262 , P273 , P280 , P301+P310+P330 , P302+P352+P310 , P304+P340+P310 , P310 | |
| NFPA 704 (огненный алмаз) | |
| Смертельная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза ) | 46 мг/кг (крыса, перорально) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 °C [77 °F], 100 кПа). Ссылки на информационные ящики | |
Тиоцианат ртути(II) (Hg(SCN) 2 ) представляет собой неорганическое химическое соединение , координационный комплекс Hg 2+ и тиоцианат - аниона . Это белый порошок. При воспламенении он образует большую извилистую «змею» — эффект, известный как змей фараона . [2]
Синтез и структура
Первый синтез тиоцианата ртути, вероятно, был завершен в 1821 году Йонсом Якобом Берцелиусом :
- HgO + 2 HSCN → Hg(SCN) 2 + H 2 O
Доказательства существования первого чистого образца были представлены в 1866 году химиком по имени Отто Гермес. [2] Его получают обработкой растворов, содержащих ртуть(II) и тиоцианат-ионы. Продукт низкой растворимости тиоцианата ртути вызывает его осаждение из раствора. [3] Большинство синтезов достигается путем осаждения:
- Hg(NO 3 ) 2 + 2 KSCN → Hg(SCN) 2 + 2KNO 3
Соединение имеет полимерную структуру с центрами Hg 2+ , линейно координированными с двумя атомами S на расстоянии 2,381 Å. Четыре слабых взаимодействия Hg 2+ --N указаны с расстояниями 2,81 Å. [4]
Использование
Тиоцианат ртути имеет несколько применений в химическом синтезе. Он является предшественником трис(тиоцианато)меркурата(II) калия (K[Hg(SCN) 3 ]) и трис(тиоцианато)меркурата(II) цезия (Cs[Hg(SCN) 3 ]). Ион Hg(SCN) 3 - также может существовать независимо и легко образуется из вышеперечисленных соединений, среди прочих. [5]
Его реакции с органическими галогенидами дают два продукта: один с серой, связанной с органическим соединением, и один с азотом, связанным с органическим соединением. [6]
Использование в анализе хлоридов
Было обнаружено, что тиоцианат ртути может улучшить пределы обнаружения при определении хлорид-ионов в воде с помощью УФ-видимой спектроскопии . Этот метод был впервые предложен в 1952 году и с тех пор является распространенным методом определения ионов хлора в лабораториях по всему миру. В 1964 году была изобретена автоматизированная система, а затем в 1974 году компания Technicon ( Тэрритаун, штат Нью-Йорк , США) выпустила коммерческий анализатор цвета . Основной механизм включает добавление тиоцианата ртути к раствору с неизвестной концентрацией ионов хлора и железа в качестве реагента .. Ионы хлорида вызывают диссоциацию соли тиоцианата ртути, а ион тиоцианата связывает Fe (III), которое интенсивно поглощает при 450 нм. Это поглощение позволяет измерить концентрацию комплекса железа. Это значение позволяет рассчитать концентрацию хлорида. [7]
Его можно использовать для определения концентрации ионов хлора в водном растворе. Тиоцианат ртути без железа (III) добавляют к раствору с неизвестной концентрацией хлорид-ионов, образуя комплекс тиоцианата ртути и хлорид-иона, который поглощает свет при 254 нм, что позволяет проводить более точные измерения концентрации, чем вышеупомянутая методика с использованием утюг. [7]
Змей фараона
Тиоцианат ртути ранее использовался в пиротехнике, вызывая эффект, известный как змея фараона или змея фараона. Когда соединение находится в присутствии достаточно сильного источника тепла, начинается быстрая экзотермическая реакция , в результате которой образуется большая масса свертывающегося змеевидного твердого вещества. Незаметное пламя, часто голубое, но также может быть желтым/оранжевым, сопровождает горение. Полученное твердое вещество может иметь цвет от темно-графитово-серого до светло-коричневого, при этом внутренняя часть обычно намного темнее, чем внешняя. [2]
Реакция состоит из следующих нескольких стадий: [8] Воспламенение тиоцианата ртути приводит к образованию нерастворимой коричневой массы, состоящей в основном из нитрида углерода C 3 N 4 . Также образуются сульфид ртути и сероуглерод.
использованная литература
- ^ СГС: GESTIS 491027 (2016)
- ^ a b c Дэвис, Т.Л. (1940). «Пиротехнические змеи». Журнал химического образования . 17 (6): 268–270. дои : 10.1021/ed017p268 .
- ^ Sekine, T.; Ishii, T. (1970). "Studies of the Liquid-Liquid Partition systems. VIII. The Solvent Extraction of Mercury (II) Chloride, Bromide, Iodide and Thiocyanate with Some Organic Solvents". Bulletin of the Chemical Society of Japan. 43 (8): 2422–2429. doi:10.1246/bcsj.43.2422.
- ^ Beauchamp, A.L.; Goutier, D. "Structure cristalline et moleculaire du thiocyanate mercuric" Canadian Journal of Chemistry 1972, volume 50, p977-p981. doi:10.1139/v72-153
- ^ Боумейкер, Джорджия; Чураков, А.В.; Харрис, РК; Ховард, JAK; Апперли, округ Колумбия (1998). «Твердофазные исследования MAS ЯМР 199 Hg тиоцианатных комплексов ртути (II) и родственных соединений. Кристаллическая структура Hg (SeCN) 2 ». Неорганическая химия . 37 (8): 1734–1743. дои : 10.1021/ic9700112 .
- ^ Китамура, Т .; Кобаяши, С .; Танигучи, Х. (1990). «Фотолиз винилгалогенидов. Реакция фотогенерированных виниловых катионов с цианатными и тиоцианат-ионами». Журнал органической химии . 55 (6): 1801–1805. дои : 10.1021/jo00293a025 .
- ^ a b Cirello-Egamino, J .; Бриндл, ID (1995). «Определение ионов хлорида по реакции с тиоцианатом ртути в отсутствие железа (III) с использованием УФ-фотометрического метода проточной инжекции». Аналитик . 120 (1): 183–186. doi : 10.1039/AN9952000183 .
- ^ "Сделайте фейерверк Змеи Фараона" . Образование . Проверено 8 февраля 2016 г. .
внешние ссылки
- «Змея фараона» . Ютуб . 2 сентября 2008 г.
- «Как сделать Змея Фараона (Меркурий (II) Тиоцианат)» . Ютуб . 24 марта 2014 г.
- тиоцианаты
- Соединения ртути(II)
