 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Карбонат калия | |
| Другие имена Карбонат калия, карбонат калия дикалий, субкарбонат калия, зола жемчужная, калий, соль винного камня, соль полыни. | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.008.665 |
| Номер E | E501 (i) (регуляторы кислотности, ...) |
PubChem CID | |
| Номер RTECS |
|
| UNII |
|
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| K 2CO 3 | |
| Молярная масса | 138,205 г / моль |
| Внешность | Белое гигроскопичное твердое вещество |
| Плотность | 2,43 г / см 3 |
| Температура плавления | 891 ° С (1636 ° F, 1164 К) |
| Точка кипения | Разлагается |
| 110,3 г / 100 мл (20 ° C) 149,2 г / 100 мл (100 ° C) | |
| Растворимость | |
| −59,0 · 10 −6 см 3 / моль | |
| Опасности | |
| Паспорт безопасности | ICSC 1588 |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| H302 , H315 , H319 , H335 | |
Меры предосторожности GHS | P261 , P305 + 351 + 338 |
| NFPA 704 (огненный алмаз) |  0 1 0 |
| точка возгорания | Негорючий |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 1870 мг / кг (перорально, крыса) [1] |
| Родственные соединения | |
Другие анионы | Бикарбонат калия |
Другие катионы | Карбонат лития Карбонат натрия Карбонат рубидия Карбонат цезия |
Родственные соединения | Карбонат аммония |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
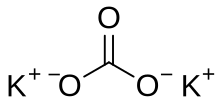
Карбонат калия - это неорганическое соединение с формулой K 2 CO 3 . Это белая соль , растворимая в воде . Он расплывается , часто выглядит как влажное или влажное твердое вещество . Карбонат калия в основном используется в производстве мыла и стекла . [2]
История [ править ]
Карбонат калия является основным компонентом поташа и более очищенной жемчужной золы или солей винного камня. Исторически сложилось так, что жемчужная зола была создана путем выпечки поташа в печи для удаления примесей. Оставшийся мелкий белый порошок был жемчужным пеплом. Первый патент, выданный Патентным ведомством США, был выдан Сэмюэлю Хопкинсу в 1790 году на улучшенный метод получения поташа и жемчужной золы.
В конце 18 века в Северной Америке , до изобретения разрыхлителя , жемчужная зола использовалась в качестве разрыхлителя для быстрого приготовления хлеба . [3] [4]
Производство [ править ]
Карбонат калия получают коммерчески реакцией гидроксида калия с диоксидом углерода : [2]
- 2 КОН + СО 2 → К 2 СО 3 + Н 2 О
Из раствора кристаллизуется полуторный К 2 СО 3 · 3 / 2 Н 2 О ( «калийный гидрат»). Нагревание этого твердого вещества выше 200 ° C дает безводную соль. В альтернативном методе хлорид калия обрабатывают диоксидом углерода в присутствии органического амина с получением бикарбоната калия , который затем кальцинируют:
- 2 KHCO 3 → K 2 CO 3 + H 2 O + CO 2
Приложения [ править ]
- (исторически) для мыла , стекла и фарфора производства
- в качестве мягкого сушильного агента, где другие сушильные агенты, такие как хлорид кальция и сульфат магния , могут быть несовместимы. Он не подходит для кислотных соединений, но может быть полезен для сушки органической фазы, если она имеет небольшое количество кислотных примесей. Его также можно использовать для сушки некоторых кетонов, спиртов и аминов перед перегонкой. [5]
- в кухне , где у него много традиционных применений. Это ингредиент для производства желе из травы , пищи, потребляемой в кухнях Китая и Юго-Восточной Азии, а также китайской лапши ручной работы и лунного пирога . Он также используется , чтобы смягчить рубец . В рецептах немецких имбирных пряников карбонат калия часто используется в качестве разрыхлителя, хотя и в сочетании с рожком . Использование карбоната калия должно быть ограничено определенным количеством, чтобы предотвратить вред, и не должно использоваться без руководства.
- при подщелачивании какао-порошка для производства шоколада голландского процесса путем уравновешивания pH (т.е. снижения кислотности) натуральных какао-бобов; он также усиливает аромат. Процесс добавления карбоната калия к какао-порошку обычно называют «голландским» (а продукты называются голландским какао-порошком), так как этот процесс был впервые разработан в 1828 году голландцем Коэнрадом Йоханнесом ван Хаутеном .
- как буферный агент при производстве медовухи или вина .
- в старинных документах сообщается, что его использовали для смягчения жесткой воды . [6]
- в качестве средства пожаротушения при тушении фритюрниц и различных других пожаров, связанных с классом B.
- в конденсированных аэрозолях пожаротушения , хотя и как побочный продукт нитрат калия.
- как ингредиент сварочных флюсов и флюсовых покрытий на стержнях для дуговой сварки.
- в качестве ингредиента корма для животных для удовлетворения потребности в калии сельскохозяйственных животных, например, производителей бройлеров.
- как регулятор кислотности в шведском снюсе
Ссылки [ править ]
- ^ Чемберс, Майкл. «ChemIDplus - 584-08-7 - BWHMMNNQKKPAPP-UHFFFAOYSA-L - Карбонат калия [USP] - Поиск похожих структур, синонимов, формул, ссылок на ресурсы и другой химической информации» . chem.sis.nlm.nih.gov . Архивировано 12 августа 2014 года.
- ^ a b Х. Шульц, Г. Бауэр, Э. Шахл, Ф. Хагедорн, П. Шмиттингер (2005). «Соединения калия». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a22_039 .CS1 maint: uses authors parameter (link)
- ^ См. Ссылки на «жемчужный пепел» в «Американской кулинарии» Амелии Симмонс, напечатанной Hudson & Goodwin, Hartford, 1796.
- ^ Civitello, Linda (2017). Войны разрыхлителей: жестокая борьба за еду, которая произвела революцию в кулинарии . Урбана, Иллинойс: Университет Иллинойса Press. С. 18–22. ISBN 9780252041082.
- ^ Леонард, Дж .; Lygo, B .; Проктер, Г. "Продвинутая практическая органическая химия" 1998, Stanley Thomas Publishers Ltd
- ^ Ребенок, Лидия М. "Американская экономная домохозяйка" 1832
Библиография [ править ]
- Научный словарь , Oxford University Press , Нью-Йорк , 2004 г.
- Ю. Платонов, Андрей; Евдокимов Андрей; Курзин Александр; Д. Майорова, Елена (29 июня 2002 г.). «Растворимость карбоната калия и гидрокарбоната калия в метаноле» . Журнал химических и технических данных . 47 (5): 1175–1176. DOI : 10.1021 / je020012v .
Внешние ссылки [ править ]
- Международная карта химической безопасности 1588