| |||
 | |||
| Имена | |||
|---|---|---|---|
| Другие имена Хлорат калия (VII); Хлорная кислота, калиевая соль; пероидин | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.011 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1489 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| KClO 4 | |||
| Молярная масса | 138,55 г / моль | ||
| Внешность | бесцветный / белый кристаллический порошок | ||
| Плотность | 2,5239 г / см 3 | ||
| Температура плавления | 610 ° C (1130 ° F; 883 K) разлагается от 400 ° C [4] [5] | ||
| 0,76 г / 100 мл (0 ° C) 1,5 г / 100 мл (25 ° C) [1] 4,76 г / 100 мл (40 ° C) 21,08 г / 100 мл (100 ° C) [2] | |||
Произведение растворимости ( K уд ) | 1,05 · 10 −2 [3] | ||
| Растворимость | незначительно в спирте нерастворим в эфире | ||
| Растворимость в этаноле | 47 мг / кг (0 ° C) 120 мг / кг (25 ° C) [2] | ||
| Растворимость в ацетоне | 1,6 г / кг [2] | ||
| Растворимость в этилацетате | 15 мг / кг [2] | ||
Показатель преломления ( n D ) | 1,4724 | ||
| Структура | |||
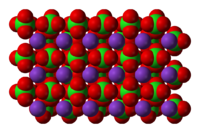
Кристальная структура | Ромбоэдрический | ||
| Термохимия | |||
Теплоемкость ( C ) | 111,35 Дж / моль · К [6] | ||
Стандартная мольная энтропия ( S | 150,86 Дж / моль · К [6] | ||
Std энтальпия формации (Δ F H ⦵ 298 ) | -433 кДж / моль [7] | ||
Свободная энергия Гиббса (Δ f G ˚) | -300,4 кДж / моль [2] | ||
| Опасности | |||
| Паспорт безопасности | Паспорт безопасности | ||
| Пиктограммы GHS | [5] | ||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H271 , H302 , H335 [5] | ||
Меры предосторожности GHS | P220 , P280 [5] | ||
| NFPA 704 (огненный алмаз) |  1 0 1 OX | ||
| Родственные соединения | |||
Другие анионы | Хлорид калия Хлорат калия Периодат калия | ||
Другие катионы | Перхлорат аммония Перхлорат натрия | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Перхлорат калия - это неорганическая соль с химической формулой K Cl O 4 . Как и другие перхлораты , эта соль является сильным окислителем, хотя обычно очень медленно реагирует с органическими веществами. Это, обычно получаемое в виде бесцветного кристаллического твердого вещества, является обычным окислителем, используемым в фейерверках , капсюлях боеприпасов , взрывных капсюлях и по-разному используется в порохах , составах вспышек , звездочках и бенгальских огнях . Он использовался как твердотопливная ракета.пропеллент, хотя в этом применении он в основном был заменен перхлоратом аммония с более высокими характеристиками . KClO 4 имеет самую низкую растворимость среди перхлоратов щелочных металлов (1,5 г в 100 мл воды при 25 ° C). [1]
Производство [ править ]
Калий перхлорат получает промышленно путем обработки водного раствора перхлората натрия с хлоридом калия . В этой единственной реакции осаждения используется низкая растворимость KClO 4 , которая составляет примерно 1/100 от растворимости NaClO 4 (209,6 г / 100 мл при 25 ° C). [8]
Он также может быть получен барботированием газообразного хлора через раствор хлората калия и гидроксида калия, [ ссылка необходима ] и реакцией хлорной кислоты с гидроксидом калия; однако это не используется широко из-за опасности хлорной кислоты.
Другой способ приготовления включает электролиз раствора хлората калия, в результате чего KClO 4 образуется и выпадает в осадок на аноде. Эта процедура осложняется низкой растворимостью как хлората калия, так и перхлората калия, последний из которых может осаждаться на электродах и препятствовать прохождению тока.
Окислительные свойства [ править ]
KClO 4 является окислителем в том смысле , что он переносит экзотермический кислород в горючие материалы, значительно увеличивая их скорость относительно сгорания , что в воздухе . Таким образом, с глюкозой дает углекислый газ:
- 3 KClO 4 + C 6 H 12 O 6 → 6 H 2 O + 6 CO 2 + 3 KCl
Превращение твердой глюкозы в горячий газообразный CO 2 лежит в основе взрывной силы этой и других подобных смесей. С сахаром KClO 4 образует слабое взрывчатое вещество при условии необходимого удержания. В противном случае такие смеси просто сгорают от яркого пурпурного пламени, характерного для калия . Вспышки, используемые в петардах, обычно состоят из смеси алюминиевого порошка и перхлората калия. Эта смесь, которую иногда называют вспышкой, также используется в наземных и воздушных фейерверках.
В качестве окислителя перхлорат калия можно безопасно использовать в присутствии серы , а хлорат калия - нет. Типична более высокая реакционная способность хлората - перхлораты кинетически более бедные окислители. Хлорат производит хлорноватую кислоту , которая очень нестабильна и может привести к преждевременному возгоранию композиции. Соответственно, хлорная кислота достаточно устойчива. [9]
При коммерческом использовании он смешивается в соотношении 50/50 с нитратом калия для создания заменителя черного пороха Pyrodex , и когда он не сжимается в дульном заряжании огнестрельного оружия или в патроне, горит с достаточно медленной скоростью, чтобы его нельзя было отнести к черному пороху как к пороху. от маловзрывоопасных до «легковоспламеняющихся».
Использование лекарств [ править ]
Перхлорат калия можно использовать в качестве антитиреоидного средства для лечения гипертиреоза , обычно в сочетании с одним другим лекарством. Это приложение использует одинаковый ионный радиус и гидрофильность перхлората и йодида .
Введение известных веществ, вызывающих гойтроген, также может быть использовано в качестве профилактики для снижения биопоглощения йода (будь то пищевой нерадиоактивный йод-127 или радиоактивный йод, радиоактивный йод - чаще всего йод-131 , поскольку организм не может различать разные изотопы йода ). Перхлорат- ионы, распространенные загрязняющие вещества в воде в США из-за аэрокосмической промышленности , снижают поглощение йода и, таким образом, классифицируются как зобогенные.. Ионы перхлората являются конкурентным ингибитором процесса, посредством которого йодид активно депонируется в фолликулярных клетках щитовидной железы. Исследования с участием здоровых взрослых добровольцев показали, что при уровнях выше 0,007 миллиграмма на килограмм в день (мг / (кг · сут)) перхлорат начинает временно подавлять способность щитовидной железы поглощать йод из кровотока («ингибирование поглощения йода», таким образом, перхлорат известный гойтроген). [10]Уменьшение пула йодидов перхлоратом имеет двойной эффект - уменьшение избыточного синтеза гормонов и гипертиреоза, с одной стороны, и снижение синтеза ингибиторов щитовидной железы и гипотиреоза, с другой. Перхлорат остается очень полезным в качестве однократной дозы в тестах, измеряющих выделение радиоактивного йода, накопленного в щитовидной железе в результате множества различных нарушений дальнейшего метаболизма йодида в щитовидной железе. [11]
Лечение тиреотоксикоза (включая болезнь Грейвса) 600–2000 мг перхлората калия (430–1400 мг перхлората) в день в течение нескольких месяцев или более когда-то было обычной практикой, особенно в Европе [10] [12], а применение перхлората в снижение доз для лечения проблем с триоидом продолжается и по сей день. [13] Хотя первоначально использовалось 400 мг перхлората калия, разделенное на четыре или пять дневных доз, и было обнаружено, что они эффективны, более высокие дозы были введены, когда было обнаружено, что 400 мг / сут не контролируют тиреотоксикоз у всех субъектов. [10] [11]
Текущие схемы лечения тиреотоксикоза (включая болезнь Грейвса), когда пациент подвергается воздействию дополнительных источников йода, обычно включают 500 мг перхлората калия два раза в день в течение 18-40 дней. [10] [14]
Было обнаружено, что профилактика перхлоратом, содержащим воду в концентрациях 17 ppm , что соответствует индивидуальному потреблению 0,5 мг / (кг в день), если человек весит 70 кг и потребляет 2 литра воды в день, снижает исходное поглощение радиоактивного йода на 67% [10 ] Это эквивалентно потреблению всего 35 мг ионов перхлората в день. В другом родственном исследовании испытуемые пили всего 1 литр перхлоратсодержащей воды в день в концентрации 10 ppm, т.е. ежедневно принималось 10 мг перхлорат-ионов, наблюдалось в среднем 38% снижение поглощения йода. [15]
Однако, когда среднее поглощение перхлората у рабочих перхлоратного завода, подвергшихся наибольшему воздействию, было оценено как приблизительно 0,5 мг / (кг в сутки), как в предыдущем абзаце, можно было бы ожидать снижения поглощения йода на 67%. Однако исследования рабочих, подвергающихся хроническому воздействию, до сих пор не выявили каких-либо нарушений функции щитовидной железы, включая поглощение йода. [16] это вполне может быть связано с достаточным ежедневным воздействием или потреблением здорового йода-127 среди рабочих и коротким 8-часовым биологическим периодом полураспада перхлората в организме. [10]
Следовательно, полностью блокировать поглощение йода-131 путем целенаправленного добавления перхлорат-ионов в водоснабжение населения, стремясь к дозировке 0,5 мг / (кг / сут) или концентрации воды 17 ppm, было бы совершенно недостаточно для истинного снижения поглощение радиоактивного йода. Концентрация перхлорат-иона в региональном водоснабжении должна быть намного выше, по крайней мере, 7,15 мг / кг веса тела в день или концентрация воды 250 ppm , при условии, что люди пьют 2 литра воды в день, чтобы быть действительно полезными для население в предотвращении биоаккумуляции при воздействии радиоактивного йода [10] [14] независимо от доступности йодата или йодидных препаратов.
Непрерывное распределение таблеток перхлората или добавление перхлората к водопроводу должно продолжаться не менее 80–90 дней, начиная сразу после обнаружения первоначального выброса радиоактивного йода, по прошествии 80–90 дней высвобожденного радиоактивного йода. 131 распался бы до менее чем 0,1% от своего первоначального количества, когда опасность биопоглощения йода-131 практически исчезла. [17]
Ссылки [ править ]
- ^ a b «Паспорт безопасности данных перхлората калия» . Дж . Т. Бейкер . 2007-02-16 . Проверено 10 декабря 2007 .
- ^ a b c d e "перхлорат калия" . chemister.ru . Проверено 14 апреля 2018 года .
- ^ "Константы произведения растворимости Ksp многих популярных солей в SolubilityOFthings" .
- ^ Бененсон, Уолтер; Штёкер, Хорст. Справочник по физике . Springer. п. 780 . ISBN 978-0387952697.
- ^ a b c d Sigma-Aldrich Co. , Перхлорат калия . Проверено 27 мая 2014.
- ^ a b Перхлорат калия в Linstrom, Peter J .; Маллард, Уильям Г. (ред.); Веб-книга NIST Chemistry, стандартная справочная база данных NIST номер 69 , Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд), http://webbook.nist.gov (получено 27 мая 2014 г.)
- ^ Zumdahl, Steven S. (2009). Химические принципы 6-е изд . Компания Houghton Mifflin. п. A22. ISBN 978-0-618-94690-7.
- ^ Helmut Vogt, Ян Балеж, Джон Э. Беннетт, Питер Wintzer, Саид Акбар Шейх, Патрицио Галлон «Хлор Оксиды и хлору Oxygen кислота» в энциклопедии Ульмана промышленной химии 2002, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a06_483
- ^ Гринвуд, штат Нью-Йорк; Эрншоу, А. (1997). Химия элементов (2-е изд.), Оксфорд: Баттерворт-Хайнеманн. ISBN 0-7506-3365-4 .
- ^ a b c d e f g Greer, Monte A .; Гудман, Гей; Pleus, Ричард С .; Грир, Сьюзан Э. (2002). «Оценка воздействия на здоровье загрязнения окружающей среды перхлоратами: реакция на дозу для ингибирования поглощения тироидного радиоактивного йода людьми» . Перспективы гигиены окружающей среды . 110 (9): 927–37. DOI : 10.1289 / ehp.02110927 . PMC 1240994 . PMID 12204829 .
- ^ а б Вольф, J (1998). «Перхлорат и щитовидная железа». Фармакологические обзоры . 50 (1): 89–105. PMID 9549759 .
- ^ Барзилай, D; Шейнфельд, М. (1966). «Смертельные осложнения после использования перхлората калия при тиреотоксикозе. Отчет о двух случаях и обзор литературы». Израильский журнал медицинских наук . 2 (4): 453–6. PMID 4290684 .
- ^ Woenckhaus, U .; Гирлич, К. (2005). "Терапия и профилактика гипертиреоза" [Терапия и профилактика гипертиреоза]. Der Internist (на немецком языке). 46 (12): 1318–23. DOI : 10.1007 / s00108-005-1508-4 . PMID 16231171 .
- ^ a b Bartalena, L .; Brogioni, S; Грассо, L; Bogazzi, F; Бурелли, А; Мартино, Э (1996). «Лечение тиреотоксикоза, вызванного амиодароном, сложная задача: результаты проспективного исследования». Журнал клинической эндокринологии и метаболизма . 81 (8): 2930–3. DOI : 10,1210 / jc.81.8.2930 . PMID 8768854 .
- ^ Лоуренс, JE; Ламм, Ш; Пино, С .; Richman, K .; Браверман, Л. Е. (2000). «Влияние кратковременных низких доз перхлората на различные аспекты функции щитовидной железы». Щитовидная железа . 10 (8): 659–63. DOI : 10.1089 / 10507250050137734 . PMID 11014310 .
- ^ Ламм, Стивен Х .; Braverman, Lewis E .; Ли, Фэн Сяо; Ричман, Кент; Пино, Сэм; Ховарт, Грегори (1999). «Состояние здоровья щитовидной железы рабочих, связанных с перхлоратом аммония: кросс-секционное исследование гигиены труда». Журнал профессиональной и экологической медицины . 41 (4): 248–60. DOI : 10.1097 / 00043764-199904000-00006 . PMID 10224590 .
- ^ «Ядерная химия: период полураспада и радиоактивное свидание - для чайников» . Dummies.com. 2010-01-06 . Проверено 21 января 2013 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме перхлората калия . |
- Страница веб-книги для KClO 4
| HClO 4 | Он | ||||||||||||||||
| LiClO 4 | Be (ClO 4 ) 2 | B (ClO4)- 4 В (ClO 4 ) 3 | ROClO 3 | N (ClO 4 ) 3 NH 4 ClO 4 NOClO 4 | О | FClO 4 | Ne | ||||||||||
| NaClO 4 | Mg (ClO 4 ) 2 | Al (ClO 4 ) 3 | Si | п | S | ClO- 4 ClOClO 3 Cl 2 O 7 | Ar | ||||||||||
| KClO 4 | Ca (ClO 4 ) 2 | Sc (ClO 4 ) 3 | Ti (ClO 4 ) 4 | VO (ClO 4 ) 3 VO 2 (ClO 4 ) | Cr (ClO 4 ) 3 | Mn (ClO 4 ) 2 | Fe (ClO 4 ) 3 | Co (ClO 4 ) 2 , Co (ClO 4 ) 3 | Ni (ClO 4 ) 2 | Cu (ClO 4 ) 2 | Zn (ClO 4 ) 2 | Ga (ClO 4 ) 3 | Ge | В качестве | Se | Br | Kr |
| RbClO 4 | Sr (ClO 4 ) 2 | Y (ClO 4 ) 3 | Zr (ClO 4 ) 4 | Nb (ClO 4 ) 5 | Пн | Tc | RU | Rh (ClO 4 ) 3 | Pd (ClO 4 ) 2 | AgClO 4 | Cd (ClO 4 ) 2 | В (ClO 4 ) 3 | Sn (ClO 4 ) 4 | Sb | TeO (ClO 4 ) 2 | я | Xe |
| CsClO 4 | Ba (ClO 4 ) 2 | Hf (ClO 4 ) 4 | Та (ClO 4 ) 5 | W | Re | Операционные системы | Ir | Pt | Au | Hg 2 (ClO 4 ) 2 , Hg (ClO 4 ) 2 | Tl (ClO 4 ) , Tl (ClO 4 ) 3 | Pb (ClO 4 ) 2 | Bi (ClO 4 ) 3 | По | В | Rn | |
| FrClO 4 | Ра | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Ур. | Ц | Og | |
| ↓ | |||||||||||||||||
| Ла | Ce (ClO 4 ) x | Pr | Nd | Вечера | Sm (ClO 4 ) 3 | Eu (ClO 4 ) 3 | Gd (ClO 4 ) 3 | Tb (ClO 4 ) 3 | Dy (ClO 4 ) 3 | Но (ClO 4 ) 3 | Er (ClO 4 ) 3 | Tm (ClO 4 ) 3 | Yb (ClO 4 ) 3 | Lu (ClO 4 ) 3 | |||
| Ac | Th (ClO 4 ) 4 | Па | UO 2 (ClO 4 ) 2 | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||