 | |
 | |
 | |
| Имена | |
|---|---|
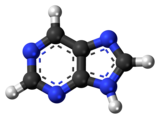
| Название ИЮПАК 9 H -пурин | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.004.020 |
| КЕГГ | |
| MeSH | Пурин |
PubChem CID | |
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| C 5 H 4 N 4 | |
| Молярная масса | 120,115 г · моль -1 |
| Температура плавления | 214 ° С (417 ° F, 487 К) |
| 500 г / л (RT) | |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Пурин - это гетероциклическое ароматическое органическое соединение , состоящее из двух колец. Растворим в воде. Пурин также дает свое имя более широкому классу молекул, пуринов , который включает замещенные пурины и их таутомеры . Они представляют собой наиболее распространенные азотсодержащие гетероциклы в природе. [1]
Пурины в высокой концентрации содержатся в мясе и мясных продуктах, особенно во внутренних органах, таких как печень и почки . В целом, рационы на основе растений содержат мало пуринов. [2] Примеры источников высокого пуриновых включают в себя: сладкое мясо , анчоусы , сардины , печень, говядина почки, мозги , мясные экстракты (например, Оксо , Bovril ), сельди , скумбрии , гребешки , мясо дичи , пиво (из дрожжей ) и соус. Некоторые бобовые, в том числе чечевица и черный горох , считаются растениями с высоким содержанием пуринов. Пища и добавки, содержащие спирулину, могут содержать исключительно пурины. [3]
Умеренное количество пурина также содержится в красном мясе, говядине , свинине , птице , рыбе и морепродуктах , спарже , цветной капусте , шпинате , грибах , зеленом горошке , чечевице , сушеном горохе, фасоли , овсянке , пшеничных отрубях , зародышах пшеницы и телятине . [4]
Пурины и пиримидины составляют две группы азотистых оснований , включая две группы нуклеотидных оснований . Основаниями пуриновых нуклеотидов являются гуанин (G) и аденин (A), которые различают соответствующие им дезоксирибонуклеотиды ( дезоксиаденозин и дезоксигуанозин ) и рибонуклеотиды ( аденозин , гуанозин ). Эти нуклеотиды являются двумя строительными блоками ДНК и РНК соответственно. Пуриновые основания также играют важную роль во многих метаболических и сигнальных процессах внутри соединений.гуанозинмонофосфат (GMP) и аденозинмонофосфат (AMP).
Для выполнения этих важных клеточных процессов клетке необходимы как пурины, так и пиримидины, причем в аналогичных количествах. Оба пуриновые и пиримидиновые являются само- ингибирующими и активирующие . Когда образуются пурины, они ингибируют те ферменты , необходимые для формирования дополнительных пуринов. Это самоингибирование происходит, поскольку они также активируют ферменты, необходимые для образования пиримидина. Пиримидин одновременно ингибирует и активирует пурин аналогичным образом. Из-за этого в клетке всегда находится примерно равное количество обоих веществ. [5]
Свойства [ править ]
Пурина является как очень слабая кислота ( рКа 8,93) и еще более слабым основанием ( рК 2,39). [6] При растворении в чистой воде pH будет находиться посередине между этими двумя значениями pKa.
Известные пурины [ править ]
Есть много пуринов природного происхождения. Они включают азотистые основания аденин ( 2 ) и гуанин ( 3 ). В ДНК эти основания образуют водородные связи со своими комплементарными пиримидинами , тимином и цитозином соответственно. Это называется дополнительным спариванием оснований. В РНК дополнением аденина является урацил вместо тимина.
Другие известные пурины - это гипоксантин , ксантин , теофиллин , теобромин , кофеин , мочевая кислота и изогуанин .
Функции [ править ]
Помимо важнейших ролей пуринов (аденин и гуанин) в ДНК и РНК, пурины также являются важными компонентами в ряде других важных биомолекул, таких как АТФ , ГТФ , цАМФ , NADH и коэнзима А . Сам пурин ( 1 ) не был обнаружен в природе, но его можно получить путем органического синтеза .
Они также могут действовать непосредственно как нейротрансмиттеры , воздействуя на пуринергические рецепторы . Аденозин активирует аденозиновые рецепторы .
История [ править ]
Слово пурин ( чистая моча ) [7] было придумано немецким химиком Эмилем Фишером в 1884 году. [8] [9] Он синтезировал его впервые в 1898 году. [9] Исходным материалом для последовательности реакций была мочевая кислота. ( 8 ), который был выделен из камней в почках по Шееле в 1776. [10] мочевой кислоты (8) подвергали взаимодействию с PCl 5 , чтобы дать 2,6,8-trichloropurine ( 10 ), который был преобразован в HI и PH 4I дать 2,6-дийодпурин ( 11 ). Продукт восстанавливали до пурина ( 1 ) с помощью цинковой пыли.
Метаболизм [ править ]
Многие организмы имеют метаболические пути синтеза и расщепления пуринов.
Пурины биологически синтезируются в виде нуклеозидов (оснований, прикрепленных к рибозе ).
Накопление модифицированных пуриновых нуклеотидов нарушает различные клеточные процессы, особенно те, которые связаны с ДНК и РНК . Чтобы быть жизнеспособными, организмы обладают рядом (дезокси) пуриновых фосфогидролаз, которые гидролизуют эти производные пурина, удаляя их из активных пулов NTP и dNTP . Дезаминирование пуриновых оснований может приводить к накоплению таких нуклеотидов, как ITP , dITP , XTP и dXTP . [11]
Дефекты ферментов, которые контролируют производство и распад пуринов, могут серьезно изменить последовательности ДНК клетки, что может объяснить, почему люди, которые несут определенные генетические варианты ферментов метаболизма пуринов, имеют более высокий риск развития некоторых типов рака .
Связь с подагрой [ править ]
Более высокий уровень потребления мяса и морепродуктов связан с повышенным риском подагры , тогда как более высокий уровень потребления молочных продуктов связан с меньшим риском. Умеренное потребление богатых пуринами овощей или белка не связано с повышенным риском подагры. [12] [13] Аналогичные результаты были получены в отношении риска гиперурикемии .
Лабораторный синтез [ править ]
Помимо синтеза пуринов in vivo при метаболизме пуринов, пурин также может быть создан искусственно.
Пурин ( 1 ) получается с хорошим выходом, если формамид нагревают в открытом сосуде при 170 ° C в течение 28 часов. [14]
Эта замечательная реакция и другие подобные ей обсуждались в контексте происхождения жизни . [15]
Запатентованный 20 августа 1968 года признанный в настоящее время метод промышленного производства аденина представляет собой модифицированную форму метода формамида. В этом методе формамид нагревается до 120 градусов Цельсия в закрытой колбе в течение 5 часов с образованием аденина. Количество реакции значительно усиливается при использовании оксихлорида фосфора (фосфорилхлорида) или пентахлорида фосфора в качестве кислотного катализатора и условий солнечного света или ультрафиолета. По прошествии 5 часов и охлаждения раствора формамид-фосфор оксихлорид-аденин в колбу наливают воду, содержащую формамид и образовавшийся аденин. Затем раствор вода-формамид-аденин пропускается через фильтровальную колонку с активированным углем. Молекулы воды и формамида, будучи небольшими молекулами, пройдут через древесный уголь в емкость для отходов;однако большие молекулы аденина будут прикрепляться или «адсорбироваться» на древесном угле из-за сил Ван-дер-Ваальса, которые взаимодействуют между аденином и углеродом в древесном угле. Поскольку древесный уголь имеет большую площадь поверхности, он способен захватывать большинство молекул, которые проходят через него определенного размера (больше, чем вода и формамид). Для извлечения аденина из аденина, адсорбированного углем, растворенный в воде газообразный аммиак (водный аммиак) выливают на структуру активированный уголь-аденин, чтобы высвободить аденин в водный раствор аммиака. Затем раствор, содержащий воду, аммиак и аденин, оставляют сушиться на воздухе, при этом аденин теряет растворимость из-за потери газообразного аммиака, который ранее сделал раствор основным и способным растворять аденин, что приводит к его кристаллизации в чистый белый порошок. которые можно хранить.[16]
Оро, Оргел и соавторы показали, что четыре молекулы HCN тетрамеризуются с образованием диаминомалеодинитрила ( 12 ), который может превращаться почти во все встречающиеся в природе пурины. [17] [18] [19] [20] [21] Например, пять молекул HCN конденсируются в экзотермической реакции с образованием аденина , особенно в присутствии аммиака.
Синтез пурина Трауба (1900) является классической реакцией (названной в честь Вильгельма Трауба ) между амином -замещенным пиримидином и муравьиной кислотой . [22]
См. Также [ править ]
- Пуриноны
- Пиримидин
- Простые ароматические кольца
- Переход
- Трансверсия
- Подагра , нарушение пуринового обмена
- Аденин
- Гуанин
Ссылки [ править ]
- ^ Rosemeyer, Helmut (март 2004). «Химическое разнообразие пурина как компонента натуральных продуктов». Химия и биоразнообразие . 1 (3): 361–401. DOI : 10.1002 / cbdv.200490033 . PMID 17191854 .
- ^ «Подагра: Список продуктов с высоким и низким содержанием пуринов» . Dietaryfiberfood.com . 2016-04-08 . Проверено 16 июля 2016 .
- ^ «Общее содержание пурина и пурина в общих пищевых продуктах» . 2014 г.
- ^ «Диета при подагре: каких продуктов следует избегать» . Healthcastle.com . Проверено 16 июля 2016 .
- ^ Гуйтон, Arthur C. (2006). Учебник медицинской физиологии . Филадельфия, Пенсильвания: Эльзевир. п. 37 . ISBN 978-0-7216-0240-0.
- ^ Ф. Сила; и другие. (2014). Эрнст Шауман (ред.). Houben-Weyl Methods of Organic Chemistry Vol. E 9b / 2, 4-е издание Дополнение: Hetarenes III (шестичленные кольца и большие гетерокольца с максимальной ненасыщенностью) - Часть 2b . п. 310. ISBN 9783131815040.
- ^ Макгиган, Хью (1921). Введение в химическую фармакологию . Сыновья П. Блэкистона и компания стр. 283 . Проверено 18 июля 2012 года .
- ^ Фишер, Эмиль (1884). "Ueber die Harnsäure. I." [О мочевой кислоте. Я.]. Berichte der Deutschen Chemischen Gesellschaft . 17 : 328–338. DOI : 10.1002 / cber.18840170196 .
С п. 329 : "Um eine rationelle Nomenklatur der so entstehenden zahlreichen Substanzen zu ermöglichen, betrachte ich dieselben als Abkömmlinge der noch unbekannten Wasserstoffverbindung CH 3 .C 5 N 4 H 3 and nenne die letpurin Methhl." (Чтобы создать рациональную номенклатуру для многочисленных существующих веществ, я рассматривал их как производные еще неизвестного соединения водорода, CH 3 .C 5 N 4 H 3 , и назвал последнее «метилпурин».) - ^ a b Фишер, Эмиль (1898). "Ueber das Purin und seine Methylderivate" [О пурине и его метильных производных]. Berichte der Deutschen Chemischen Gesellschaft . 31 (3): 2550–2574. DOI : 10.1002 / cber.18980310304 .
С п. 2550 : «… hielt ich es für zweckmäßig, all diese Produkte ebenso wie die Harnsäure als Derivate der sauerstofffreien Verbindung C 5 H 4 N 4 zu betrachten, und wählte für diese den Namen Purin, welcher auromb den wörum war». (… Я счел целесообразным рассматривать все эти продукты, как и мочевую кислоту, как производные бескислородного соединения C 5 H 4 N 4 , и выбрал для них название «пурин», которое образовалось от [ Latin] слова purum и uricum .) - ^ Шееле, CW (1776). «Examen chemicum calci urinari» [Химическое исследование камней в почках]. Opuscula . 2 : 73.
- ^ Дэвис, О .; Mendes, P .; Smallbone, K .; Малыс, Н. (2012). «Характеристика нескольких субстрат-специфичных (d) ITP / (d) XTPase и моделирование метаболизма дезаминированных пуриновых нуклеотидов» . BMB Reports . 45 (4): 259–264. DOI : 10.5483 / BMBRep.2012.45.4.259 . PMID 22531138 .
- ^ Чой, Хён К .; Аткинсон, Карен; Карлсон, Элизабет В .; Уиллетт, Уолтер; Курхан, Гэри (2004). «Продукты, богатые пуринами, потребление молочных продуктов и белков, и риск подагры у мужчин». Медицинский журнал Новой Англии . 350 (11): 1093–1103. DOI : 10.1056 / NEJMoa035700 . PMID 15014182 .
- ^ "Здоровье костей" . USDA . Проверено 17 июля 2016 .
- ^ Yamada, H .; Окамото, Т. (1972). «Одностадийный синтез пуринового кольца из формамида» . Химико-фармацевтический бюллетень . 20 (3): 623. DOI : 10,1248 / cpb.20.623 . Архивировано 16 мая 2016 года.
- ^ Саладино, Раффаэле; Крестини, Клаудиа; Чичириелло, Фабиана; Костанцо, Джованна; Мауро, Эрнесто; и другие. (2006). «О происхождении информационных полимеров на основе формамида: синтез азотистых оснований и благоприятные термодинамические ниши для ранних полимеров». Истоки жизни и эволюция биосфер . 36 (5–6): 523–531. Bibcode : 2006OLEB ... 36..523S . DOI : 10.1007 / s11084-006-9053-2 . PMID 17136429 .
- ^ [1] , "Процесс получения аденина", выпущенный 10 ноября 1966 г.
- ^ Санчес, РА; Феррис, JP; Оргель, Л. Е. (1967). «Исследования в области синтеза пребиотиков. II. Синтез предшественников пурина и аминокислот из водного цианистого водорода». Журнал молекулярной биологии . 30 (2): 223–253. DOI : 10.1016 / S0022-2836 (67) 80037-8 . PMID 4297187 .
- ^ Феррис, Джеймс П .; Оргель, Л. Е. (март 1966 г.). «Необычная фотохимическая перегруппировка при синтезе аденина из цианида водорода». Журнал Американского химического общества . 88 (5): 1074. DOI : 10.1021 / ja00957a050 .
- ^ Феррис, JP; Kuder, JE; Каталано, О. В. (1969). «Фотохимические реакции и химическая эволюция пуринов и производных никотинамида». Наука . 166 (3906): 765–766. Bibcode : 1969Sci ... 166..765F . DOI : 10.1126 / science.166.3906.765 . PMID 4241847 .
- ^ Оро, Дж .; Камат, JS (1961). «Синтез аминокислот из цианистого водорода в возможных условиях примитивной земли». Природа . 190 (4774): 442–443. Bibcode : 1961Natur.190..442O . DOI : 10.1038 / 190442a0 . PMID 13731262 .
- Перейти ↑ Bauer, Wolfgang (1985). Houben-Weyl Methods of Organic Chemistry Vol. E 5, 4-е издание Дополнение . Thieme Georg Verlag. п. 1547. ISBN 9783131811547.
- ^ Хасснер, Альфред; Штумер, К. (2002). Органический синтез на основе именных реакций (2-е изд.). Эльзевир. ISBN 0-08-043259-X.
Внешние ссылки [ править ]
- Содержание пурина в пище