 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC 3-хлорпроп-1-ен | |||
| Другие имена | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.144 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1100 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 3 H 5 Cl | |||
| Молярная масса | 76,52 г · моль -1 | ||
| Внешность | Бесцветная, коричневая, желтая или пурпурная жидкость [1] | ||
| Запах | острый, неприятный [1] | ||
| Плотность | 0,94 г / мл | ||
| Температура плавления | -135 ° С (-211 ° F, 138 К) | ||
| Точка кипения | 45 ° С (113 ° F, 318 К) | ||
| 0,36 г / 100 мл (20 ° С) | |||
| Растворимость | растворим в эфире , ацетоне , бензоле , хлороформе | ||
| Давление газа | 295 мм рт. Ст. [1] | ||
Показатель преломления ( n D ) | 1,4055 | ||
| Вязкость | 0,3130 мПа · с [2] | ||
| Опасности | |||
| Пиктограммы GHS | |||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H225 , H302 , H312 , H315 , H319 , H332 , H335 , H341 , H351 , H373 , H400 | ||
Меры предосторожности GHS | Р201 , Р202 , Р210 , Р233 , Р240 , Р241 , P242 , P243 , P260 , P261 , P264 , P270 , P271 , P273 , P280 , P281 , P301 + 312 , P302 + 352 , P303 + 361 + 353 , Р304 + 312 , P304 + 340 , P305 + 351 + 338 , P308 + 313 , P312 , P314 | ||
| NFPA 704 (огненный алмаз) |  3 3 1 | ||
| точка возгорания | -32 ° С (-26 ° F, 241 К) | ||
самовоспламенения температуру | 390 ° С (734 ° F, 663 К) | ||
| Пределы взрываемости | 2,9–11,2% | ||
| Смертельная доза или концентрация (LD, LC): | |||
ЛК 50 ( средняя концентрация ) | 11000 мг / м 3 (крыса, 2 часа) 11500 мг / м 3 (мышь, 2 часа) 5800 мг / м 3 (морская свинка, 2 часа) 22500 мг / м 3 (кролик, 2 часа) 10500 мг / м 3 (кот, 2 ч.) [3] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 1 ppm (3 мг / м 3 ) [1] | ||
REL (рекомендуется) | TWA 1 ppm (3 мг / м 3 ) ST 2 ppm (6 мг / м 3 ) [1] | ||
IDLH (Непосредственная опасность) | 250 страниц на миллион [1] | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
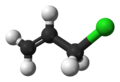
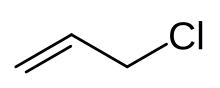
Аллил хлорид представляет собой органическое соединение с формулой C H 2 = СНСН 2 Cl . Эта бесцветная жидкость не растворяется в воде, но растворяется в обычных органических растворителях. В основном он превращается в эпихлоргидрин , используемый в производстве пластмасс. Это хлорированное производное пропилена . Это алкилирующий агент , который делает его полезным и опасным в обращении. [4]
Производство [ править ]
Лабораторные весы [ править ]
Аллилхлорид был впервые произведен в 1857 году Огюстом Кауром и Августом Хофманном путем взаимодействия аллилового спирта с треххлористым фосфором . [5] [4] Современные протоколы приготовления экономят этот подход, заменяя относительно дорогой трихлорид фосфора соляной кислотой и катализатором, таким как хлорид меди (I) . [6]
Промышленный масштаб [ править ]
Аллилхлорида получают путем хлорирования из пропилена . При более низких температурах основным продуктом является 1,2-дихлорпропан , но при 500 ° C преобладает аллилхлорид, образующийся в результате свободнорадикальной реакции:
- CH 3 CH = CH 2 + Cl 2 → ClCH 2 CH = CH 2 + HCl
Примерно 800 000 метрических тонн было произведено таким образом в 1997 году. [4]
Реакции и использование [ править ]
Подавляющее большинство аллилхлорида превращается в эпихлоргидрин . [4] Другие коммерчески значимые производные включают аллиловый спирт , аллиламин , аллилизотиоцианат (синтетическое горчичное масло), [7] и 1-бром-3-хлорпропан .
В качестве алкилирующего агента он используется в производстве фармацевтических препаратов и пестицидов , таких как горчичное масло.
Иллюстративные реакции [ править ]
Примерами его реакционной способности является цианирование с аллилового цианида (СН 2 = СНСН 2 CN). [8] Будучи реакционноспособным алкилгалогенидом, он подвергается восстановительному взаимодействию с образованием диаллила : [9]
- 2 ClCH 2 CH = CH 2 + Mg → (CH 2 ) 2 (CH = CH 2 ) 2 + MgCl 2
Он подвергается окислительному присоединению к палладию (0) с образованием димера хлорида аллилпалладия , (C 3 H 5 ) 2 Pd 2 Cl 2 . Дегидрогалогенирование дает циклопропен .
Безопасность [ править ]
Аллилхлорид очень токсичен и легко воспламеняется . Воздействие на глаза может быть отложенным и может привести к возможному ухудшению зрения. [10]
См. Также [ править ]
- Аллил
- Бромистый аллил
- Аллил йодид
Внешние ссылки [ править ]
- Международная карта химической безопасности 0010
- Карманный справочник NIOSH по химической опасности. «# 0018» . Национальный институт охраны труда и здоровья (NIOSH).
- Монография МАИР * Аллилхлорид.
Ссылки [ править ]
- ^ a b c d e f g h Карманное руководство NIOSH по химическим опасностям. «# 0018» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Вишванат, DS; Натараджан, Г. (1989). Сборник данных по вязкости жидкостей . Издательство Hemisphere Publishing Corporation. ISBN 0-89116-778-1.
- ^ "Аллилхлорид" . Немедленно опасная для жизни или здоровья концентрация (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ a b c d Людгер Крэлинг, Юрген Крей, Джеральд Якобсон, Иоганн Гролиг, Леопольд Микше «Аллильные соединения» в Энциклопедии промышленной химии Ульманна Wiley-VCH, Вайнхайм, 2005. Опубликовано онлайн: 15 июня 2000 г.
- ^ Хофманн. Август Уильям и Каур. Август (1857) «Исследования нового класса спиртов», « Философские труды Лондонского королевского общества» , 147 : 555–574; см. стр. 558–559.
- ^ Фернисс, Брайан; Ханнафорд, Энтони; Смит, Питер; Татчелл, Остин (1996). Учебник практической органической химии Фогеля (5-е изд.). Лондон: Longman Science & Technical. С. 558 . ISBN 9780582462366.
- ^ Ф. Романовски, Х. Кленк «Тиоцианаты и изотиоцианаты, органические» в Энциклопедии промышленной химии Ульмана, 2005, Wiley-VCH: Weinheim. DOI : 10.1002 / 14356007.a26_749
- ^ СП Supniewski & PL Salzberg (1941). «Аллилцианид» . Органический синтез .; Сборник , 1 , стр. 46
- ↑ Амос Терк; Генри Чанан (1947). «Биаллыл». Орг. Synth . 27 : 7. DOI : 10,15227 / orgsyn.027.0007 .
- ^ Международная программа по химической безопасности и Комиссия Европейских сообществ. «Аллилхлорид» . Международные карты химической безопасности . © МПХБ CEC 1993. Архивировано из оригинала на 2016-03-04 . Проверено 13 февраля 2012 года .