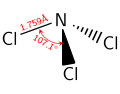| |||
| Имена | |||
|---|---|---|---|
| Другие названия Трихлорамин Аген Азот (III) хлорид Трихлоразан Трихлорнитрид | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.030.029 | ||
| Номер ЕС |
| ||
| 1840 г. | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| NCl 3 | |||
| Появление | желтая маслянистая жидкость | ||
| Запах | хлора -подобный | ||
| Плотность | 1,653 г / мл | ||
| Температура плавления | -40 ° С (-40 ° F, 233 К) | ||
| Точка кипения | 71 ° С (160 ° F, 344 К) | ||
| несмешивающийся медленно разлагается | |||
| Растворимость | растворим в бензоле , хлороформе , CCl 4 , CS 2 , PCl 3 | ||
| Состав | |||
| орторомбический (ниже −40 ° C) | |||
| тригонально-пирамидальный | |||
| 0,6 D | |||
| Термохимия | |||
Std энтальпия формации (Δ F H ⦵ 298 ) | 232 кДж / моль | ||
| Опасности | |||
Классификация ЕС (DSD) (устарела) | нет в списке | ||
| NFPA 704 (огненный алмаз) |  2 0 4 OX | ||
самовоспламенения температуру | 93 ° С (199 ° F, 366 К) | ||
| Родственные соединения | |||
Другие анионы | Трифторид азота Трибромид азота Трииодид азота | ||
Другие катионы | Треххлористый фосфор Треххлористый мышьяк | ||
Связанные хлорамины | Монохлорамин Дихлорамин | ||
Родственные соединения | Нитрозилхлорид | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Трихлорид азота , также известный как трихлорамин , представляет собой химическое соединение с формулой NCl 3 . Эта желтая, маслянистая, с резким запахом и взрывоопасная жидкость чаще всего встречается как побочный продукт химических реакций между производными аммиака и хлором (например, в плавательных бассейнах ). Наряду с монохлорамином и дихлорамином , трихлорамин отвечает за характерный `` запах хлора '', связанный с плавательными бассейнами, где соединение легко образуется в виде продукта из хлорноватистой кислоты, реагирующей с аммиаком.и другие азотистые вещества в воде, такие как мочевина из мочи . [1]
Подготовка и структура [ править ]
Соединение получают обработкой солей аммония, таких как нитрат аммония, хлором.
Промежуточные соединения в этом превращении включают монохлорамин и дихлорамин , NH 2 Cl и NHCl 2 соответственно.
Как и аммиак, NCl 3 представляет собой пирамидальную молекулу . Расстояния N-Cl составляют 1,76 Å, а углы Cl-N-Cl составляют 107 °. [2]
Реакции и использование [ править ]
Химия NCl 3 хорошо изучена. [3] Он умеренно полярный, с дипольным моментом 0,6 D. Азотный центр является основным, но гораздо слабее аммиака. Он гидролизуется горячей водой с высвобождением аммиака и хлорноватистой кислоты .
- NCl 3 + 3 H 2 O → NH 3 + 3 HOCl
NCl 3 взрывается с образованием N 2 и газообразного хлора. Эта реакция подавлена для разбавленных газов.
Трихлорид азота может образовываться в небольших количествах при дезинфекции монохлорамином водоснабжения в общественных местах и в плавательных бассейнах при дезинфекции хлором, вступающим в реакцию с мочевиной в моче и потом купающихся.
Трихлорид азота, торговую марку , как Agene , в свое время , использованное для отбеливателя муки , [4] , но эта практика была запрещена в Соединенных Штатах в 1949 году из - за соображений безопасности.
Безопасность [ править ]
Трихлорид азота может раздражать слизистые оболочки - это слезотечение , но никогда не использовалось как таковое. [5] [6] Чистое вещество (встречается редко) является опасным взрывчатым веществом, поскольку оно чувствительно к свету, теплу, даже умеренному удару и органическим соединениям. Пьер Луи Дюлон впервые приготовил его в 1812 году и потерял два пальца и глаз в результате двух взрывов. [7] В 1813 году взрыв NCl 3 временно ослепил сэра Хамфри Дэви , побудив его нанять Майкла Фарадея в качестве сослуживца. Вскоре после этого они оба были ранены в результате еще одного взрыва NCl 3 . [8]
См. Также [ править ]
- Список случаев заражения пищевых продуктов
Ссылки [ править ]
- ^ «Химия хлора - соединение хлора месяца: хлорамины: понимание« запаха бассейна » » . Американский химический совет . Проверено 17 декабря 2019 .
- ^ Holleman, AF; Виберг, Э. (2001). Неорганическая химия . Сан-Диего: Academic Press. ISBN 978-0-12-352651-9.
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- ^ Боярышник, J .; Тодд, JP (1955). «Некоторые эффекты кислорода на замес хлебного теста». Журнал продовольственной науки и сельского хозяйства . 6 (9): 501–511. DOI : 10.1002 / jsfa.2740060906 .
- Перейти ↑ White, GC (1999). Справочник по хлорированию и альтернативным дезинфицирующим средствам (4-е изд.). Вайли. п. 322. ISBN. 978-0-471-29207-4.
- ^ «Отчет об оценке опасности для здоровья: исследование симптомов у сотрудников в крытом аквапарке» (PDF) . NIOSH ENews . 6 (4). Август 2008 г. HETA 2007-0163-3062.
- ^ Thénard JL ; Бертолле С.Л. (1813 г.). «Репортаж о творчестве Пьера Луи Дюлонга». Annales de Chimie et de Physique . 86 (6): 37–43.
- Перейти ↑ Thomas, JM (1991). Майкл Фарадей и Королевский институт: Гений человека и места (PBK) . CRC Press. п. 17. ISBN 978-0-7503-0145-9.
Дальнейшее чтение [ править ]
- Джандер, Дж. (1976). Недавние химические и структурные исследования трииодида, трибромида, трихлорида азота и родственных соединений . Успехи неорганической химии . Успехи неорганической химии и радиохимии. 19 . С. 1–63. DOI : 10.1016 / S0065-2792 (08) 60070-9 . ISBN 9780120236190.
- Kovacic, P .; Лоури, МК; Поле, кВт (1970). «Химия N-бромаминов и N-хлораминов». Химические обзоры . 70 (6): 639–665. DOI : 10.1021 / cr60268a002 .
- Hartl, H .; Schöner, J .; Jander, J .; Шульц, Х. (1975). «Die Struktur des Festen Stickstofftrichlorids (-125 ° C)». Zeitschrift für Anorganische und Allgemeine Chemie . 413 (1): 61–71. DOI : 10.1002 / zaac.19754130108 .
- Cazzoli, G .; Фаверо, PG; Даль Борго, А. (1974). "Молекулярная структура, ядерная квадрупольная константа взаимодействия и дипольный момент трихлорида азота из микроволновой спектроскопии". Журнал молекулярной спектроскопии . 50 (1–3): 82–89. Bibcode : 1974JMoSp..50 ... 82С . DOI : 10.1016 / 0022-2852 (74) 90219-7 .
- Bayersdorfer, L .; Engelhardt, U .; Фишер, Дж .; Höhne, K .; Джандер, Дж. (1969). "Untersuchungen an Stickstoff – Chlor-Verbindungen. V. Infrarot- und RAMAN-Spektren von Stickstofftrichlorid". Zeitschrift für Anorganische und Allgemeine Chemie . 366 (3–4): 169–179. DOI : 10.1002 / zaac.19693660308 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме трихлорида азота . |
- OSHA - Трихлорид азота
- Трихлорид азота - Ссылки на здоровье
| NH 3 N 2 H 4 | Он (N 2 ) 11 | ||||||||||||||||
| Ли 3 Н | Be 3 N 2 | BN | β-C 3 N 4 г-C 3 N 4 C x N y | № 2 | N x O y | NF 3 | Ne | ||||||||||
| Na 3 N | Mg 3 N 2 | AlN | Si 3 N 4 | PN P 3 N 5 | S x N y SN S 4 N 4 | NCl 3 | Ar | ||||||||||
| К 3 Н | Ca 3 N 2 | ScN | Банка | VN | CrN Cr 2 N | Mn x N y | Fe x N y | Против | Ni 3 N | CuN | Zn 3 N 2 | GaN | Ge 3 N 4 | В виде | Se | NBr 3 | Kr |
| Руб. | Sr 3 N 2 | YN | ZrN | NbN | β-Mo 2 N | Tc | RU | Rh | PdN | Ag 3 N | CdN | Гостиница | Sn | Sb | Te | NI 3 | Xe |
| CS | Ba 3 N 2 | Hf 3 N 4 | TaN | WN | Re | Операционные системы | Ir | Pt | Au | Hg 3 N 2 | TlN | Pb | BiN | По | В | Rn | |
| Пт | Ra 3 N 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Ур. | Ц | Og | |
| ↓ | |||||||||||||||||
| Ла | CeN | Pr | Nd | Вечера | См | Евросоюз | GdN | Tb | Dy | Хо | Э | Тм | Yb | Лу | |||
| Ac | Чт | Па | U 2 N 3 | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||