| |||
 Структура безводного соединения | |||
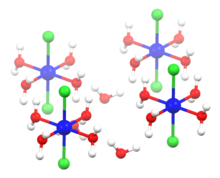 Структура гексагидрата | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Хлорид кобальта (II) | |||
| Другие имена | |||
| Идентификаторы | |||
| |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.718 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII |
| ||
| Номер ООН | 3288 | ||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| CoCl 2 | |||
| Молярная масса | 129,839 г / моль (безводный) 165,87 г / моль (дигидрат) 237,93 г / моль (гексагидрат) | ||
| Внешность | синие кристаллы (безводные) фиолетово-синие (дигидрат) розовые красные кристаллы (гексагидрат) | ||
| Плотность | 3,356 г / см 3 (безводный) 2,477 г / см 3 (дигидрат) 1,924 г / см 3 (гексагидрат) | ||
| Температура плавления | 726 ° C (1339 ° F, 999 K) ± 2 (безводный) [2] 140 ° C (моногидрат) 100 ° C (дигидрат) 86 ° C (гексагидрат) | ||
| Точка кипения | 1049 ° С (1,920 ° F, 1322 К) | ||
| 43,6 г / 100 мл (0 ° C) 45 г / 100 мл (7 ° C) 52,9 г / 100 мл (20 ° C) 105 г / 100 мл (96 ° C) | |||
| Растворимость | 38,5 г / 100 мл (метанол) 8,6 г / 100 мл (ацетон) растворим в этаноле , пиридине , глицерине | ||
| + 12,660 · 10 −6 см 3 / моль | |||
| Структура | |||
| CdCl 2 Структура | |||
Координационная геометрия | гексагональный (безводный) моноклинный (дигидрат) Октаэдрический (гексагидрат) | ||
| Опасности | |||
| Паспорт безопасности | ICSC 0783 | ||
| Пиктограммы GHS | |||
| NFPA 704 (огненный алмаз) | [3]  3 0 0 | ||
| точка возгорания | Негорючий | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 80 мг / кг (крыса, перорально) | ||
| Родственные соединения | |||
Другие анионы | Фторид кобальта (II) Бромид кобальта (II) Иодид кобальта (II) | ||
Другие катионы | Хлорид родия (III) Хлорид иридия (III) | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Кобальт (II) , хлорид представляет собой неорганическое соединение из кобальта и хлора , с формулой COCl
2. Это небесно-голубое кристаллическое твердое вещество.
Соединение образует несколько гидратов CoCl
2• n H
2O для n = 1, 2, 6 и 9. Утверждения об образовании три- и тетрагидратов не подтвердились. [4] Дигидрат имеет фиолетовый цвет, а гексагидрат розовый. Обычно поставляется в виде гексагидрата CoCl.
2· 6 H
2О , который является одним из наиболее часто используемых соединений кобальта в лаборатории. [5]
Из-за легкости реакции гидратации / дегидратации и возникающего в результате изменения цвета хлорид кобальта используется в качестве индикатора воды в осушителях .
Ниши использования хлорида кобальта включают его роль в органическом синтезе и гальванике объектов металлическим кобальтом.
Хлорид кобальта был классифицирован Европейским химическим агентством как вещество, вызывающее серьезную озабоченность , поскольку он предположительно является канцерогеном.
Свойства [ править ]
Безводный [ править ]
При комнатной температуре безводный хлорид кобальта имеет структуру хлорида кадмия (II) ( CdCl
2) (R 3 m), в котором ионы кобальта (II) координированы октаэдрически. Считается, что примерно при 706 ° C (на 20 градусов ниже точки плавления) координация меняется на тетраэдрическую. [2] Давление паров при температуре плавления составляет 7,6 мм рт . [6]
Решения [ править ]
Хлорид кобальта хорошо растворяется в воде. При атмосферном давлении, то массовая концентрация в А насыщенном раствор из CoCl
2в воде около 54% при температуре кипения 120,2 ° C; 48% при 51,25 ° С; 35% при 25 ° C; 33% при 0 ° С; и 29% при -27,8 ° C. [4]
Разбавленные водные растворы CoCl
2содержат виды [Co (H
2O)
6]2+
, кроме хлорид- ионов. Концентрированные растворы имеют красный цвет при комнатной температуре, но становятся синими при более высоких температурах. [7]
Увлажняет [ править ]
Кристаллическая единица твердого гексагидрата CoCl
2• 6 часов
2O содержит нейтральную молекулу транс - CoCl
2(ЧАС
2O)
4и две молекулы кристаллизационной воды . [8] Этот вид легко растворяется в воде и спирте .
Безводная соль гигроскопична, а гексагидрат расплывается . [ необходима цитата ] Дигидрат CoCl 2 (H 2 O) 2 является координационным полимером . Каждый Со-центр координирован с четырьмя двойными мостиковыми мостиковыми лигандами . Октаэдр завершается парой взаимно транскволигандов . [9]
Подготовка [ править ]
Хлорид кобальта может быть приготовлен в водном растворе из кобальта (II) гидроксид или кобальта (II) карбоната и соляной кислоты :
- CoCO
3+ 2 HCl (водн.) → CoCl
2(водн.) + CO
2 - Со (ОН)
2+ 2 HCl (водн.) → CoCl
2(водн.) + 2 H
2О
Твердый дигидрат и гексагидрат можно получить выпариванием. Охлаждение насыщенных водных растворов дает дигидрат при температуре от 120,2 ° C до 51,25 ° C и гексагидрат ниже 51,25 ° C. Водяной лед, а не хлорид кобальта, будет кристаллизоваться из растворов с концентрацией ниже 29%. Моногидрат и безводные формы могут быть получены путем охлаждения растворов только под высоким давлением, выше 206 ° C и 335 ° C соответственно. [4]
Безводное соединение можно получить путем нагревания гидратов. [10] При быстром нагревании или в закрытом контейнере каждый из 6-, 2- и 1-гидратов частично плавится в смесь следующего низшего гидрата и насыщенного раствора - при 51,25 ° C, 206 ° C, и 335 ° C соответственно. При медленном нагревании в открытом контейнере вода испаряется из каждого твердого 6-, 2- и 1-гидрата, оставляя следующий более низкий гидрат - примерно при 40 ° C, 89 ° C и 126 ° C соответственно. . [4]
Обезвоживание также можно осуществить с помощью триметилсилилхлорида : [11]
- CoCl
2• 6 часов
2O + 12 (CH
3)
3SiCl → CoCl
2+ 6 [(CH
3)
3SiCl]
2O + 12 HCl
Безводное соединение можно очистить сублимацией в вакууме. [2]
Реакции [ править ]
В лаборатории хлорид кобальта (II) является обычным предшественником других соединений кобальта. Обычно водные растворы соли ведут себя так же, как и другие соли кобальта (II), поскольку эти растворы состоят из [Co (H
2O)
6]2+
ион независимо от аниона. Например, в таких растворах при обработке сероводородом H образуется осадок сульфида кобальта CoS.
2S .
Комплексные хлориды [ править ]
Гексагидрат и безводная соль являются слабыми кислотами Льюиса . В аддуктах , как правило , либо октаэдрические или тетраэдрические . С пиридином ( C
5ЧАС
5N ) получается октаэдрический комплекс:
- CoCl
2· 6 H
2O + 4 C
5ЧАС
5N → CoCl
2(C
5ЧАС
5N)
4+ 6 часов
2О
С трифенилфосфином ( P (C
6ЧАС
5)
3), получается тетраэдрический комплекс:
- CoCl
2· 6 H
2O + 2 P (C
6ЧАС
5)
3→ CoCl
2[ПК
6ЧАС
5)
3]
2+ 6 часов
2О
Соли анионного комплекса CoCl 4 2− могут быть получены с использованием хлорида тетраэтиламмония: [12]
- CoCl
2+ 2 [(C 2 H 5 ) 4 N] Cl → [(C 2 H 5 ) 4 N)] 2 [CoCl 4 ]
Ион [CoCl 4 ] 2- представляет собой синий ион, который образуется при добавлении соляной кислоты к водным растворам гидратированного хлорида кобальта, которые имеют розовый цвет.
Сокращение [ править ]
Реакция безводного соединения с циклопентадиенидом натрия дает кобальтоцен Co (C
5ЧАС
5)
2. Эта 19-электронная разновидность является хорошим восстановителем, легко окисляясь до желтого 18-электронного катиона кобальтацения [Co (C
5ЧАС
5)
2]+
.
Окисление до кобальта (III) [ править ]
Существуют соединения кобальта в степени окисления +3, такие как фторид кобальта (III) CoF
3, нитрат Co (NO
3)
3, и сульфат Co
2(ТАК
4)
3; однако хлорид кобальта (III) CoCl
3нестабилен в нормальных условиях и немедленно разлагается на CoCl
2и хлор . [13]
С другой стороны, хлориды кобальта (III) могут быть получены, если кобальт связан также с другими лигандами с большей основностью по Льюису, чем хлорид, такими как амины . Например, в присутствии аммиака хлорид кобальта (II) легко окисляется кислородом воздуха до хлорида гексамминкобальта (III) :
- 4 CoCl
2· 6 H
2O + 4 NH
4Cl + 20 NH
3+ O
2→ 4 [Co (NH
3)
6] Cl
3+ 26 часов
2О
Аналогичные реакции происходят с другими аминами . Эти реакции часто проводят в присутствии древесного угля в качестве катализатора или с перекисью водорода H.
2О
2заменен атмосферным кислородом. Другие высокоосновные лиганды, включая карбонат , ацетилацетонат и оксалат , вызывают образование производных Co (III). Простые карбоксилаты и галогениды этого не делают.
В отличие от комплексов Co (II), комплексы Co (III) очень медленно обмениваются лигандами , поэтому они считаются кинетически инертными . Немецкий химик Альфред Вернер был удостоен Нобелевской премии в 1913 году за свои исследования серии этих соединений кобальта (III), работа, которая привела к пониманию структуры таких координационных соединений .
Окисление до кобальта (IV) [ править ]
Реакция 1-норбониллития с CoCl
2· ТГФ в пентане производит коричневый, термически стабильный тетралкил кобальта (IV) [14] [15] - редкий пример стабильного соединения переходного металла / насыщенного алкана [5], различные продукты получают в других растворителях. [16]
Проблемы со здоровьем [ править ]
Кобальт необходим для большинства высших форм жизни, но более нескольких миллиграммов в день вредны. Хотя отравления редко вызываются соединениями кобальта, их хроническое употребление вызывает серьезные проблемы со здоровьем при дозах, намного меньших, чем смертельная. В 1966 году добавление соединений кобальта для стабилизации пивной пены в Канаде привело к своеобразной форме вызванной токсинами кардиомиопатии , которая стала известна как кардиомиопатия пьющих пиво . [17] [18] [19]
Кроме того, согласно Монографиям Международного агентства по исследованию рака (IARC) , хлорид кобальта (II) подозревается как вызывающий рак (т.е. возможно канцерогенный , группа 2B IARC). [20]
В 2005–2006 годах хлорид кобальта был восьмым по распространенности аллергеном в патч-тестах (8,4%). [21]
Другое использование [ править ]
- Невидимые чернила : при суспендировании в растворе хлорид кобальта (II) может казаться невидимым на поверхности; когда эта же поверхность впоследствии подвергается значительному нагреву (например, от ручного теплового пистолета или зажигалки), чернила навсегда / необратимо становятся синими.
- Хлорид кобальта является признанным химическим индуктором гипоксических реакций, таких как эритропоэз . [ необходима цитата ] Добавки кобальта не запрещены и, следовательно, не будут обнаружены текущими антидопинговыми тестами. [22] Хлорид кобальта запрещен Советом по чистокровным гонкам Австралии. [23]
- Хлорид кобальта - это один из методов, используемых для индукции легочной артериальной гипертензии у животных для исследования и оценки эффективности лечения.
Ссылки [ править ]
- ^ "Кобальт хлористый, номер CAS: 7646-79-9" . www.chemindustry.com . Проверено 19 апреля 2018 года .
- ^ a b c Wojakowska, A., Krzyżak, E. и Plińska, S. (2007): "Плавление и высокотемпературные твердотельные переходы в галогенидах кобальта (II)". Журнал термического анализа и калориметрии , том 88, выпуск 2, страницы 525-530. DOI : 10.1007 / s10973-006-8000-9
- ^ Санта-Крус Биотехнология: хлорид кобальта (II)
- ^ a b c d М. Т. Сожье, М. Ноайи, Р. Коэн-Адад, Ф. Паулик и Дж. Паулик (1977): "Equilibres solide liquid vapeur du systeme binaire CoCl.
2- H
2O " Журнал термического анализа , том 11, выпуск 1, страницы 87–100. Doi : 10.1007 / BF02104087 Примечание: самая низкая точка на рис. 6 несовместима с рис. 7; вероятно, должна быть -27,8 ° C вместо 0 ° C. . - ^ a b Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- ^ Юзо Саеки, Рёко Мацудзаки, Наоми Аояма (1977): «Давление паров кобальта дихлорида». Журнал менее распространенных металлов , том 55, выпуск 2, страницы 289-291. DOI : 10.1016 / 0022-5088 (77) 90204-1
- ^ The Merck Index , 7-е издание, Merck & Co, Рэуэй, Нью-Джерси, США, 1960.
- ^ Уэллс, AF (1984), Структурная неорганическая химия (5-е изд.), Oxford: Clarendon Press, ISBN 0-19-855370-6
- ^ Морозин, Б .; Грэбер, EJ (1965). «Кристаллические структуры дигидрата хлорида марганца (II) и железа (II)». Журнал химической физики . 42 (3): 898–901. Bibcode : 1965JChPh..42..898M . DOI : 10.1063 / 1.1696078 .
- ^ Джон Даллас Дональдсон, Детмар Бейерсманн, «Соединения кобальта и кобальта» в Энциклопедии промышленной химии Ульманна, Wiley-VCH, Weinheim, 2005. doi : 10.1002 / 14356007.a07_281.pub2
- ^ Филипп Boudjouk, Jeung-Ho So (1992). «Сольватированные и несольватированные безводные хлориды металлов из гидратов хлоридов металлов». Неорганические синтезы . Неорг. Synth . Неорганические синтезы. 29 . С. 108–111. DOI : 10.1002 / 9780470132609.ch26 . ISBN 9780470132609.CS1 maint: использует параметр авторов ( ссылка )
- Перейти ↑ Gill, NS & Taylor, FB (1967). Тетрагалогические комплексы дипозитных металлов в первой переходной серии . Неорг. Synth. Неорганические синтезы. 9 . С. 136–142. DOI : 10.1002 / 9780470132401.ch37 . ISBN 9780470132401.
- ^ Справочник по химии и физике , 71-е издание, CRC Press, Анн-Арбор, Мичиган, 1990.
- ↑ Бартон К. Бауэр и Ховард Г. Теннент (1972). «Бицикло [2.2.1] гепт-1-илы переходного металла». Варенье. Chem. Soc. 94 (7): 2512–2514. DOI : 10.1021 / ja00762a056 .
- ^ Эрин К. Бирн; Даррин С. Ричсон и Клаус Х. Теопольд (1986). «Тетракис (1-норборнил) кобальт, низкоспиновый тетраэдрический комплекс переходного металла первого ряда». J. Chem. Soc., Chem. Commun. (19): 1491–1492. DOI : 10.1039 / C39860001491 .
- ^ Эрин К. Бирн; Клаус Х. Теопольд (1989). «Синтез, характеристика и электронная реакционная способность норборнильных комплексов кобальта в необычно высоких степенях окисления». Варенье. Chem. Soc. 111 (11): 3887–3896. DOI : 10.1021 / ja00193a021 .
- ^ Morin Y; Tětu A; Мерсье Дж. (1969). "Кардиомиопатия пьющих пиво Квебека: Клинические и гемодинамические аспекты". Летопись Нью-Йоркской академии наук . 156 (1): 566–576. Bibcode : 1969НЯСА.156..566M . DOI : 10.1111 / j.1749-6632.1969.tb16751.x . PMID 5291148 . S2CID 7422045 .
- ^ Barceloux, Дональд Г. & Barceloux, Дональд (1999). «Кобальт». Клиническая токсикология . 37 (2): 201–216. DOI : 10,1081 / CLT-100102420 . PMID 10382556 .
- ^ 11.1.5 Необычный тип миокардиопатии, выявленный в 1965 и 1966 годах в Квебеке (Канада), Миннеаполисе (Миннесота), Лёвене (Бельгия) и Омахе (Небраска), был связан с эпизодами острой сердечной недостаточности (e / g /, 50 смертей среди 112 пьющих пиво).
- ^ Zug KA, Warshaw EM, Fowler JF Jr, Maibach HI, Belsito DL, Pratt MD, Sasseville D, Storrs FJ, Taylor JS, Mathias CG, Deleo VA, Rietschel RL, Marks J. Результаты патч-теста североамериканского контакта Группа дерматитов 2005–2006 гг. Дерматит. 2009 май – июнь; 20 (3): 149-60.
- Перейти ↑ Lippi G, Franchini M, Guidi GC (ноябрь 2005 г.). «Введение хлорида кобальта спортсменам: новый взгляд на допинг крови?» . Br J Sports Med . 39 (11): 872–3. DOI : 10.1136 / bjsm.2005.019232 . PMC 1725077 . PMID 16244201 .
- ↑ Бартли, Патрик (6 февраля 2015 г.). «Кобальтовый кризис обращает взоры всего мира на австралийские гонки» . Сидней Морнинг Геральд .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы, связанные с хлоридом кобальта (II) . |
- Международная карта химической безопасности 0783
- Национальный реестр загрязнителей - информационный бюллетень по кобальту
- Монография МАИР «Кобальт и соединения кобальта»

