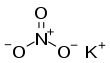| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Азотнокислый калий | |||
| Другие имена | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.926 | ||
| Номер ЕС |
| ||
| Номер E | E252 (консерванты) | ||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1486 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| KNO 3 | |||
| Молярная масса | 101,1032 г / моль | ||
| Внешность | белое твердое вещество | ||
| Запах | без запаха | ||
| Плотность | 2,109 г / см 3 (16 ° С) | ||
| Температура плавления | 334 ° С (633 ° F, 607 К) | ||
| Точка кипения | 400 ° С (752 ° F, 673 К) (разлагается) | ||
| 133 г / л (0 ° C) 316 г / л (20 ° C) 383 г / л (25 ° C) 2439 г / л (100 ° C) [3] | |||
| Растворимость | мало растворим в этаноле растворим в глицерине , аммиаке | ||
| Основность (p K b ) | 15.3 [4] | ||
Магнитная восприимчивость (χ) | -33,7 · 10 -6 см 3 / моль | ||
Показатель преломления ( n D ) | 1,335, 1,5056, 1,5604 | ||
| Структура | |||
Кристальная структура | Орторомбический , Арагонит | ||
| Термохимия | |||
Теплоемкость ( C ) | 95.06 Дж / моль К | ||
Std энтальпия формации (Δ F H ⦵ 298 ) | -494,00 кДж / моль | ||
| Опасности | |||
| Основные опасности | Окислитель, вреден при проглатывании, вдыхании или попадании на кожу. Вызывает раздражение кожи и области вокруг глаз. | ||
| Паспорт безопасности | См .: страницу данных ICSC 0184 | ||
| Пиктограммы GHS | |||
Положения об опасности GHS | H272 , H315 , H319 , H335 | ||
Меры предосторожности GHS | P102 , P210 , P220 , P221 , P280 | ||
| NFPA 704 (огненный алмаз) |  1 0 0 OX | ||
| точка возгорания | негорючий (окислитель) | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 1901 мг / кг (перорально, кролик) 3750 мг / кг (перорально, крыса) [5] | ||
| Родственные соединения | |||
Другие анионы | Нитрит калия | ||
Другие катионы | Нитрат лития Нитрат натрия Нитрат рубидия Нитрат цезия | ||
Родственные соединения | Сульфат калия Хлорид калия | ||
| Страница дополнительных данных | |||
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. | ||
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ | ||
Спектральные данные | УФ , ИК , ЯМР , МС | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Нитрат калия - это химическое соединение с химической формулой K N O.
3. Это ионную соль из калия ионов К + и нитрат - ионов NO 3 - , и поэтому является нитрат щелочного металла . Он встречается в природе в виде минерала, селитры (или селитры в Великобритании). [6] Это источник азота , и азот был назван в честь селитры. Нитрат калия - одно из нескольких азотсодержащих соединений, вместе называемых селитрой (или селитрой в Великобритании). [6]
В основном нитрат калия используется в удобрениях , удалении пней , ракетном топливе и фейерверках . Это один из основных компонентов пороха (черного пороха). [7] В обработанном мясе нитрат калия вступает в реакцию с гемоглобином и миоглобином, образуя синий цвет. [8]
Этимология [ править ]
Нитрат калия из-за своего раннего и глобального использования и производства имеет много названий. В еврейских и египетских словах для этого слова были согласные буквы ntr, что указывает на вероятное родство в греческом языке nitron , который был латинизирован до nitrum или nitrium . Отсюда старофранцузский язык селитры и среднеанглийский селитра . К 15 веку европейцы стали называть его селитрой [9], а позже - нитратом калия, поскольку химия этого соединения была более понятна.
Арабы называли его «китайским снегом» ( арабский : ثلج الصين thalj аль-син ). Она была названа "китайской солью" иранцы / персами [10] [11] [12] [13] [14] или "соль из китайских солончаков" ( персидские : نمک شوره چينی намак Шура Chini ). [15] [16]
Свойства [ править ]
Нитрат калия имеет ромбическую кристаллическую структуру при комнатной температуре, которая превращается в тригональную систему при 129 ° C (264 ° F).
Нитрат калия умеренно растворим в воде, но его растворимость увеличивается с температурой. Водный раствор почти нейтрален, показывая pH 6,2 при 14 ° C (57 ° F) для 10% раствора коммерческого порошка. Он не очень гигроскопичен , впитывает около 0,03% воды при относительной влажности 80% в течение 50 дней. Он не растворяется в спирте и не ядовит; он может взрывоопасно реагировать с восстановителями , но сам по себе не взрывоопасен. [3]
Термическое разложение [ править ]
Между 550–790 ° C (1022–1,454 ° F) нитрат калия достигает зависимого от температуры равновесия с нитритом калия : [17]
- 2 KNO 3 ⇌ 2 KNO 2 + O 2
История производства [ править ]
Из минеральных источников [ править ]
В Древней Индии производители селитры составляли касту Нуния. [18] селитра находит упоминание в Каутилии Артхашастров (составитель 300BC - 300CE), который упоминает , используя свой ядовитый дым в качестве орудия войны, [19] , хотя его использование для приведения в движении не появлялось до средневековья.
Процесс очистки нитрата калия был описан в 1270 году химиком и инженером Хасаном аль-Раммах из Сирии в его книге « Аль-Фурусийя ва аль-Манасиб аль-Харбийя» ( «Книга о военном искусстве и изобретательных военных устройствах» ). В этой книге аль-Раммах сначала описывает очистку баруда (неочищенного минерала селитры) кипячением его с минимальным количеством воды и использованием только горячего раствора, а затем использование карбоната калия (в виде древесной золы ) для удаления кальция и магния. путем осаждения их карбонатов из этого раствора, в результате чего остается раствор очищенного нитрата калия, который затем может быть высушен. [20]Его использовали для изготовления пороха и взрывных устройств. Терминология, использованная аль-Раммахом, указала на китайское происхождение порохового оружия, о котором он писал. [21]
По крайней мере, еще в 1845 году месторождения нитратита разрабатывались в Чили и Калифорнии.
Из пещер [ править ]
Основным естественным источником нитрата калия были отложения, кристаллизующиеся из стен пещер, и скопления гуано летучих мышей в пещерах. [22] Экстракция осуществляется путем погружения гуано в воду на день, фильтрации и сбора кристаллов в фильтрованной воде. Традиционно гуано использовалось в Лаосе для производства пороха для ракет Bang Fai .
ЛеКонт [ править ]
Возможно, наиболее исчерпывающим обсуждением создания этого материала является текст ЛеКонта 1862 года . [23] Он писал с явной целью увеличения производства в Конфедеративных Штатах для поддержки их потребностей во время Гражданской войны в США . Поскольку он призывал сельские фермерские общины за помощью, описания и инструкции просты и понятны. Он подробно описывает «французский метод» вместе с несколькими вариациями, а также «швейцарский метод». NB. Было сделано много ссылок на метод, использующий только соломинку и мочу, но в данной работе такого метода нет.
Французский метод [ править ]
Тюрго и Лавуазье создали Régie des Poudres et Salpêtres за несколько лет до Французской революции . Грядки селитры были подготовлены путем смешивания навоза с строительным раствором или древесной золой, обычной землей и органическими материалами, такими как солома, чтобы придать пористость компостной куче, обычно 4 фута (1,2 м) в высоту, 6 футов (1,8 м) в ширину и 15 футов. (4,6 м) в длину. [23] Куча обычно находилась под укрытием от дождя, увлажнялась мочой , часто переворачивалась для ускорения разложения, а затем, наконец, через год выщелачивалась водой для удаления растворимого нитрата кальция.который затем был преобразован в нитрат калия путем фильтрации через калий .
Швейцарский метод [ править ]
ЛеКонт описывает процесс, в котором используется только моча, а не навоз, называя его швейцарским методом . Мочу собирают прямо в песочнице под хлевом. Сам песок выкапывают и выщелачивают на нитраты, которые затем превращают в нитрат калия с помощью поташа, как указано выше.
Из азотной кислоты [ править ]
С 1903 года до начала Первой мировой войны нитрат калия для получения черного пороха и удобрений производился в промышленных масштабах из азотной кислоты, производимой с использованием процесса Биркеланда – Эйда , в котором для окисления азота из воздуха использовалась электрическая дуга. Во время Первой мировой войны новый промышленный процесс Габера (1913) был объединен с процессом Оствальда после 1915 года, что позволило Германии производить азотную кислоту для войны после того, как она была отрезана от поставок минеральных нитратов натрия из Чили (см. Нитратит ).
Производство [ править ]
Нитрат калия можно получить, объединив нитрат аммония и гидроксид калия .
- NH 4 NO 3 (водн.) + KOH (водн.) → NH 3 (г) + KNO 3 (водн.) + H 2 O (л)
Альтернативный способ получения нитрата калия без побочного продукта аммиака является сочетание нитрата аммония, найденный в мгновенные пакеты со льдом , [24] и хлорид калия , легко получить в виде натриевой свободной заменитель соли .
- NH 4 NO 3 (водн.) + KCl (водн.) → NH 4 Cl (водн.) + KNO 3 (водн.)
Нитрат калия можно также получить путем нейтрализации азотной кислоты гидроксидом калия. Эта реакция очень экзотермична.
- КОН (водн.) + HNO 3 → KNO 3 (водн.) + H 2 O (л)
В промышленных масштабах его получают путем реакции двойного вытеснения между нитратом натрия и хлоридом калия.
- NaNO 3 (водн.) + KCl (водн.) → NaCl (водн.) + KNO 3 (водн.)
Использует [ редактировать ]
Нитрат калия имеет множество применений, в основном как источник нитрата.
Производство азотной кислоты [ править ]
Исторически азотная кислота производилась путем соединения серной кислоты с нитратами, такими как селитра. В наше время все наоборот: нитраты производятся из азотной кислоты, полученной с помощью процесса Оствальда .
Окислитель [ править ]
Наиболее известное применение нитрата калия, вероятно, в качестве окислителя в черном порохе . С древнейших времен до конца 1880-х годов черный порох обеспечивал взрывную силу для всего огнестрельного оружия в мире. По истечении этого времени, стрелковое оружие и большие артиллерии все чаще стали зависеть от кордита , в бездымный порох . Черный порох по-прежнему используется в ракетных двигателях на черном порохе , но также в сочетании с другими видами топлива, такими как сахар в « ракетных конфетах ». Он также используется в фейерверках, таких как дымовые шашки . [25] Он также добавляется в сигареты для поддержания равномерного горения табака [26] и используется для обеспечения полного сгорания табака.бумажные патроны для капсюльных и шаровых револьверов. [27] Его также можно нагреть до нескольких сотен градусов, чтобы использовать для воронения селитры , которая менее долговечна, чем другие формы защитного окисления, но допускает специфическое и часто красивое окрашивание стальных деталей, таких как винты, штифты и т. Д. мелкие части огнестрельного оружия.
Обработка мяса [ править ]
Нитрат калия был обычным ингредиентом соленого мяса с древних времен [28] или средневековья . [29] Широкое распространение использования нитратов произошло сравнительно недавно и связано с развитием крупномасштабной мясопереработки. [7] Использование нитрата калия было в основном прекращено из-за медленных и противоречивых результатов по сравнению с соединениями нитрита натрия, такими как «пражский порошок» или розовая « отверждающая соль ». Несмотря на это, нитрат калия все еще используется в некоторых пищевых продуктах, таких как салями, вяленая ветчина, мясные закуски и (в некоторых странах) в рассоле, используемом для приготовления солонины.(иногда вместе с нитритом натрия ). [30] При использовании в качестве пищевой добавки в Европейском Союзе [31] соединение обозначается как E252 ; он также одобрен для использования в качестве пищевой добавки в США [32], Австралии и Новой Зеландии [33] (где он указан под номером INS 252). [3]
Приготовление пищи [ править ]
В западноафриканской кухне нитрат калия (селитра) широко используется в качестве загустителя в супах и тушеных блюдах, таких как суп с бамией [34] и isi ewu . Он также используется для смягчения пищи и сокращения времени приготовления при варке фасоли и крутого мяса. Селитра также является важным ингредиентом при приготовлении особых каш, таких как кунун канва [35], что дословно переводится с языка хауса как «каша из селитры». На Шетландских островах (Великобритания) его используют при консервировании баранины для приготовления местного деликатеса - баранины реестит . [36]
Удобрение [ править ]
Нитрат калия используется в удобрениях как источник азота и калия - двух макроэлементов для растений. При использовании отдельно он имеет рейтинг NPK 13-0-44. [37] [38]
Фармакология [ править ]
- Используется в некоторых зубных пастах для чувствительных зубов . [39] В последнее время увеличилось использование нитрата калия в зубных пастах для лечения чувствительных зубов. [40] [41]
- Исторически использовался для лечения астмы. [42] Используется в некоторых зубных пастах для облегчения симптомов астмы. [43]
- Используется в Таиланде в качестве основного ингредиента таблеток для почек для облегчения симптомов цистита , пиелита и уретрита . [44]
- Борется с повышенным кровяным давлением и когда-то использовался как гипотензивное средство . [45]
Другое использование [ править ]
- Электролит в солевом мостике
- Действующее вещество конденсированных аэрозольных систем пожаротушения . При сжигании свободными радикалами пламени огня образуется карбонат калия . [46]
- Работает как очиститель алюминия.
- Компонент (обычно около 98%) некоторых продуктов для удаления пней . Он ускоряет естественное разложение пня, поставляя азот грибам, поражающим древесину пня. [47]
- При термической обработке металлов в ванне расплава солей средней температуры, обычно в сочетании с нитритом натрия. Подобная ванна используется для получения прочного сине-черного покрытия, которое обычно встречается на огнестрельном оружии. Его окислительные свойства, водорастворимость и низкая стоимость делают его идеальным краткосрочным ингибитором ржавчины . [48]
- Чтобы вызвать цветение манговых деревьев на Филиппинах. [49] [50]
- Тепловой накопитель в энергосистемах . Соли нитрата натрия и калия хранятся в расплавленном состоянии с солнечной энергией, собираемой гелиостатами на Гемасолар термосолнечной установке . Было обнаружено, что тройные соли с добавлением нитрата кальция или нитрата лития улучшают способность аккумулировать тепло в расплавленных солях. [51]
- Как источник ионов калия для обмена с ионами натрия в химически упрочненном стекле .
- Как окислитель в модельном ракетном топливе называется Ракетная конфета .
В фольклоре и массовой культуре [ править ]
Когда-то считалось, что нитрат калия вызывает импотенцию , и до сих пор ходят слухи, что он присутствует в пищевых продуктах (например, в военной еде) как анафродизиак ; однако нет никаких научных доказательств таких свойств. [52] [53]
В фильме «Пролетая над гнездом кукушки» медсестры просят Рэндалла принять его лекарства, но, не зная, что это такое, он упоминает, что не хочет, чтобы кто-то «подсунул мне селитру». Затем он переходит к имитации мастурбации в отношении ее предполагаемых эффектов как анафродизиака .
В 1776 году Джон Адамс просит свою жену Абигейл сделать селитру для Континентальной армии. В конце концов, она может сделать это в обмен на булавки для шитья. [54]
В эпизоде « Арена » из « Звездного пути » капитан Кирк ранит горна, используя рудиментарную пушку, которую он построил с использованием нитрата калия в качестве ключевого ингредиента смеси пороха .
На 21 Jump Street Дженко, которого играет Ченнинг Татум , сделал рифмованную презентацию о нитрате калия для своего урока химии.
В манге и аниме-сериале Dr. Stone », нитрат калия используется вместе с этанолом, чтобы избавить людей от вымышленного состояния под названием« окаменение ».
В « Поедании Рауля» Пол нанимает Доминатрикс, чтобы она выдавала себя за медсестру и обманом заставила Рауля съесть Соль Питера, чтобы уменьшить его сексуальный аппетит к жене.
См. Также [ править ]
- Нитроцеллюлоза
- Перхлорат калия
- Нитра , минеральная форма нитрата калия
Ссылки [ править ]
- ^ Запись о нитрате калия в базе данных веществ GESTIS Института безопасности и гигиены труда , доступ осуществлен 09 марта 2007 г. Ошибка в шаблоне * недопустимый параметр ( шаблон: GESTIS ): 'CAS'
- Перейти ↑ Gustafson, AF (1949). Справочник удобрений - их источники, состав, действие и использование . п. 25. ISBN 9781473384521. Архивировано 17 февраля 2017 года.
- ^ a b c Б. Дж. Косанке; Б. Стурман; К. Косанке; И. фон Мальтиц; Т. Симидзу; М.А. Уилсон; Н. Кубота; К. Дженнингс-Уайт; Д. Чепмен (2004). «2» . Пиротехническая химия . Журнал пиротехники. С. 5–6. ISBN 978-1-889526-15-7. Архивировано 05 мая 2016 года.
- ^ Колтхофф Трактат по аналитической химии, НьюЙорк, Межнаучной Encyclopedia, Inc., 1959.
- ^ Chem.sis.nlm.nih.gov Архивировано 12 августа 2014 г. в Wayback Machine.
- ^ a b Краткий Оксфордский словарь английского языка (6-е изд.). Соединенное Королевство: Издательство Оксфордского университета . 2007. с. 3804. ISBN 9780199206872.
- ^ a b Лауэр, Клаус (1991). «История нитритов в питании человека: материалы из немецких кулинарных книг». Журнал клинической эпидемиологии . 44 (3): 261–264. DOI : 10.1016 / 0895-4356 (91) 90037-A . ISSN 0895-4356 . PMID 1999685 .
- Перейти ↑ Haldane, J. (1901). «Красный цвет соленого мяса» . Журнал гигиены . 1 (1): 115–122. DOI : 10.1017 / S0022172400000097 . ISSN 0022-1724 . PMC 2235964 . PMID 20474105 .
- ^ Спенсер, Дэн (2013). Селитра: Мать Пороха . Оксфорд, Великобритания: Издательство Оксфордского университета. п. 256. ISBN 9780199695751.
- ^ Питер Уотсон (2006). Идеи: история мысли и изобретений, от огня до Фрейда . HarperCollins. п. 304. ISBN 978-0-06-093564-1. Архивировано 17 октября 2015 года.
Впервые металлическая трубка в этом контексте была использована примерно в 1280 году в войнах между Сун и монголами, где был изобретен новый термин, чонг, для описания нового ужаса ... Как бумага, он достиг Запада через Мусульмане, в данном случае сочинения андалузского ботаника Ибн аль-Байтара, который умер в Дамаске в 1248 году. Арабское название селитры - «китайский снег», а персидское использование - «китайская соль» 28.
- ^ Катал Дж. Нолан (2006). Эпоха религиозных войн, 1000–1650: энциклопедия глобальной войны и цивилизации . Том 1 энциклопедий Гринвуда о современных мировых войнах. Издательская группа "Гринвуд". п. 365. ISBN 978-0-313-33733-8. Архивировано 01 января 2014 года . Проверено 28 ноября 2011 .
В любом случае есть лингвистические свидетельства китайского происхождения технологии: в Дамаске арабы называли селитру, используемую для изготовления пороха, «китайским снегом», а в Иране - «китайской солью». Каким бы ни был миграционный маршрут
- ↑ Оливер Фредерик Гиллилан Хогг (1970). Артиллерия: ее происхождение, расцвет и упадок . Книги Архонта. п. 123. Архивировано 19 сентября 2015 года.
Китайцы, безусловно, были знакомы с селитрой, основным ингредиентом пороха.
Они назвали его «Китайский снег» и использовали его в начале христианской эры для изготовления фейерверков и ракет.
- ↑ Оливер Фредерик Гиллилан Хогг (1963). Английская артиллерия, 1326–1716 гг .: история артиллерии в этой стране до образования Королевского артиллерийского полка . Королевский артиллерийский институт. п. 42.
Китайцы, безусловно, были знакомы с селитрой, основным ингредиентом пороха.
Они назвали его «Китайский снег» и использовали его в начале христианской эры для изготовления фейерверков и ракет.
- ↑ Оливер Фредерик Гиллилан Хогг (1993). Булавы к пушке: война и оружие до введения пороха (переиздание ред.). Barnes & Noble Books. п. 216. ISBN. 978-1-56619-364-1. Проверено 28 ноября 2011 .
Китайцы, безусловно, были знакомы с селитрой, основным ингредиентом пороха. Они назвали его китайским снегом и использовали его в начале христианской эры для изготовления фейерверков и ракет.
- ^ Партингтон, JR (1960). История греческого огня и пороха (иллюстрировано, переиздание ред.). JHU Press. п. 335. ISBN 978-0801859540. Проверено 21 ноября 2014 .
- ^ Нидхэм, Джозеф; Ю, Пинг-Ю (1980). Нидхэм, Джозеф (ред.). Наука и цивилизация в Китае: Том 5, Химия и химическая технология, Часть 4, Спагирические открытия и изобретения: Аппарат, теории и дары . Том 5. Авторы Джозеф Нидхэм, Лу Гвей-Джен, Натан Сивин (иллюстрировано, перепечатано под ред.). Издательство Кембриджского университета. п. 194. ISBN 978-0521085731. Проверено 21 ноября 2014 .
- ↑ Эли С. Фриман (1957). «Кинетика термического разложения нитрата калия и реакции нитрита калия с кислородом». Варенье. Chem. Soc . 79 (4): 838–842. DOI : 10.1021 / ja01561a015 .
- ^ Сен, Судипта (2019). Ганг: Множество прошлых индийской реки . Нью-Хейвен: издательство Йельского университета. п. 318. ISBN 978-0-300-11916-9.
- ^ Рой, Кошик (2014). Военный переход в Азии раннего Нового времени, 1400-1750 гг . Лондон: Bloomsbury Academic. п. 19. ISBN 978-1-7809-3765-6.
- ↑ Ahmad Y Hassan , Нитрат калия в арабских и латинских источниках. Архивировано 26 февраля2008 г. в Wayback Machine , История науки и технологий в исламе .
- ^ Джек Келли (2005). Порох: алхимия, бомбардировки и пиротехника: история взрывчатого вещества, изменившего мир . Основные книги. п. 22. ISBN 978-0-465-03722-3. Архивировано 11 мая 2016 года.
Около 1240 года арабы узнали о селитре («китайский снег») с Востока, возможно, через Индию. Вскоре они узнали о порохе. Они также узнали о фейерверках («китайские цветы») и ракетах («китайские стрелы»). К 1280 году арабские воины обзавелись огненными копьями. Примерно в том же году сирийский по имени Хасан аль-Раммах написал книгу, в которой, как он выразился, «говорится об огненных машинах, которые можно использовать для развлечения или в полезных целях». Он говорил о ракетах, фейерверках, огненных копьях и других зажигательных веществах, используя термины, которые предполагали, что он получил свои знания из китайских источников. Он дал инструкции по очистке селитры и рецепты изготовления различных видов пороха.
- ^ Майор Джордж Рейнс (1861). Заметки о изготовлении селитры из Земли пещер . Новый Орлеан, Лос-Анджелес: Daily Delta Job Office. п. 14. Архивировано 29 июля 2013 года . Проверено 13 сентября 2012 года .
- ^ а б Джозеф ЛеКонт (1862). Инструкция по изготовлению селитры . Колумбия, Южная Каролина: Военное ведомство Южной Каролины. п. 14. Архивировано 13 октября 2007 года . Проверено 19 октября 2007 .
- ^ "Как работают холодильники" . HowStuffWorks . 2006-11-29 . Проверено 2 ноября 2018 .
- ^ Amthyst галереи, Inc архивации 2008-11-04 в Wayback Machine . Galleries.com. Проверено 7 марта 2012.
- ^ Неорганические добавки для улучшения табака Архивировано 1ноября 2007 г.в Wayback Machine , TobaccoDocuments.org
- ^ Кирст, WJ (1983). Самопотребляющиеся бумажные картриджи для перкуссионного револьвера . Миннеаполис, Миннесота: Northwest Development Co.
- ^ Бинкерд, Э. Ф; Колари, О. Э (1975-01-01). «История и использование нитратов и нитритов при консервировании мяса». Пищевая и косметическая токсикология . 13 (6): 655–661. DOI : 10.1016 / 0015-6264 (75) 90157-1 . ISSN 0015-6264 . PMID 1107192 .
- ^ «Мясная наука» , Университет Висконсина. uwex.edu.
- ^ Солонины архивации 2008-03-19 в Wayback Machine , пищевой сети
- ^ Агентство по пищевым стандартам Великобритании: «Текущие добавки, одобренные ЕС, и их номера E» . Архивировано 07.10.2010 . Проверено 27 октября 2011 .
- ^ Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США: «Список пищевых добавок, часть II» . Архивировано 8 ноября 2011 года . Проверено 27 октября 2011 .
- ^ Кодекс пищевых стандартов Австралии и Новой Зеландии «Стандарт 1.2.4 - Маркировка ингредиентов» . Проверено 27 октября 2011 .
- ^ "Готовьте чистый ганский рецепт сайта" . CookClean Ghana . Архивировано 28 августа 2013 года.
- ^ Marcellina Ulunma Okehie-Offoha (1996). Этническое и культурное разнообразие Нигерии . Трентон, Нью-Джерси: Africa World Press.
- ^ Браун, Кэтрин (2011-11-14). Год в шотландской кухне . Нил Уилсон Паблишинг Лтд. ISBN 9781906476847.
- ^ Университет штата Мичиган Расширение Bulletin E-896: NPK Удобрения архивации 2015-12-24 в Wayback Machine
- ^ Холл, Уильям L; Робарж, Уэйн П.; Встреча Американского химического общества (2004 г.). Воздействие удобрений на почву и воду на окружающую среду . п. 40. ISBN 9780841238114. Архивировано 27 января 2018 года.
- ^ «Зубная паста Sensodyne для чувствительных зубов» . 2008-08-03. Архивировано из оригинального 7 -го августа 2007 года . Проверено 3 августа 2008 .
- ^ Эномото, K; и другие. (2003). «Влияние нитрата калия и кремнезема на поверхность дентина» . Японский журнал консервативной стоматологии . 46 (2): 240–247. Архивировано из оригинала на 2010-01-11.
- ^ R. Orchardson & DG Гиллы (2006). «Управление гиперчувствительностью дентина» (PDF) . Журнал Американской стоматологической ассоциации . 137 (7): 990–8, викторина 1028–9. DOI : 10,14219 / jada.archive.2006.0321 . PMID 16803826 . Архивировано (PDF) из оригинала 29.07.2013.
- ^ Орвилл Гарри Браун (1917). Астма, представляя изложение теории непассивного выдоха . Резюме компании Мосби. п. 277 .
- ^ Джо Graedon (15 мая 2010). « „ Sensitive“зубная паста может помочь астмы» . Чикаго Трибьюн . Архивировано из оригинального 16 сентября 2011 года . Проверено 18 июня 2012 года .
- ^ МЕСТНАЯ РЕГИСТРАЦИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ ДЛЯ ЧЕЛОВЕКА (КОМБИНАТ) [ постоянная мертвая ссылка ] . fda.moph.go.th
- ^ Райхерт ET. (1880). «О физиологическом действии нитрита калия». Являюсь. J. Med. Sci . 80 : 158–180. DOI : 10.1097 / 00000441-188007000-00011 .
- ^ Адам Чаттэуэй; Роберт Дж. Данстер; Ральф Галл; Дэвид Дж. Спринг. «ОЦЕНКА НЕПИРОТЕХНИЧЕСКИХ АЭРОЗОЛЕЙ В КАЧЕСТВЕ ПОДАЧИ ПОЖАРА» (PDF) . Национальный институт стандартов и технологий США ( NIST ). Архивировано (PDF) из оригинала 29.07.2013.
- ↑ Стэн Рорк (27 февраля 2008 г.). «Удаление пней для домовладельцев» . Совместная система расширения штата Алабама . Архивировано из оригинального 23 марта 2012 года.
- ^ Дэвид Э. Тюркотт; Фрэнсис Э. Локвуд (8 мая 2001 г.). «Водный ингибитор коррозии. Примечание. В этом патенте нитрат калия упоминается как второстепенный компонент в сложной смеси. Поскольку ржавчина является продуктом окисления, это утверждение требует обоснования» . Патент США. 6,228,283. Архивировано 27 января 2018 года.
- ↑ Элизабет Марч (июнь 2008 г.). «Ученый, патент и манго - утроение урожая манго на Филиппинах» . Журнал ВОИС . Всемирная организация интеллектуальной собственности Организации Объединенных Наций ( ВОИС ). Архивировано 25 августа 2012 года.
- ^ "Филиппинский ученый получает премию Диоскоро Л. Умали 2011" . Региональный центр аспирантуры и исследований в области сельского хозяйства Юго-Восточной Азии ( SEARCA ). Архивировано из оригинального 30 ноября 2011 года.
- ^ Juan Ignacio Burgaleta; Сантьяго Ариас; Диего Рамирес. «Gemasolar, первая коммерческая термосолнечная башня с башней с системой хранения расплавленной соли» (PDF) (пресс-релиз). Torresol Energy . Архивировано из оригинального (PDF) 9 марта 2012 года . Проверено 7 марта 2012 года .
- ^ "Прямой допинг: Селитра подавляет мужской пыл?" . 1989-06-16. Архивировано 11 октября 2007 года . Проверено 19 октября 2007 .
- ^ Ричард Э. Джонс и Кристин Х. Лопес (2006). Репродуктивная биология человека, третье издание . Elsevier / Academic Press . п. 225. ISBN 978-0-12-088465-0. Архивировано 01 мая 2016 года.
- ^ "10 причин, по которым истинные американцы должны посмотреть '1776' этого 4 июля" . EW.com . Проверено 1 августа 2019 .
Библиография [ править ]
- Барнум, Деннис В. (декабрь 2003 г.). «Немного истории нитратов». Журнал химического образования . 80 (12): 1393. Bibcode : 2003JChEd..80.1393B . DOI : 10.1021 / ed080p1393 .
- Дэвид Кресси. Селитра: мать пороха (Oxford University Press, 2013), 237 стр. Онлайн-обзор Роберта Тигса.
- Алан Уильямс. «Производство селитры в средние века», Ambix , 22 (1975), стр. 125–33. Maney Publishing , ISSN 0002-6980.
Внешние ссылки [ править ]
| В Wikiquote есть цитаты, связанные с: Нитрат калия |
- Международная карта химической безопасности 018402216
| HNO 3 | Он | ||||||||||||||||
| LiNO 3 | Быть (NO 3 ) 2 | B (НЕТ3)- 4 | РОНО 2 | НЕТ- 3 NH 4 NO 3 | HOONO 2 | FNO 3 | Ne | ||||||||||
| NaNO 3 | Mg (NO 3 ) 2 | Al (NO 3 ) 3 | Si | п | S | ClONO 2 | Ar | ||||||||||
| KNO 3 | Ca (NO 3 ) 2 | СБН (NO 3 ) 3 | Ti (NO 3 ) 4 | VO (NO 3 ) 3 | Cr (NO 3 ) 3 | Mn (NO 3 ) 2 | Fe (NO 3 ) 2 Fe (NO 3 ) 3 | Co (NO 3 ) 2 Co (NO 3 ) 3 | Ni (NO 3 ) 2 | CuNO 3 Cu (NO 3 ) 2 | Zn (NO 3 ) 2 | Ga (NO 3 ) 3 | Ge | В качестве | Se | Br | Kr |
| RbNO 3 | Sr (NO 3 ) 2 | Д (НЕТ 3 ) 3 | Zr (NO 3 ) 4 | Nb | Пн | Tc | Ru (NO 3 ) 3 | Rh (NO 3 ) 3 | Pd (NO 3 ) 2 Pd (NO 3 ) 4 | AgNO 3 Ag (NO 3 ) 2 | CD (NO 3 ) 2 | В (NO 3 ) 3 | Sn (NO 3 ) 4 | Сб (NO 3 ) 3 | Te | INO 3 | Xe (NO 3 ) 2 |
| CsNO 3 | Ba (NO 3 ) 2 | Hf (NO 3 ) 4 | Та | W | Re | Операционные системы | Ir | Pt (NO 3 ) 2 Pt (NO 3 ) 4 | Au (NO 3 ) 3 | Hg 2 (NO 3 ) 2 Hg (NO 3 ) 2 | TlNO 3 Tl (NO 3 ) 3 | Pb (NO 3 ) 2 | Би (NO 3 ) 3 BiO (NO 3 ) | Po (NO 3 ) 4 | В | Rn | |
| Пт № 3 | Ра (NO 3 ) 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Ур. | Ц | Og | |
| ↓ | |||||||||||||||||
| Ла (NO 3 ) 3 | Ce (NO 3 ) 3 Ce (NO 3 ) 4 | Pr (NO 3 ) 3 | Nd (NO 3 ) 3 | PM (NO 3 ) 3 | См (NO 3 ) 3 | Eu (NO 3 ) 3 | Б-г (NO 3 ) 3 | Tb (NO 3 ) 3 | Dy (NO 3 ) 3 | Хо (нет 3 ) 3 | Er (NO 3 ) 3 | Тм (№ 3 ) 3 | Yb (NO 3 ) 3 | Лу (NO 3 ) 3 | |||
| Ac (NO 3 ) 3 | Чт (NO 3 ) 4 | PaO 2 (NO 3 ) 3 | UO 2 (NO 3 ) 2 | Np (NO 3 ) 4 | Pu (NO 3 ) 4 | Am (NO 3 ) 3 | См (NO 3 ) 3 | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||