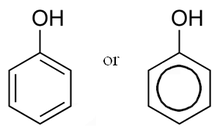
В органической химии , фенолов , иногда называемых фенольных , представляют собой класс химических соединений , состоящих из одного или нескольких гидроксильных групп (- O Н ) присоединены непосредственно к ароматической углеводородной группе. Самый простой - фенол , C
6ЧАС
5ОН . Фенольные соединения классифицируются как простые фенолы или полифенолы в зависимости от количества фенольных звеньев в молекуле.
Фенолы синтезируются промышленным способом и производятся растениями и микроорганизмами. [1]
Свойства [ править ]
Кислотность [ править ]
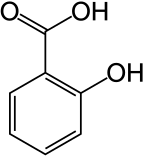
Фенолы более кислые, чем обычные спирты. Кислотность гидроксильной группы в фенолах обычно является промежуточной между кислотностью алифатических спиртов и карбоновых кислот (их pK a обычно составляет от 10 до 12). При депротонировании фенола образуется соответствующий отрицательный ион фенолята или ион феноксида , и соответствующие соли называются фенолятами или феноксидами ( арилоксидами согласно Золотой книге IUPAC ).
Конденсация с альдегидами и кетонами [ править ]
Фенолы подвержены электрофильным ароматическим заменам . Конденсация с формальдегидом дает смолистые материалы, известные как бакелит .
Другим электрофильным ароматическим замещением в промышленных масштабах является производство бисфенола А , который получают конденсацией с ацетоном . [2]
C-алкилирование алкенами [ править ]
Фенол легко алкилируется в орто-положениях с использованием алкенов в присутствии кислоты Льюиса, такой как феноксид алюминия:
- CH 2 = CR 2 + C 6 H 5 OH → R 2 CHCH 2 -2-C 6 H 4 OH
Таким способом ежегодно производится более 100 000 тонн трет-бутилфенолов (год: 2000) с использованием изобутилена (CH 2 = CMe 2 ) в качестве алкилирующего агента. Особенно важен 2,6-дитрет-бутилфенол , универсальный антиоксидант . [2]
Другие реакции [ править ]
Фенолы подвергаются этерификации . Сложные эфиры фенола - активные сложные эфиры , склонные к гидролизу. Фенолы являются химически активными веществами по отношению к окислению . Окислительное расщепление, например расщепление 1,2-дигидроксибензола до монометилового эфира 2,4-гексадиендиовой кислоты с кислородом, хлорид меди в пиридине [3] Окислительная деароматизация до хинонов, также известная как реакция Тейбера . [4] и оксон . [5] В реакции, описанной ниже, 3,4,5-триметилфенол реагирует с синглетным кислородом, образующимся из оксона / карбоната натрия.в смеси ацетонитрил / вода до пара-пероксихинола. Этот гидропероксид восстанавливается до хинола тиосульфатом натрия .
Фенолы окисляются до гидрохинонов при окислении персульфата Эльбса .
Взаимодействие нафтолов, гидразинов и бисульфита натрия в синтезе карбазола Бюхерера
Синтез [ править ]
Многие фенолы, представляющие коммерческий интерес, получают путем переработки фенола или крезолов . Они , как правило , получают путем алкилирования бензола / толуола с пропиленом с образованием кумола затем O
2добавляется с H
2ТАК
4с образованием фенола ( скакательный отросток ). В дополнение к реакциям, описанным выше, многие другие более специализированные реакции производят фенолы:
- перегруппировка сложных эфиров перегруппировка Фриса
- перегруппировка N- фенилгидроксиламинов в перегруппировке Бамбергера
- деалкилирование фенольных эфиров
- уменьшение хинонов
- замена ароматического амина на гидроксильную группу водой и бисульфидом натрия в реакции Бюхерера
- термическое разложение солей арилдиазония , соли превращаются в фенол [6]
- окислением арилсиланов - ароматической разновидностью окисления Флеминга-Тамао [7]
Классификация [ править ]
Существуют различные схемы классификации . [8] : 2 Обычно используемая схема основана на количестве атомов углерода и была разработана Джеффри Харборном и Симмондсом в 1964 году и опубликована в 1980 году: [8] : 2 [9]
| Фенол | исходное соединение, используемое в качестве дезинфицирующего средства и для химического синтеза |
| Бисфенол А | и другие бисфенолы, полученные из кетонов и фенола / крезола |
| BHT | (бутилированный гидрокситолуол) - жирорастворимый антиоксидант и пищевая добавка |
| 4-нонилфенол | продукт распада моющих средств и ноноксинола-9 |
| Ортофенил фенол | фунгицид используется для депиляции цитрусовых |
| Пикриновая кислота | (тринитрофенол) - взрывчатое вещество |
| Фенолфталеин | индикатор pH |
| Ксиленол | используется в антисептических и дезинфицирующих средствах |
Лекарства и биоактивные натуральные продукты [ править ]
| тирозин | одна из 20 стандартных аминокислот |
| L-ДОПА | пролекарство дофамина, используемое для лечения болезни Паркинсона |
| пропофол | короткое действие внутривенного анестезирующего агента |
| витамин К гидрохинон | свертывающий агент, превращающий |
| левотироксин (L-тироксин) | Самый продаваемый препарат для лечения дефицита гормонов щитовидной железы. |
| амоксициллин | Самый продаваемый антибиотик |
| эстрадиол | главный женский половой гормон |
Ссылки [ править ]
- ^ Hättenschwiler, Стефан; Витаусек, Питер М. (2000). «Роль полифенолов в круговороте питательных веществ наземных экосистем». Тенденции в экологии и эволюции . 15 (6): 238–243. DOI : 10.1016 / S0169-5347 (00) 01861-9 . PMID 10802549 .
- ^ a b Fiege H; Voges HW; Хамамото Т; Умемура S; Iwata T; Miki H; Fujita Y; Buysch HJ; Гарбе Д (2000). «Производные фенола». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a19_313 .
- ^ 2,4-Hexadienedioic acid, монометиловый эфир, (Z, Z) - Organic Syntheses , Coll. Vol. 8, p.490 (1993); Vol. 66, p.180 (1988) Статья
- ^ "2,5-Циклогексадиен-1,4-дион, 2,3,5-триметил". Органический синтез . 52 : 83.1972.
- ^ Карреньо, М. Кармен; Гонсалес-Лопес, Маркос; Урбано, Антонио (2006). «Окислительная деароматизация пара-алкилфенолов в пара-пероксихинолы и пара-хинолы, опосредованная оксоном как источником синглетного кислорода». Angewandte Chemie International Edition . 45 (17): 2737–2741. DOI : 10.1002 / anie.200504605 . PMID 16548026 .
- ^ ОН Ungnade, EF Orwoll (1943). «3-Бром-4-гидрокситолуол». Органический синтез . 23 : 11. DOI : 10,15227 / orgsyn.023.0011 .
- ^ Брейсгедл, Соня; Андерсон, Эдвард А. (2010). «Окисление арилсилана - новые пути получения гидроксилированных ароматических углеводородов» . Chem. Comm . 46 (20): 3454–6. DOI : 10.1039 / b924135c . PMID 20582346 . S2CID 31736757 .
- ^ a b Уилфред Вермеррис и Ральф Николсон. Биохимия фенольных соединений Springer, 2008 г.
- ^ Harborne, JB (1980). «Растительные фенолы». В Белле, EA; Чарлвуд, Б.В. (ред.). Энциклопедия физиологии растений, том 8 Вторичные растительные продукты . Берлин Гейдельберг Нью-Йорк: Springer-Verlag. С. 329–395.