| Имена | |||
|---|---|---|---|
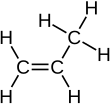
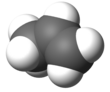
| Предпочтительное название IUPAC Пропен [1] | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100,003,693 | ||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1077 В сжиженном углеводородном газе : 1075 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 3 Н 6 | |||
| Молярная масса | 42,081 г · моль -1 | ||
| Внешность | Бесцветный газ | ||
| Плотность | 1,81 кг / м 3 , газ (1,013 бар, 15 ° C) 1,745 кг / м 3 , газ (1,013 бар, 25 ° C) 613,9 кг / м 3 , жидкость | ||
| Температура плавления | -185,2 ° С (-301,4 ° F, 88,0 К) | ||
| Точка кипения | -47,6 ° С (-53,7 ° F, 225,6 К) | ||
| 0,61 г / м 3 | |||
| -31,5 · 10 −6 см 3 / моль | |||
| Вязкость | 8,34 мкПа · с при 16,7 ° C | ||
| Структура | |||
Дипольный момент | 0,366 D (газ) | ||
| Опасности | |||
| Паспорт безопасности | Внешний паспорт безопасности материала | ||
Классификация ЕС (DSD) (устарела) | |||
| R-фразы (устаревшие) | 12 | ||
| S-фразы (устаревшие) | 9-16-33 | ||
| NFPA 704 (огненный алмаз) |  1 4 1 | ||
| точка возгорания | -108 ° С (-162 ° F, 165 К) | ||
| Родственные соединения | |||
Родственные алкены ; связанные группы | Этилен , изомеры бутилена ; Аллил , пропенил | ||
Родственные соединения | Пропан , пропин пропадиен , 1-пропанол 2-пропанол | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Пропен , также известный как пропилен или метилэтилен , представляет собой ненасыщенное органическое соединение с химической формулой . Он имеет одну двойную связь и является вторым простейшим представителем алкенового класса углеводородов . Это бесцветный газ со слабым запахом нефти [2]
Биопропилен является аналогом пропилена на биологической основе . [3] [4]
Производство [ править ]
Взлом Steam [ править ]
Доминирующей технологией производства пропилена является паровой крекинг. Та же технология применяется к этану этилену. Судя по масштабу, эти две конверсии являются процессами №2 и №1 в химической промышленности. [5] В этом процессе пропан подвергается дегидрированию . Побочный продукт - водород:
- СН 3 СН 2 СН 3 → СН 3 СН = СН 2 + Н 2
Выход пропена составляет около 85%. Побочные продукты обычно используются в качестве топлива для реакции дегидрирования пропана. Паровой крекинг - один из самых энергоемких промышленных процессов.
Исходным сырьем является нафта или пропан , особенно на Ближнем Востоке , где имеется большое количество пропана, добываемого при нефтегазовых операциях. [6] Пропен можно отделить фракционной перегонкой от углеводородных смесей, полученных в результате крекинга и других процессов нефтепереработки; Пропен нефтеперерабатывающего качества составляет от 50 до 70%. [7] В США сланцевый газ является основным источником пропана .
Технология преобразования олефинов [ править ]
В технологии конверсии триолефина или олефина Phillips пропилен взаимно превращается с этиленом и 2-бутенами. Применяются рениевые и молибденовые катализаторы: [8]
- СН 2 = СН 2 + СН 3 СН = СНСН 3 → 2 СН 2 = СНСН 3
В основе технологии лежит реакция метатезиса олефинов, открытая в компании Phillips Petroleum . [9] [10] Достигнут выход пропена около 90 мас.%.
Связанный является Метанол-к-олефинов / метанол-к-пропена процесс. Он преобразует синтез-газ (синтез-газ) в метанол , а затем преобразует метанол в этилен и / или пропен . В качестве побочного продукта процесса образуется вода. Синтез-газ производится путем реформирования природного газа или реформирования паром нефтепродуктов, таких как нафта, или путем газификации угля .
Каталитический крекинг в псевдоожиженном слое [ править ]
Каталитический крекинг с псевдоожиженным слоем высокой жесткости (FCC) использует традиционную технологию FCC в жестких условиях (более высокое отношение катализатора к маслу, более высокая скорость впрыска пара, более высокие температуры и т. Д.), Чтобы максимизировать количество пропена и других легких продуктов. В установку FCC с высокой степенью строгости обычно подают газойли (парафины) и остатки, и при этом в сырье производится около 20–25 млн.% Пропена вместе с большими объемами автомобильного бензина и побочных продуктов дистиллята.
Рынок и исследования [ править ]
Производство пропена оставалось неизменным на уровне около 35 миллионов тонн (только Европа и Северная Америка) с 2000 по 2008 год, но оно увеличивалось в Восточной Азии, особенно в Сингапуре и Китае. [11] Общее мировое производство пропена в настоящее время составляет примерно половину от производства этилена.
Было изучено использование сконструированных ферментов , но оно не имеет коммерческой ценности. [12]
Использует [ редактировать ]
Пропен - второй по важности исходный продукт в нефтехимической промышленности после этилена . Это сырье для самых разных продуктов. Производители пластикового полипропилена обеспечивают почти две трети всего спроса. [13] Конечные области применения полипропилена включают пленки, волокна, контейнеры, упаковку, а также крышки и укупорочные средства. Пропен также используется для производства важных химических веществ, таких как оксид пропилена, акрилонитрил, кумол, масляный альдегид и акриловая кислота. В 2013 году во всем мире было переработано около 85 миллионов тонн пропена. [13]
Пропен и бензол превращаются в ацетон и фенол в процессе кумола .
Пропен также используется для производства изопропанола (пропан-2-ол), акрилонитрила , оксида пропилена и эпихлоргидрина . [14] Промышленное производство акриловой кислоты включает каталитическое частичное окисление пропена. [15] Пропен также является промежуточным продуктом при одностадийном селективном окислении пропана до акриловой кислоты. [16] [17] [18] [19] В промышленности и мастерских пропен используется в качестве альтернативного топлива ацетилену при газокислородной сварке и резке , пайке и нагревании металла с целью гибки. Это стало стандартом в BernzOmatic.продукты и другие в заменителях MAPP, [20] теперь, когда настоящий газ MAPP больше не доступен.
Реакции [ править ]
Пропен напоминает другие алкен в том , что она претерпевает аддитивные реакции относительно легко при комнатной температуре. Относительная слабость его двойной связи объясняет его склонность вступать в реакцию с веществами, которые могут осуществить это преобразование. Алкеновые реакции включают: 1) полимеризацию , 2) окисление , 3) галогенирование и гидрогалогенирование , 4) алкилирование , 5) гидратацию , 6) олигомеризацию и 7) гидроформилирование .
Сжигание [ править ]
Пропен вступает в реакции горения аналогично другим алкенам . В присутствии достаточного или избыточного кислорода пропен горит с образованием воды и углекислого газа .
- 2 C 3 H 6 + 9 O 2 → 6 CO 2 + 6 H 2 O
Когда кислорода недостаточно для полного сгорания, происходит неполное сгорание, что приводит к образованию окиси углерода и / или сажи ( углерода ).
- С 3 Н 6 + 2 О 2 → 3 Н 2 О + 2 С + CO
Экологическая безопасность [ править ]
Пропен - продукт сгорания от лесных пожаров, сигаретного дыма, выхлопных газов автомобилей и самолетов. Это примесь в некоторых отопительных газах. Наблюдаемые концентрации были в диапазоне 0.1-4.8 частей на миллиард ( частей на миллиард ) в сельском воздухе, 4-10.5 частей на миллиард в городском воздухе, и 7-260 частей на миллиард в образцах промышленных воздуха. [7]
В Соединенных Штатах и некоторых европейских странах пороговое значение 500 частей на миллион ( ppm ) было установлено для профессионального воздействия (8-часовое средневзвешенное по времени ) воздействие. Он считается летучим органическим соединением (ЛОС), и его выбросы регулируются правительствами многих стран, но Агентство по охране окружающей среды США (EPA) не внесло его в список опасных загрязнителей воздуха в соответствии с Законом о чистом воздухе . При относительно коротком периоде полураспада не ожидается его биоаккумуляции. [7]
Пропен имеет низкую острую токсичность при вдыхании. Вдыхание газа может вызвать обезболивающее действие, а при очень высоких концентрациях - потерю сознания. Однако предел удушья для человека примерно в 10 раз выше (23%), чем нижний уровень воспламеняемости. [7]
Хранение и обращение [ править ]
Поскольку пропен летуч и легко воспламеняется, необходимо принимать меры, чтобы избежать опасности возгорания при обращении с газом. Если пропен загружается в какое-либо оборудование, способное вызвать возгорание, такое оборудование должно быть отключено при загрузке, разгрузке, подключении или отключении. Пропен обычно хранится в жидком виде под давлением, хотя его также можно безопасно хранить в виде газа при температуре окружающей среды в одобренных контейнерах. [21]
Фармакология [ править ]
Пропен действует как депрессант центральной нервной системы за счет аллостерического агонизма рецептора ГАМК А. Чрезмерное воздействие может привести к седации и амнезии , прогрессированию до комы и смерти по механизму, эквивалентному передозировке бензодиазепина . Преднамеренное вдыхание также может привести к смерти в результате удушья (внезапная смерть при вдыхании ).
Встречаемость в природе [ править ]
Пропен обнаружен в межзвездной среде с помощью микроволновой спектроскопии. [22] 30 сентября 2013 года НАСА также объявило, что орбитальный аппарат Кассини, входящий в миссию Кассини-Гюйгенс , с помощью спектроскопии обнаружил небольшие количества природного пропена в атмосфере Титана . [23] [24]
См. Также [ править ]
- Катастрофа в Лос-Альфакес
- Злоупотребление ингалянтами
- 2014 г. взрывы газа в Гаосюне
- Взрыв в Хьюстоне 2020
Ссылки [ править ]
- ^ "Front Matter". Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 31. DOI : 10.1039 / 9781849733069-FP001 . ISBN 978-0-85404-182-4.
- ^ «Пропилен» .
- ^ Биологически активные добавки, интеллектуальные и специальные химикаты
- ^ Duurzame bioplastics op base van hernieuwbare grondstoffen
- ^ Джованни Маггини (2013-04-17). «Экономика технологий: пропилен дегидрированием пропана, часть 3» . Slideshare.net . Проверено 12 ноября 2013 .
- ^ Словарь промышленных химикатов Эшфорда, третье издание, 2011 г., ISBN 978-0-9522674-3-0 , страницы 7766-9
- ^ a b c d «Оценка безопасности продукта (PSA): пропилен» . Dow Chemical Co. Архивировано из оригинала на 2013-06-22 . Проверено 11 июля 2011 .
- ^ Ghashghaee Мохаммад (2018). «Гетерогенные катализаторы газофазной конверсии этилена в высшие олефины». Rev. Chem. Англ . 34 (5): 595–655. DOI : 10,1515 / revce-2017-0003 . S2CID 103664623 .
- ^ Банки, RL; Бейли, GC (1964). «Диспропорционирование олефинов. Новый каталитический процесс». Исследования и разработки продуктов в области промышленной и инженерной химии . 3 (3): 170–173. DOI : 10.1021 / i360011a002 .
- ^ Лайонел Делод, Альфред Ф. Ноэлс (2005). «Метатезис». Энциклопедия химической технологии Кирка-Отмера . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 0471238961.metanoel.a01 . ISBN 978-0471238966.CS1 maint: использует параметр авторов ( ссылка )
- ^ Амгизар, Исмаэль; Vandewalle, Laurien A .; Ван Гем, Кевин М .; Марин, Гай Б. (2017). «Новые тенденции в производстве олефинов» . Инженерное дело . 3 (2): 171–178. DOI : 10.1016 / J.ENG.2017.02.006 .
- Рианна де Гусман, Дорис (12 октября 2012 г.). «Глобальная биоэнергетика в био-пропилене» . Блог зеленых химикатов .
- ^ a b «Исследование рынка: пропилен (2-е издание), Ceresana, декабрь 2014 г.» . ceresana.com . Проверено 3 февраля 2015 .
- ^ Budavari, Сьюзен, изд. (1996). «8034. Пропилен». Индекс Мерк, двенадцатое издание . Нью-Джерси: Merck & Co., стр. 1348–1349.
- ^ JGL, Fierro (ред.) (2006). Оксиды металлов, химия и применение . CRC Press. С. 414–455.CS1 maint: extra text: authors list (link)
- ^ Науманн д'Алнонкур, Рауль; Чепеи, Ленард-Иштван; Хэвекер, Майкл; Гиргсдис, Франк; Schuster, Manfred E .; Шлёгль, Роберт; Траншке, Аннетт (март 2014 г.). «Реакционная сеть в окислении пропана над фазово-чистыми оксидными катализаторами MoVTeNb M1». Журнал катализа . 311 : 369–385. DOI : 10.1016 / j.jcat.2013.12.008 . hdl : 11858 / 00-001M-0000-0014-F434-5 .
- ^ Amakawa, Кадзухико; Коленько, Юрий В .; Вилла, Альберто; Шустер, Манфред Э /; Чепеи, Ленард-Иштван; Вайнберг, Гизела; Врабец, Сабина; Науманн д'Алнонкур, Рауль; Гиргсдис, Франк; Прати, Лаура; Шлёгль, Роберт; Траншке, Аннетт (7 июня 2013 г.). «Многофункциональность кристаллических оксидных катализаторов MoV (TeNb) M1 в селективном окислении пропана и бензилового спирта». Катализ ACS . 3 (6): 1103–1113. DOI : 10.1021 / cs400010q . hdl : 11858 / 00-001M-0000-000E-FA39-1 .
- ^ Хэвекер, Майкл; Врабец, Сабина; Крёнерт, Ютта; Чепеи, Ленард-Иштван; Науманн д'Алнонкур, Рауль; Коленько, Юрий В .; Гиргсдис, Франк; Шлёгль, Роберт; Траншке, Аннетт (январь 2012 г.). «Химия поверхности фазово-чистого оксида M1 MoVTeNb при работе в режиме селективного окисления пропана до акриловой кислоты». Журнал катализа . 285 (1): 48–60. DOI : 10.1016 / j.jcat.2011.09.012 . hdl : 11858 / 00-001M-0000-0012-1BEB-F .
- ^ Csepei, Ленард-Иштван (2011). Кинетические исследования окисления пропана на Мо и катализаторов смешанного оксида на основе V . С. 3-24, 93.. DOI : 10,14279 / depositonce-2972 .
- ^ Например, "MAPP-Pro"
- ^ Энциклопедия химической технологии, четвертое издание, 1996, ISBN 0471-52689-4 (v.20), стр. 261
- ^ Марселино, N .; Cernicharo, J .; Agúndez, M .; Roueff, E .; Герин, М .; Martín-Pintado, J .; Mauersberger, R .; Тум, К. (10 августа 2007 г.). «Открытие межзвездного пропилена (CH2CHCH3): недостающие звенья в химии межзвездной газовой фазы» . Астрофизический журнал . ВГД. 665 (2): L127 – L130. DOI : 10.1086 / 521398 . S2CID 15832967 .
- ^ "Космический корабль находит пропилен на спутнике Сатурна, Титане" . UPI.com. 2013-09-30 . Проверено 12 ноября 2013 .
- ^ «Кассини находит ингредиент бытовых пластиком Сатурн луны» . Spacedaily.com . Проверено 12 ноября 2013 .