 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Имитрекс, Имигран, другие |
| AHFS / Drugs.com | Монография |
| Данные лицензии |
|
Категория беременности |
|
| Пути администрирования | Внутрь, подкожная инъекция , назальный спрей, трансдермальный электрофорез. |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетические данные | |
| Биодоступность | 15% (внутрь) / 96% (sc) |
| Связывание с белками | 14–21% |
| Метаболизм | МАО |
| Ликвидация Период полувыведения | 2,5 часа |
| Экскреция | 60% моча ; 40% кал |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| CompTox Dashboard ( EPA ) |
|
| ECHA InfoCard | 100.130.518 |
| Химические и физические данные | |
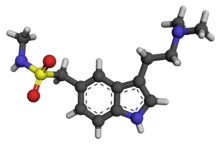
| Формула | C 14 H 21 N 3 O 2 S |
| Молярная масса | 295,40 г · моль -1 |
| 3D модель ( JSmol ) |
|
Улыбки
| |
ИнЧИ
| |
| (проверять) | |
Суматриптан , продаваемый, среди прочего, под торговой маркой Imitrex , представляет собой лекарство, используемое для лечения мигреней и кластерных головных болей . [1] Его принимают внутрь, в нос или путем инъекции под кожу . [2] Эффект обычно наступает в течение трех часов. [2]
Общие побочные эффекты включают давление в груди , усталость, рвоту, покалывание и ощущение, что мир вращается. [2] Серьезные побочные эффекты могут включать серотониновый синдром , сердечные приступы , инсульты и судороги . [2] При чрезмерном употреблении лекарств могут возникнуть головные боли . [2] Неясно, безопасно ли использование во время беременности или кормления грудью . [3] Не совсем понятно, как это работает. [2] Это препарат класса триптанов . [2]
Суматриптан был запатентован в 1982 году и одобрен для медицинского применения в 1991 году. [4] Он доступен в виде дженерика . [1] В 2017 году это было 97-е место среди наиболее часто назначаемых лекарств в Соединенных Штатах, было выписано более восьми миллионов рецептов. [5] [6] Он также доступен в виде комбинированного препарата суматриптан / напроксен .
Медицинское использование [ править ]
Суматриптан эффективен для прекращения или уменьшения интенсивности мигрени и кластерных головных болей . [7] Он наиболее эффективен, если принимать его сразу после начала боли. [7] Суматриптан в инъекциях более эффективен, чем другие препараты. [8]
Побочные эффекты [ править ]
Передозировка суматриптана может вызвать сульфгемоглобинемию - редкое состояние, при котором цвет крови меняется с красного на зеленый из-за интеграции серы в молекулу гемоглобина . [9] Если отменить суматриптан, состояние изменится в течение нескольких недель.
Серьезные сердечные события, в том числе со смертельным исходом, произошли после использования инъекции суматриптана или таблеток. Сообщенные события включали вазоспазм коронарной артерии , преходящую ишемию миокарда, инфаркт миокарда , желудочковую тахикардию и фибрилляцию желудочков (V-Fib). [10] [ необходима ссылка ]
Наиболее частыми побочными эффектами [11], о которых сообщили не менее 2% пациентов в контролируемых испытаниях суматриптана (таблетки 25, 50 и 100 мг) при мигрени, являются атипичные ощущения (парестезии и ощущение тепла / холода), о которых сообщили 4 человека. % в группе плацебо и 5-6% в группах суматриптана, о боли и других ощущениях давления (включая боль в груди) сообщили 4% в группе плацебо и 6-8% в группах суматриптана, неврологические события ( головокружение ) сообщили менее 1% в группе плацебо и менее 1–2% в группах суматриптана. Недомогание / утомляемость наблюдались менее чем в 1% группы плацебо и 2–3% группы суматриптана. Нарушение сна происходило от менее чем 1% в группе плацебо до 2% в группе суматриптана.
Механизм действия [ править ]
Суматриптан структурно подобен серотонину (5-HT) и является агонистом рецептора 5-HT (типы 5-HT 1D и 5-HT 1B [12] ) . Однако основной терапевтический эффект суматриптана заключается в его ингибировании высвобождения пептида, связанного с геном кальцитонина (CGRP), вероятно, благодаря его действию агониста рецептора 5-HT 1D / 1B . [13] Это подтверждается эффективностью недавно разработанных антагонистов CGRP и антител в профилактическом лечении мигрени. [14] Однако как агонизм 5-HT 1D / 1Bрецепторы подавляют высвобождение CGRP до конца не изучены. Считается, что CGRP вызывает сенсибилизацию ноцицептивных нейронов тройничного нерва, способствуя боли, испытываемой при мигрени. [15]
Суматриптан также снижает активность тройничного нерва , что, по-видимому, объясняет эффективность суматриптана при лечении кластерных головных болей. Было показано, что инъекционная форма препарата снимает кластерную головную боль в течение 30 минут в 77% случаев. [16]
Фармакокинетика [ править ]
Суматриптан применяется в нескольких формах: таблетки, подкожная инъекция и назальный спрей. Пероральное введение (в виде соли сукцината ) страдает плохой биодоступностью , отчасти из-за пресистемного метаболизма - некоторые из них расщепляются в желудке и кровотоке, прежде чем достигнут артерий-мишеней. Новая форма таблеток с быстрым высвобождением имеет такую же биодоступность, но максимальная концентрация достигается в среднем на 10–15 минут раньше. При инъекции суматриптан действует быстрее (обычно в течение 10 минут), но эффект длится более короткое время. Суматриптан метаболизируется в основном моноаминоксидазой А в 2- {5 - [(метилсульфамоил) метил] -индол-3-ил} уксусную кислоту.который затем конъюгируется с глюкуроновой кислотой . Эти метаболиты выводятся с мочой и желчью. Только около 3% активного препарата может быть восстановлено без изменений.
Не существует простой и прямой зависимости между концентрацией суматриптана (фармакокинетикой) как таковой в крови и его противомигренозным действием (фармакодинамикой). Этот парадокс до некоторой степени разрешается путем сравнения скорости абсорбции различных форм суматриптана, а не абсолютных количеств лекарства, которое они доставляют. [17] [18]
История [ править ]
Утверждение [ править ]
В 1991 году Glaxo получила одобрение на применение суматриптана, который был первым доступным триптаном . В Соединенных Штатах он доступен только по рецепту врача (и часто без предварительного разрешения количество ограничивается девятью в 30-дневный период). Это требование о рецепте врача также существует в Австралии. [19] Однако его можно купить без рецепта в Великобритании [20] и Швеции. [21] Было одобрено несколько лекарственных форм суматриптана, [ кем? ], включая таблетки , раствор для инъекций и назальные ингаляторы . [ необходима цитата ]
В июле 2009 года FDA США одобрило одноразовый состав суматриптана для струйных инъекций . Устройство вводит 6 мг суматриптана подкожно без использования иглы. Автоинжекторы с иглами уже несколько лет были доступны в Европе и Северной Америке. [22]
Исследования фазы III с использованием ионтофоретического трансдермального пластыря (Zelrix / Zecuity) начались в июле 2008 года. [23] В этом пластыре используется низкое напряжение, контролируемое предварительно запрограммированным микрочипом, для доставки разовой дозы суматриптана через кожу в течение 30 минут. [24] [25] Zecuity был одобрен FDA США в январе 2013 года. [26] Продажи Zecuity были прекращены после сообщений о ожогах и раздражении кожи. [27]
Дженерики [ править ]
Патенты Glaxo на суматриптан истекли в феврале 2009 года. В то время Imitrex продавался по цене около 25 долларов за таблетку. [28] 6 ноября 2008 г. Par Pharmaceutical объявила, что немедленно приступит к поставкам дженериков суматриптана для инъекций (инъекция суматриптана сукцината), стартовых наборов на 4 и 6 мг и картриджей для шприцев на 4 и 6 мг. Кроме того, Par планирует запустить в начале 2009 г. флаконы по 6 мг [29].
Mylan Laboratories Inc. , Ranbaxy Laboratories , Sandoz (дочерняя компания Novartis ), Dr. Reddy's Laboratories и другие компании получили одобрение FDA на генерические версии таблеток суматриптана в дозах 25, 50 и 100 мг с 2009 года. Препарат в общем доступен на рынках США и Европы, поскольку в этих юрисдикциях истек срок действия патентной защиты Glaxo. Суматриптан в виде назального спрея также широко доступен. [30]
Правовой статус [ править ]
В России разновидности суматриптана, не зарегистрированные в Национальном реестре лекарственных средств, могут рассматриваться как наркотические средства (производные диметилтриптамина ). [31]
Ссылки [ править ]
- ^ a b Британский национальный формуляр: BNF 76 (76 изд.). Фармацевтическая пресса. 2018. с. 474. ISBN 9780857113382.
- ^ a b c d e f g "Суматриптан Монография для профессионалов" . Drugs.com . Американское общество фармацевтов систем здравоохранения . Дата обращения 3 марта 2019 .
- ^ «Использование суматриптана во время беременности» . Drugs.com . Дата обращения 3 марта 2019 .
- ^ Фишер, Джнос; Ганеллин, С. Робин (2006). Открытие лекарств на основе аналогов . Джон Вили и сыновья. п. 531. ISBN. 9783527607495.
- ^ «Топ 300 2020» . ClinCalc . Проверено 11 апреля 2020 .
- ^ «Суматриптан - Статистика употребления наркотиков» . ClinCalc . Проверено 11 апреля 2020 .
- ^ а б Дерри, CJ; Дерри, S; Мур, РА (28 мая 2014 г.). «Суматриптан (все способы введения) при острых приступах мигрени у взрослых - обзор Кокрановских обзоров» . Кокрановская база данных систематических обзоров . 5 (5): CD009108. DOI : 10.1002 / 14651858.CD009108.pub2 . PMC 6469574 . PMID 24865446 .
- ^ Dahlöf, Карл GH «Суматриптан: фармакологическая основа и клинические результаты» . Medscape . Архивировано 17 февраля 2017 года . Проверено 16 июля 2016 .
- ^ "Пациент истекает темно-зеленой кровью" . BBC News . 8 июня 2007 года. Архивировано 5 августа 2010 года . Проверено 6 марта 2010 года .
- ↑ Келли К.М. (июнь 1995 г.). «Остановка сердца после применения суматриптана». Неврология . 45 (6): 1211–3. DOI : 10,1212 / wnl.45.6.1211 . PMID 7783891 . S2CID 35168945 .
- ^ «Таблетки» . fda.gov . Проверено 19 февраля 2018 .
- ^ Razzaque Z, Heald MA, Pickard JD и др. (1999). «Сужение сосудов в изолированных средних менингеальных артериях человека: определение вклада активации 5-HT1B- и 5-HT1F-рецепторов» . Br J Clin Pharmacol . 47 (1): 75–82. DOI : 10.1046 / j.1365-2125.1999.00851.x . PMC 2014 192 . PMID 10073743 .
- ^ Юхас, G; Жомбок, Т; Jakab, B; Немет, Дж; Szolcsanyi, J; Багды, Г. (26 июня 2016 г.). «Суматриптан вызывает параллельное снижение в плазме концентрации пептидов, связанных с геном кальцитонина (CGRP), и мигрень во время приступа мигрени, индуцированного нитроглицерином». Цефалгия . 25 (3): 179–183. DOI : 10.1111 / j.1468-2982.2005.00836.x . PMID 15689192 . S2CID 13007101 .
- ^ Цо, Эми R .; Гоудсби, Питер Дж. (1 августа 2017 г.). "Моноклональные антитела против CGRP: новая эра профилактики мигрени?" . Современные варианты лечения в неврологии . 19 (8): 27. DOI : 10.1007 / s11940-017-0463-4 . ISSN 1092-8480 . PMC 5486583 . PMID 28653227 .
- ^ Гиниатуллин, Рашид; Нистри, Андреа; Фаббретти, Эльза (1 февраля 2008 г.). «Молекулярные механизмы сенсибилизации рецепторов P2X3, вызывающих боль, медиаторами мигрени CGRP и NGF». Молекулярная нейробиология . 37 (1): 83–90. DOI : 10.1007 / s12035-008-8020-5 . ISSN 0893-7648 . PMID 18459072 . S2CID 25689799 .
- ^ «Лечение острой кластерной головной боли суматриптаном. Группа изучения кластерной головной боли суматриптана». N Engl J Med . 325 (5): 322–6. 1991. DOI : 10,1056 / NEJM199108013250505 . PMID 1647496 .
- Перейти ↑ Fox, AW (2004). «Начало действия агонистов 5-HT1B / 1D: модель с фармакокинетической проверкой». Головная боль . 44 (2): 142–147. DOI : 10.1111 / j.1526-4610.2004.04030.x . PMID 14756852 . S2CID 25587940 .
- ^ Freidank-Mueschenborn, E .; Фокс, А. (2005). «Разрешение различий концентрация-ответ в начале эффекта между подкожным и пероральным суматриптаном». Головная боль . 45 (6): 632–637. DOI : 10.1111 / j.1526-4610.2005.05129a.x . PMID 15953294 . S2CID 20755695 .
- ^ «Стандарт ядов, июнь 2017» . 18 мая 2017. Архивировано 31 июля 2017 года . Проверено 22 июля 2017 года .
- ^ «Пресс-релиз: появилась первая безрецептурная таблетка от мигрени» . Агентство по регулированию лекарственных средств и товаров медицинского назначения. Архивировано из оригинала на 5 декабря 2014 года . Проверено 28 января 2015 .
- ^ Европейское агентство по лекарственным средствам (23 ноября 2011 г.). «Отчет об оценке: Суматриптан Галфарм в таблетках 50 мг» (PDF) . Европейское агентство по лекарственным средствам. п. 20. Архивировано 7 января 2016 года (PDF) . Проверено 28 января 2015 .
- ^ Брандес, J .; Cady, R .; Freitag, F .; Smith, T .; Chandler, P .; Fox, A .; Linn, L .; Фарр, С. (2009). «Безыгольный подкожный суматриптан (Sumavel DosePro): биоэквивалентность и простота применения». Головная боль . 49 (10): 1435–1444. DOI : 10.1111 / j.1526-4610.2009.01530.x . PMID 19849720 . S2CID 25696109 .
- ^ Номер клинического испытания NCT00724815 "Эффективность и переносимость пластыря NP101 в лечении острой мигрени (NP101-007)" на сайте ClinicalTrials.gov
- ^ "SmartRelief - доставка лекарств с помощью электроники (ионтофорез)" . nupathe.com . Архивировано 7 января 2016 года . Проверено 19 февраля 2018 .
- ^ Пирс, М; Марбери, Т; О'Нил, К; Сигель, S; Du, W; Себри, Т. (2009). «Zelrix: новый трансдермальный препарат суматриптана» . Головная боль . 49 (6): 817–25. DOI : 10.1111 / j.1526-4610.2009.01437.x . PMID 19438727 . S2CID 205683188 .
- ^ «Zecuity одобрен FDA для лечения острой мигрени» . nupathe.com . Архивировано 7 января 2016 года . Проверено 19 февраля 2018 .
- ^ «Тева тянет мигрень патча Zecuity на сообщения горения, рубцевание | FiercePharma» . www.fiercepharma.com . Архивировано 21 марта 2017 года . Проверено 10 апреля 2017 года .
- ^ "GlaxoSmithKline пытается обмануть страдающих мигренью дымом и зеркалами Treximet" . Катализатор сообщества. 24 апреля 2008 . Проверено 22 марта 2019 .
- ^ «Par Pharmaceutical начинает поставки суматриптана для инъекций» . Par Pharmaceutical . 6 ноября 2008 года Архивировано из оригинала 10 декабря 2008 . Проверено 25 ноября 2008 года .
- ^ LaMattina, Джон (2 марта 2015). «Если вы хотите сделать хорошее лекарство отличным, необходимо учитывать его стоимость» . Forbes . Архивировано 14 февраля 2017 года . Проверено 13 февраля +2017 .
- ^ "Постановление Правительства РФ от 30 июня 1998 г. N 681" Об утверждении перечня наркотических средств, психотропных веществ и их прекурсоров, иммунных контролю в Российской Федерации "(с изменениями и дополнениями)" (на русском языке). Гарант . Проверено 28 апреля 2019 .
ДМТ (диметилтриптамин) и его производные, за исключением производных, включенных в качестве самостоятельных позиций в перечень
Внешние ссылки [ править ]
- «Суматриптан» . Информационный портал о наркотиках . Национальная медицинская библиотека США.