 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | ЗОНСТВЕННОСТЬ |
| Другие имена | SCH-530348 |
| Данные лицензии | |
| Пути администрирования | Устный |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетические данные | |
| Биодоступность | ~ 100% [1] |
| Связывание с белками | ≥99% |
| Метаболизм | печеночный ( CYP3A4 и CYP2J2 ) |
| Ликвидация Период полураспада | 5–13 дней |
| Экскреция | кал (58%), моча (25%) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| ChemSpider | |
| UNII | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard | 100.116.767 |
| Химические и физические данные | |
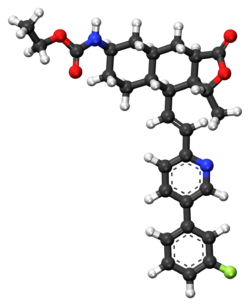
| Формула | C 29 H 33 F N 2 O 4 |
| Молярная масса | 492,591 г · моль -1 |
| 3D модель ( JSmol ) | |
| Температура плавления | 278 ° С (532 ° F) |
| |
ИнЧИ
| |
| | |
Vorapaxar (торговая марка Zontivity , ранее известная как SCH 530348 ) представляет собой антагонист рецептора тромбина ( рецептор , активируемый протеазой , PAR-1) на основе природного продукта химбацина , открытого Schering-Plough и разработанного Merck & Co. [2]
Медицинское использование [ править ]
Vorapaxar используется для людей с историей инфаркта миокарда (сердечного приступа) или людей с заболеванием периферических артерий . Исследования показали, что этот препарат может снизить частоту комбинированной конечной смерти от сердечно-сосудистых заболеваний, инфаркта миокарда, инсульта и неотложной коронарной реваскуляризации. [1]
Противопоказания [ править ]
Ворапаксар противопоказан людям с инсультом, преходящей ишемической атакой или внутримозговым кровоизлиянием. [1] В исследованиях ворапаксара на лицах, перенесших ишемический инсульт, был отмечен повышенный риск внутричерепного кровоизлияния без улучшения основных сосудистых событий. Ворапаксар обладает длительным периодом полураспада, что является проблемой, поскольку в настоящее время не существует лечения, которое бы обращало антиагрегантные эффекты ворапаксара. [1]В связи с этим важно не применять ворапаксар у лиц с инсультом, транзиторной ишемической атакой, внутричерепным кровоизлиянием или активным патологическим кровотечением в анамнезе. Это семейство лекарств, антагонистов PAR-1, в целом было связано с повышенным риском внутричерепного кровотечения, продемонстрированным объединенным анализом данных, в котором изучались 42000 пациентов с тромботическим сосудистым заболеванием или острым коронарным синдромом в анамнезе, сравнивая лекарство и плацебо. [3]
Взаимодействие с лекарствами [ править ]
Ворапаксар выводится в первую очередь за счет метаболизма ферментов CYP3A. Лучше избегать любых сильных ингибиторов CYP3A4 (например, кетоконазола, итраконазола, позаконазола, кларитромицина, нефазодона, ритонавира, саквинавира, нелфинавира, индинавира, боцепревира, телапревира, телитромицина и конивапревира). Также следует избегать индукторов CYP3A4 (карбамазепин, рифампин, зверобой и фенитоин). [1]
Корректировка дозы [ править ]
У пациентов с почечной недостаточностью коррекции дозы не требуется. [1] У пациентов с печеночной недостаточностью легкой и средней степени тяжести коррекции дозы не требуется. Если у человека тяжелая печеночная недостаточность, ворапаксар не рекомендуется из-за риска кровотечения. [1]
Механизм действия [ править ]
Ворапаксар - это новый антитромбоцитарный препарат, который является частью семейства антагонистов PAR-1, нового класса антитромбоцитарных препаратов. Он действует путем ингибирования агрегации тромбоцитов, связанной с тромбином. Этот механизм работает по другому пути, чем другие антиагрегантные препараты, такие как аспирин и ингибиторы P2Y12. В отличие от многих других лекарств, ворапаксар не влияет на АДФ-опосредованную агрегацию тромбоцитов, параметры коагуляции или время кровотечения. [4]
Хранилище [ править ]
Vorapaxar можно хранить при 20-25 ° C (68-77 ° F). Лучше всего хранить ворапаксар в оригинальной упаковке с плотно закрытым флаконом и во избежание попадания влаги. [1]
История [ править ]
В январе 2011 года клинические испытания, проводимые Merck, были остановлены для пациентов с инсультом и легкими сердечными заболеваниями из-за учащения мозговых кровотечений. [5] В рандомизированном двойном слепом исследовании, в котором ворапаксар сравнивался с плацебо в дополнение к стандартной терапии у 12 944 пациентов с острыми коронарными синдромами, не было значительного снижения комбинированной конечной точки смерти от сердечно-сосудистых причин, инфаркта миокарда, инсульта, рецидивов. ишемия с повторной госпитализацией или срочная коронарная реваскуляризация. Однако был повышенный риск сильного кровотечения. [6]В исследовании, опубликованном в феврале 2012 года, не было обнаружено никаких изменений в смертности от всех причин, при этом снизился риск сердечной смерти и увеличился риск большого кровотечения, включая внутричерепные кровоизлияния. Через два года комиссия по мониторингу данных и безопасности рекомендовала прекратить прием исследуемого препарата у людей с инсультом в анамнезе из-за риска внутричерепного кровоизлияния.
Исследование ворапаксара TRA 2 ° P – TIMI 50 проводилось на пациентах, которые ранее перенесли сердечный приступ, инсульт или заболевание периферических артерий (ЗПА). В этом трехлетнем исследовании с участием более 26000 пациентов добавление ворапаксара к стандарту лечения (аспирин и / или антагонист АДФ, такой как клопидогрель) значительно снизило риск основной комбинированной конечной точки сердечно-сосудистой смерти, сердечного приступа, инсульта или неотложной помощи. коронарная реваскуляризация на 12 процентов по сравнению с плацебо плюс стандартное лечение (11,2 процента против 12,4 процента, p = 0,001). Ворапаксар показал наиболее многообещающий результат среди пациентов с сердечным приступом в анамнезе. Среди этих пациентов препарат снизил относительный риск смерти от сердечно-сосудистых заболеваний, сердечного приступа или инсульта на 20 процентов. Было усиление умеренного или сильного кровотечения,но нет статистически значимого увеличения смертельного кровотечения.[7] Ворапаксар был рекомендован для одобрения FDA 15 января 2014 г. [8]
5 мая 2014 г. ворапаксар получил одобрение FDA.
Ссылки [ править ]
- ^ a b c d e f g h «ZONTIVITY ™ (ворапаксар), таблетки 2,08 мг, для перорального применения. Полная информация по назначению» (PDF) . Merck & Co., Inc. Первоначальное одобрение в США: 05/2014 . Проверено 17 июня 2014 года .
- ^ Chackalamannil S; Ван Ю; Гринли WJ; Hu Z; Xia Y; Ahn HS; Boykow G; Hsieh Y; Palamanda J; Аганс-Фантуцци Дж; Kurowski S; Graziano M; Чинтала М. Открытие нового перорально активного антагониста тромбиновых рецепторов на основе химбацина (SCH 530348) с сильной антиагрегантной активностью. Журнал медицинской химии 2008, 51, 3061–3064.
- ^ Морроу, Дэвид А. и Марк Дж. Альбертс. «Эффективность и безопасность Vorapaxar у пациентов с предшествующим ишемическим инсультом». Журнал Американской кардиологической ассоциации (2013): 691-98. Американская Ассоциация Сердца. Интернет. 2 ноября 2014 г. < http://stroke.ahajournals.org/content/44/3/ 691.full.pdf + html>.
- ^ Бейкер, Северная Каролина; Липински, MJ; Лермюзье, Т; Ваксман, Р. (7 октября 2014 г.). «Обзор заседания консультативного комитета по сердечно-сосудистым и почечным препаратам при администрации пищевых продуктов и медикаментов по ворапаксару в 2014 году» . Тираж . 130 (15): 1287–94. DOI : 10.1161 / cycleaha.114.011471 . PMID 25287768 .
- ^ Мерк крови Разбавитель Исследования Halted в Select Пациентов , Bloomberg News , 13 января 2011
- ^ Tricoci; и другие. (2012). «Антагонист тромбиновых рецепторов Vorapaxar при острых коронарных синдромах». Медицинский журнал Новой Англии . 366 (1): 20–33. DOI : 10.1056 / NEJMoa1109719 . hdl : 2445/49763 . PMID 22077816 .
- ^ Морроу Д.А., Браунвальд Е, Бонаца М.П., Ameriso С.Ф., Долби AJ, Рыба МП, Фокс К.А., Липка LJ, Лю Х, Николау JC, Ophuis AJ, Paolasso Е, Scirica Б. М., спинар Дж, Теру Р, Wiviott С.Д., Strony Дж., Мерфи С.А., Руководящий комитет TRA 2P – TIMI 50 и следователи (12 апреля 2012 г.). «Vorapaxar во вторичной профилактике атеротромботических событий» (PDF) . Медицинский журнал Новой Англии . 366 (15): 1404–13. DOI : 10.1056 / NEJMoa1200933 . ЛВП : 10447/94482 . PMID 22443427 .
- ^ «Заявление компании Merck о консультативном комитете FDA для Vorapaxar, исследовательской антитромбоцитарной медицины Merck» . Merck . Проверено 16 января 2014 года .
Внешние ссылки [ править ]
- Стю Борман (2005). «Надежды на лекарства-кандидаты: исследователи раскрывают новые потенциальные лекарства от тромбоза, тревоги, диабета и рака» . Новости химии и машиностроения . 83 (16): 40–44. DOI : 10.1021 / СЕН-v083n016.p040 .