 | |
 | |
| Клинические данные | |
|---|---|
| Код УВД |
|
| Легальное положение | |
| Легальное положение |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| ECHA InfoCard | 100.164.420 |
| Химические и физические данные | |
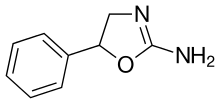
| Формула | C 9 H 10 N 2 O |
| Молярная масса | 162,192 г · моль -1 |
| 3D модель ( JSmol ) | |
| Хиральность | Рацемическая смесь |
| |
| |
| (проверять) | |
Аминорекс ( Menocil , Apiquel , aminoxaphen , aminoxafen , MCN-742 ) является потерей веса ( анорексия ) стимулятор препарата . Его сняли с продажи после того, как было установлено, что он вызывает легочную гипертензию . [1] В США это запрещенный препарат из Списка I. Это означает, что он имеет высокий потенциал злоупотребления, недопустимое медицинское использование и плохой профиль безопасности.
Аминорекс, относящийся к классу 2-амино-5-арилоксазолина, был разработан McNeil Laboratories в 1962 году. [2] Он тесно связан с 4-метиламинорексом . Аминорекс был показан, опорно - двигательный аппарат стимулирующего эффекта, лежащим на полпути между декстроамфетамин и метамфетамин . Эффекты аминорекса связывают с высвобождением катехоламинов . [3] Он может вырабатываться как метаболит левамизола , лекарства от гельминтов , который иногда используется в качестве режущего агента незаконно производимого кокаина . [4] [5]
История [ править ]
Он был обнаружен в 1962 году Эдвард Джон Hurlburt , [6] и был быстро найден в 1963 году , чтобы иметь аноректических эффект у крыс . Он был введен как средство подавления аппетита по рецепту в Германии , Швейцарии и Австрии в 1965 году, но был отменен в 1972 году после того, как было обнаружено, что он вызывает легочную гипертензию примерно у 0,2% пациентов и был связан с рядом смертей. [3] [7]
Синтез [ править ]
Впервые о синтезе сообщалось в исследовании взаимосвязи структура-активность 2-амино-5-арил-2-оксазолинов, в котором аминорекс оказался примерно в 2,5 раза более эффективным, чем сульфат D- амфетамина, в индукции анорексии у крыс, а также Сообщается, что обладает стимулирующим действием на ЦНС.
Рацемический синтез включает в себя добавление / реакцию циклизации 2-амино-1-фенилэтанола с цианогенбромидом . [8] Аналогичный синтез был также опубликован. [9] В поисках более дешевого синтетического пути немецкая группа разработала альтернативный путь [10], который с использованием хирального оксида стирола позволяет получить энантиочистый продукт.
См. Также [ править ]
- 4-Метиламинорекс
- Кломинорекс
- Циклазодон
- Фенозолон
- Флуминорекс
- Пемолин
- Тозалинон
Ссылки [ править ]
- ^ Gaine SP, Рубин LJ, Kmetzo JJ, Палевский HI, Traill TA (ноябрь 2000). «Рекреационное применение аминорекса и легочной гипертензии» . Сундук . 118 (5): 1496–7. DOI : 10,1378 / chest.118.5.1496 . PMID 11083709 . Архивировано из оригинала на 2013-01-12.
- ^ US 3161650 , «2-амино-5-арилоксазолиновые продукты»
- ^ a b Фишман А.П. (Январь 1991 г.). «Аминорекс фен / фен - предсказанная эпидемия» . Тираж . 99 (1): 156–161. DOI : 10.1161 / 01.CIR.99.1.156 . ISSN 0009-7322 . PMID 9884392 .
- ↑ Ho EN, Leung DK, Leung GN, Wan TS, Wong AS, Wong CH, Soma LR, Rudy JA, Uboh C, Sams R (апрель 2009 г.). «Аминорекс и рексамино как метаболиты левамизола у лошади». Analytica Chimica Acta . 638 (1): 58–68. DOI : 10.1016 / j.aca.2009.02.033 . PMID 19298880 .
- Перейти ↑ Bertol E, Mari F, Milia MG, Politi L, Furlanetto S, Karch SB (июль 2011 г.). «Определение аминорекса в образцах мочи человека с помощью ГХ-МС после использования левамизола». Журнал фармацевтического и биомедицинского анализа . 55 (5): 1186–9. DOI : 10.1016 / j.jpba.2011.03.039 . PMID 21531521 .
- ^ US 3115494 , "2-амино-5,6-дигидро-4ii-1,3-оксазины и способ их получения"
- ^ Вейгл, DS (июнь 2003). «Фармакологическая терапия ожирения: прошлое, настоящее, будущее» . Журнал клинической эндокринологии и метаболизма . 88 (6): 2462–9. DOI : 10.1210 / jc.2003-030151 . PMID 12788841 .
- ^ Поос GI, Carson JR, Rosenau JD, Roszowski А.П., Kelley Н.М., McGowin J (май 1963 г.). «2-амино-5-арил-2-оксазолины. Новые сильнодействующие аноректические агенты». Журнал медицинской химии . 6 (3): 266–272. DOI : 10.1021 / jm00339a011 . PMID 14185981 .
- ↑ Ueda S, Terauchi H, Yano A, Ido M, Matsumoto M, Kawasaki M (январь 2004 г.). «Производные 4,5-дизамещенного-1,3-оксазолидин-2-имина: новый класс пероральных биодоступных ингибиторов синтазы оксида азота». Биоорг. Med. Chem. Lett . 14 (2): 313–316. DOI : 10.1016 / j.bmcl.2003.11.010 . PMID 14698148 .
- ^ DE Патент 2101424 Получение 2-амино-5-фенил-2-оксазолина