 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК дигидрофосфат аммония | |
| Другие имена моноаммонийфосфат | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.028.877 |
| Номер ЕС |
|
| Номер E | E342 (i) (антиоксиданты, ...) |
PubChem CID | |
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| H 6 N O 4 P | |
| Молярная масса | 115,025 г · моль -1 |
| Внешность | белые кристаллы |
| Запах | никто |
| Плотность | 1,80 г / см 3 |
| Температура плавления | 190 ° С (374 ° F, 463 К) |
| (г / дл ) 28 (10 ° C) 36 (20 ° C) 44 (30 ° C) 56 (40 ° C) 66 (50 ° C) 81 (60 ° C) 99 (70 ° C) 118 (80 ° C) 173 (100 ° C) [2] [3] | |
| Растворимость | не растворим в этаноле [2] нерастворим в ацетоне |
Показатель преломления ( n D ) | 1,525 |
| Структура | |
| четырехугольный | |
| Термохимия | |
Std энтальпия формации (Δ F H ⦵ 298 ) | -1445,07 кДж / моль [4] |
| Опасности | |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
Формулировки опасности GHS | H319 |
Меры предосторожности GHS | Р261 , Р264 , Р271 , Р280 , Р302 + 352 , Р304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , Р405 , Р501 |
| NFPA 704 (огненный алмаз) |  1 0 0 |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 5750 мг / кг (крыса, перорально) |
| Родственные соединения | |
Другие анионы | Фосфат аммония Фосфат диаммония |
Другие катионы | Мононатрий фосфат Дигидрофосфат калия |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
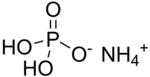
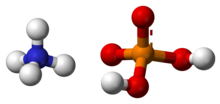
Дигидрофосфат аммония ( ADP ), также известный как моноаммонийфосфат ( MAP ) [5], представляет собой химическое соединение с химической формулой (NH 4 ) (H 2 PO 4 ). ADP является основным ингредиентом сельскохозяйственных удобрений [6] и некоторых огнетушителей . Он также широко используется в оптике [7] и электронике . [8]
Химические свойства [ править ]
Моноаммонийфосфат растворим в воде и кристаллизуется из нее в виде безводной соли в тетрагональной системе, в виде удлиненных призм или игл. [7] Практически не растворяется в этаноле . [2]
На практике твердый моноаммонийфосфат можно считать стабильным при температурах до 200 ° C, когда он разлагается на газообразный аммиак NH.
3и расплав фосфорной кислоты H
3PO
4. [9] При 125 ° C парциальное давление аммиака составляет 0,05 мм рт. [10]
Раствор стехометрического моноаммонийфосфата кислый ( pH 4,7 при концентрации 0,1%, 4,2 при 5%). [11]
Подготовка [ править ]
Моноаммонийфосфат получают в промышленных масштабах путем экзотермической реакции фосфорной кислоты и аммиака в правильных пропорциях: [12]
- NH
3+ H
3PO
4→ NH
6PO
4
Затем кристаллический MAP выпадает в осадок.
Использует [ редактировать ]
Сельское хозяйство [ править ]
Наибольшее массовое использование моноаммонийфосфата используется в сельском хозяйстве в качестве ингредиента удобрений. Она поставляет почву с элементами азотом и фосфором в форме , пригодные растениями. Его этикетка NPK - 12-61-0 (12-27-0), что означает, что он содержит 12% по весу элементарного азота и (номинально) 61% пентоксида фосфора P.
2О
5, или 27% элементарного фосфора.
Огнетушители [ править ]
Это соединение также входит в состав порошка ABC в некоторых сухих химических огнетушителях .
Оптика [ править ]
Моноаммонийфосфат - широко используемый кристалл в области оптики из-за его свойств двойного лучепреломления . Благодаря своей тетрагональной кристаллической структуре этот материал имеет отрицательную одноосную оптическую симметрию с типичными показателями преломления n o = 1,522 и n e = 1,478 в оптических длинах волн. [7]
Электроника [ править ]
Моноаммониевая кристаллы фосфата являются пьезоэлектрической , свойство требуется в некоторых активных гидроакустических преобразователях (альтернативные датчики существа , которые используют магнитострикцию ). В 1950-х годах кристаллы ADP в значительной степени вытеснили кристаллы кварца и соли Рошеля в преобразователях, поскольку с ними легче работать, чем с кварцем, и, в отличие от соли Рошель, они не растворяются . [8]
Игрушки [ править ]
Будучи относительно нетоксичным [ необходима ссылка ] , MAP также является популярным веществом для выращивания кристаллов в развлекательных целях, поскольку продается в виде игрушечных наборов, смешанных с красителями различных цветов.
Естественное явление [ править ]
Соединение встречается в природе как редкий минерал бифосфаммит. Он образуется в отложениях гуано. [13] [14] Родственное соединение, являющееся аналогом одноатомного водорода, представляет собой еще более дефицитный фосфаммит [15] https://www.ima-mineralogy.org/Minlist.htm
Ссылки [ править ]
- ^ Лиде, Дэвид Р. (1998). Справочник по химии и физике (87 изд.). Бока-Ратон, Флорида: CRC Press. С. 4–40. ISBN 0-8493-0594-2.
- ^ a b c Децзюн Сюй, Син Сюн, Линь Ян, Чжие Чжан и Синьлун Ван (2016): «Определение растворимости дигидрофосфата аммония в системе вода-этанол при различных температурах от 283,2 до 343,2 К». Журнал химических инженерных данных , том 61, выпуск 1, страницы 78–82. DOI : 10.1021 / acs.jced.5b00224
- ^ Химическая книга: « Дигидрофосфат аммония ». Проверено 14 августа 2018 г.
- ^ Национальное бюро стандартов. Избранные значения химико-термодинамических свойств. Техническое примечание 270-3. 1968 [1]
- ^ "Моноаммонийфосфат (MAP)" (PDF) . www.mosaicco.com . Дата обращения 5 июня 2015 .
- ^ IPNI. «Моноаммонийфосфат (МАФ)» (PDF) . www.ipni.net . Международный институт питания растений . Проверено 21 июля 2014 года .
- ^ a b c Амнон Ярив, Почи Йех (1984). Оптические волны в кристаллах . Wiley, Inc.
- ^ a b Виллем Хакманн (1984). Ищи и ударяй: сонар, противолодочная война и Королевский флот, 1914–1954 . Канцелярия Ее Величества. ISBN 0-11-290423-8.
- ^ Г.О. Геррант и Д.Е. Браун (196): «Термическое разложение удобрений с высоким уровнем анализа на основе фосфата аммония». Журнал сельскохозяйственной и пищевой химии , том 13, выпуск 6, страницы 493-497. DOI : 10.1021 / jf60142a002
- ↑ Джон Р. Ван Вазер (1958). Фосфор и его соединения - Том I: Химия . Нью-Йорк: Interscience Publishers, Inc., стр. 503.
- ^ Haifa Chemicals Ltd.: " Моноаммонийфосфат 12-61-0 ". Информационный бюллетень о продукте, по состоянию на 13 августа 2018 г.
- ^ Мартин Бекман, Мартин Gunnarsson, Линни Коллберг, Мартин Мюллер, и Саймон Tallvod (2016): « Производство аммофоса в Yara AB архивного 18 ноября 2017 года в Wayback Machine ». Технический отчет, Лундский университет.
- ^ https://www.mindat.org/min-678.html
- ^ https://www.ima-mineralogy.org/Minlist.htm
- ^ https://www.mindat.org/min-3197.html