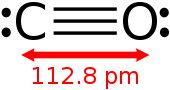 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Монооксид углерода | |||
| Другие имена Монооксид углерод оксид углеродсодержащего углерод оксид (II) , карбонильные дымовые газы Окись | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| 3587264 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.010.118 | ||
| Номер ЕС |
| ||
| 421 | |||
| КЕГГ | |||
| MeSH | Углерод + монооксид | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1016 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| CO | |||
| Молярная масса | 28,010 г / моль | ||
| Внешность | бесцветный газ | ||
| Запах | без запаха | ||
| Плотность | 789 кг / м 3 , жидкость 1,250 кг / м 3 при 0 ° C, 1 атм 1,145 кг / м 3 при 25 ° C, 1 атм | ||
| Температура плавления | -205,02 ° С (-337,04 ° F, 68,13 К) | ||
| Точка кипения | -191,5 ° С (-312,7 ° F, 81,6 К) | ||
| 27,6 мг / л (25 ° С) | |||
| Растворимость | растворим в хлороформе , уксусной кислоте , этилацетате , этаноле , гидроксиде аммония , бензоле | ||
Константа закона Генри ( k H ) | 1,04 атм · м 3 / моль | ||
Магнитная восприимчивость (χ) | −9,8 · 10 −6 см 3 / моль | ||
Показатель преломления ( n D ) | 1.0003364 | ||
Дипольный момент | 0,122 Д | ||
| Термохимия | |||
Теплоемкость ( C ) | 29,1 Дж / (К · моль) | ||
Стандартная мольная энтропия ( S | 197,7 Дж / (моль · К) | ||
Std энтальпия формации (Δ F H ⦵ 298 ) | -110,5 кДж / моль | ||
Std энтальпии сгорания (Δ с Н ⦵ 298 ) | -283,4 кДж / моль | ||
| Фармакология | |||
Код УВД | V04CX08 ( ВОЗ ) | ||
| Опасности | |||
| Паспорт безопасности | См .: страницу данных ICSC 0023 | ||
| Пиктограммы GHS | |||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H220 , H331 , H360 , H372 | ||
Меры предосторожности GHS | Р201 , Р202 , Р210 , Р260 , Р261 , Р264 , Р270 , Р271 , Р281 , Р304 + 340 , P308 + 313 , P311 , P314 , P321 , P377 , P381 , P403 , P403 + 233 , Р405 , Р501 | ||
| NFPA 704 (огненный алмаз) | [2]  3 4 0 | ||
| точка возгорания | -191 ° С (-311,8 ° F, 82,1 К) | ||
самовоспламенения температуру | 609 ° С (1128 ° F, 882 К) | ||
| Пределы взрываемости | 12,5–74,2% | ||
| Смертельная доза или концентрация (LD, LC): | |||
ЛК 50 ( средняя концентрация ) | 8636 частей на миллион (крыса, 15 минут) 5207 частей на миллион (крыса, 30 минут) 1784 частей на миллион (крыса, 4 часа) 2414 частей на миллион (мышь, 4 часа) 5647 частей на миллион (морская свинка, 4 часа) [1] | ||
LC Lo ( самый низкий опубликованный ) | 4000 частей на миллион (человек, 30 мин) 5000 частей на миллион (человек, 5 минут) [1] | ||
| NIOSH (пределы воздействия на здоровье в США): [3] | |||
PEL (Допустимо) | TWA 50 частей на миллион (55 мг / м 3 ) | ||
REL (рекомендуется) | TWA 35 частей на миллион (40 мг / м 3 ) C 200 частей на миллион (229 мг / м 3 ) | ||
IDLH (Непосредственная опасность) | 1200 частей на миллион | ||
| Родственные соединения | |||
Связанные оксиды углерода | Двуокись углерода Недокись углерода Оксоуглероды | ||
| Страница дополнительных данных | |||
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. | ||
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ | ||
Спектральные данные | УФ , ИК , ЯМР , МС | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Окись углерода ( CO ) - это горючий газ без цвета, запаха и вкуса, который немного менее плотен, чем воздух. Он токсичен для животных , использующих гемоглобин в качестве переносчика кислорода, когда встречается в концентрациях выше примерно 35 ppm, вызывая отравление угарным газом . Некоторое количество окиси углерода также вырабатывается при нормальном метаболизме животных в небольших количествах и, как считается, выполняет некоторые нормальные биологические функции . В атмосфере он пространственно изменчив и недолговечен, играя роль в образовании приземного озона .
Окись углерода состоит из одного атома углерода и одного атома кислорода , связанных тройной связью, которая состоит из двух чистых пи-связей и одной сигма-связи . Это самый простой оксиды углерода и является изоэлектронным с другими трехкратно связаны двухатомных видов , обладающих 10 валентных электронов, в том числе цианида аниона, в нитрозония катион, бора монофторида и молекулярного азота . В координационных комплексах лиганд окиси углерода называется карбонилом .
Примерно половина угарного газа в атмосфере Земли образуется в результате сжигания ископаемого топлива и биомассы (например, лесных пожаров и лесных пожаров ). [5] Большая часть остального приходится на химические реакции с органическими соединениями, выделяемыми в результате деятельности человека и растений. Попадая в атмосферу, он косвенно влияет на процесс радиационного воздействия , важный механизм, вызывающий изменение климата .
Люди также используют окись углерода для различных промышленных процессов в качестве источника для другого промышленного химического производства и для металлургии. Окись углерода также может использоваться в упаковке с модифицированной атмосферой, чтобы предотвратить порчу пищевых продуктов .
История [ править ]
Аристотель (384–322 до н.э.) первым записал, что при сжигании углей образуются ядовитые пары. Древний метод казни заключался в том, чтобы запереть преступника в ванной с тлеющими углями; однако тогда еще не было известно о механизме смерти. Греческий врач Гален (129–199 гг. Н.э.) предположил, что произошло изменение в составе воздуха, которое причиняло вред при вдыхании. [6] В 1776 году французский химик де Лассон произвел CO путем нагревания оксида цинка с коксом , но ошибочно пришел к выводу, что газообразным продуктом был водород , поскольку он горел голубым пламенем. Газ был идентифицирован как соединение, содержащее углерод.и кислород - шотландским химиком Уильямом Круикшенком в 1800 году. [7] [8] Его токсические свойства для собак были тщательно исследованы Клодом Бернаром около 1846 года [9].
Во время Второй мировой войны газовая смесь, включающая окись углерода, использовалась для поддержания работы автомобилей в тех частях мира, где не хватало бензина и дизельного топлива . Были установлены внешние (за некоторыми исключениями) генераторы древесного угля или древесного газа , и смесь атмосферного азота, водорода, монооксида углерода и небольших количеств других газов, полученная при газификации, подавалась по трубопроводу в газовый смеситель. Газовая смесь, полученная в результате этого процесса, известна как древесный газ . Окись углерода также широко использовалась во время Холокоста в некоторых лагерях смерти нацистской Германии , наиболее заметными из которых являлись газовые фургоны.в Хелмно и в программе « Эвтаназия » Action T4 . [10]
Источники [ править ]
Окись углерода образуется в результате частичного окисления углеродсодержащих соединений; он образуется, когда кислорода недостаточно для производства диоксида углерода (CO 2 ), например, при работе печи или двигателя внутреннего сгорания в замкнутом пространстве. В присутствии кислорода, в том числе в атмосферных концентрациях, окись углерода горит синим пламенем, образуя двуокись углерода. [11] Угольный газ , который широко использовался до 1960-х годов для домашнего освещения, приготовления пищи и отопления, содержал окись углерода в качестве важной составляющей топлива. Некоторые процессы в современной технологии, такие как выплавка чугуна , по-прежнему производят окись углерода в качестве побочного продукта.[12] Большое количество побочного продукта CO образуется во время окислительных процессов при производстве химикатов. По этой причине отходящие технологические газы необходимо очищать. С другой стороны, значительные исследовательские усилия прилагаются для оптимизации условий процесса [13], разработки катализатора с улучшенной селективностью [14] и понимания путей реакции, ведущих к целевому продукту и побочным продуктам. [15] [16]
Самый крупный источник окиси углерода в мире является естественным по происхождению из-за фотохимических реакций в тропосфере, которые производят около 5 × 10 12 килограммов в год. [17] Другие естественные источники CO включают вулканы, лесные пожары, другие формы горения и молекулы, выделяющие монооксид углерода .
В биологии оксид углерода естественным образом образуется под действием гемоксигеназы 1 и 2 на гем в результате распада гемоглобина . В результате этого процесса у нормальных людей образуется определенное количество карбоксигемоглобина , даже если они не дышат угарным газом. После первого сообщения о том, что окись углерода является нормальным нейромедиатором в 1993 году [18] [19], а также одним из трех газов, которые естественным образом модулируют воспалительные реакции в организме (два других - оксид азота и сероводород,), оксид углерода получил большое клиническое внимание как биологический регулятор. Во многих тканях, все три газа , как известна, выступает в качестве противовоспалительных средств , сосудорасширяющих средств , а также промоторов неоваскулярного роста. [20] Клинические испытания небольшого количества окиси углерода в качестве лекарственного средства продолжаются. [21] Слишком много окиси углерода вызывает отравление угарным газом .
Известно, что некоторые виды морских глубоководных млекопитающих содержат в крови концентрация окиси углерода, которая напоминает уровни, наблюдаемые у хронических курильщиков сигарет. [22] Считается, что эти повышенные уровни CO увеличивают сродство животных к гемоглобину и кислороду, что может помочь животным более эффективно доставлять кислород во время тяжелой гипоксемии, с которой они обычно сталкиваются во время длительных погружений. Кроме того, эти уровни CO могут помочь животным в предотвращении травм, связанных с ишемией / реперфузией, связанных с физиологической реакцией на погружение. [23]
Молекулярные свойства [ править ]
Окись углерода имеет молярную массу 28,0, что, согласно закону идеального газа , делает его немного менее плотным, чем воздух, средняя молярная масса которого составляет 28,8.
Длина связи между атомом углерода и атомом кислорода составляет 112,8 мкм . [24] [25] Эта длина связи соответствует тройной связи, как в молекулярном азоте (N 2 ), который имеет аналогичную длину связи (109,76 пм) и почти такую же молекулярную массу . Двойные связи углерод-кислород значительно длиннее, например, 120,8 пм в формальдегиде . [26] Точка кипения (82 К) и точка плавления (68 К) очень похожи на температуры N 2 (77 К и 63 К соответственно). Энергия диссоциации связи 1072 кДж / моль сильнее, чем у N 2.(942 кДж / моль) и представляет собой самую прочную из известных химических связей. [27]
Землю электронного состояние окиси углерода является синглетным состоянием [28] , так как нет неспаренных электронов.
Связь и дипольный момент [ править ]
Углерод и кислород вместе имеют в общей сложности 10 электронов в валентной оболочке . Следуя правилу октетов как для углерода, так и для кислорода, два атома образуют тройную связь с шестью общими электронами на трех связывающих молекулярных орбиталях, а не обычную двойную связь, обнаруживаемую в органических карбонильных соединениях. Поскольку четыре общих электрона происходят от атома кислорода и только два - от углерода, одна связывающая орбиталь занята двумя электронами кислорода, образуя дательную или дипольную связь . Это вызывает поляризацию C ← Oмолекулы с небольшим отрицательным зарядом углерода и небольшим положительным зарядом кислорода. Две другие связывающие орбитали каждая занята одним электроном от углерода и одной из кислорода, образуя (полярные) ковалентные связи с обратной поляризацией C → O, поскольку кислород более электроотрицателен, чем углерод. В свободной молекуле окиси углерода, чистый отрицательный заряд δ - остатки в конце углерода , и молекула имеет небольшой дипольный момент от 0,122 D . [29]
Таким образом, молекула асимметрична: кислород имеет большую электронную плотность, чем углерод, а также слегка положительно заряжен по сравнению с отрицательным углеродом. Напротив, изоэлектронная молекула диазота не имеет дипольного момента.
Окись углерода имеет вычисленный дробный порядок связи 2,6, что указывает на то, что «третья» связь важна, но составляет несколько меньшую, чем полная связь. [30] Таким образом, в терминах валентных связей, - C≡O + является наиболее важной структурой, в то время как: C = O , не является октет, но имеет нейтральный формальный заряд на каждом атоме и представляет собой второй наиболее важный резонансный вкладчика. Из-за неподеленной пары и двухвалентности углерода в этой резонансной структуре оксид углерода часто считается чрезвычайно стабилизированным карбеном . [31] Изоцианиды представляют собой соединения, в которых О заменен группой NR (R = алкил или арил) и имеют аналогичную схему связывания.
Если монооксид углерода действует как лиганд , полярность диполя может измениться на противоположную, что приведет к появлению отрицательного заряда на кислородном конце, в зависимости от структуры координационного комплекса . [32] См. Также раздел «Координационная химия» ниже.
Полярность связи и степень окисления [ править ]
Теоретические и экспериментальные исследования показывают, что, несмотря на большую электроотрицательность кислорода, дипольный момент указывает от более отрицательного конца углерода к более положительному концу кислорода. [33] [34] Эти три связи на самом деле являются полярными ковалентными связями , которые сильно поляризованы. Расчетная поляризация по отношению к атому кислорода составляет 71% для σ-связи и 77% для обеих π-связей . [35]
Степень окисления углерода в монооксиде углерода +2 в каждой из этих структур. Он рассчитывается путем подсчета всех связывающих электронов как принадлежащих к более электроотрицательному кислороду. Только два несвязывающих электрона на углероде относятся к углероду. Таким образом, углерод имеет только два валентных электрона в молекуле по сравнению с четырьмя в свободном атоме.
Биологические и физиологические свойства [ править ]
Токсичность [ править ]
Отравление угарным газом - самый распространенный вид смертельного отравления воздуха во многих странах. [36] Окись углерода бесцветна, без запаха и вкуса, но очень токсична. Он соединяется с гемоглобином, образуя карбоксигемоглобин , связываясь с участком гемоглобина, который обычно переносит кислород, что делает его неэффективным для доставки кислорода к тканям тела. Такие низкие концентрации, как 667 частей на миллион, могут вызвать превращение до 50% гемоглобина в организме в карбоксигемоглобин. [37] Уровень карбоксигемоглобина 50% может привести к судорогам, коме и летальному исходу. В Соединенных Штатах OSHA ограничивает уровни долгосрочного воздействия на рабочем месте выше 50 ppm. [38]
Наиболее частые симптомы отравления угарным газом могут напоминать другие типы отравлений и инфекций, включая такие симптомы, как головная боль , тошнота , рвота , головокружение , усталость и чувство слабости. Пострадавшие семьи часто считают себя жертвами пищевого отравления. Младенцы могут быть раздражительными и плохо питаться. Неврологические признаки включают спутанность сознания, дезориентацию, нарушение зрения, обмороки (обмороки) и судороги. [39]
Некоторые описания отравления окиси углерода включают в себя ретинальные геморрагии и ненормальное вишнево-красный оттенок крови. [40] В большинстве клинических диагнозов эти признаки редко замечаются. [39] Одна из трудностей с полезностью этого вишнево-красного эффекта заключается в том, что он исправляет или маскирует то, что в противном случае было бы нездоровым, поскольку главный эффект удаления деоксигенированного гемоглобина - сделать асфиксированного человека более нормальным или мертвые люди выглядят более реалистично, подобно эффекту красных красителей в бальзамирующей жидкости. «Ложный» или нефизиологический эффект красного окрашивания в ткани, отравленной аноксическим CO, связан с коммерческим использованием окиси углерода для окрашивания мяса, обсуждаемым ниже.
Окись углерода также связывается с другими молекулами, такими как миоглобин и митохондриальная цитохромоксидаза . Воздействие окиси углерода может вызвать значительное повреждение сердца и центральную нервную систему , особенно в бледном шар , [41] часто с длительными хроническими патологическими состояниями . Окись углерода может иметь серьезные неблагоприятные последствия для плода беременной женщины. [42]
Нормальная физиология человека [ править ]
Окись углерода вырабатывается организмом человека в качестве сигнальной молекулы . Таким образом, окись углерода может играть физиологическую роль в организме, например, как нейротрансмиттер или релаксант кровеносных сосудов . [43] Из-за роли окиси углерода в организме нарушения его метаболизма были связаны с множеством заболеваний, включая нейродегенерации, гипертонию, сердечную недостаточность и патологическое воспаление. [43] По сравнению с воспалением, угарный газ подавляет движение лейкоцитов к воспаленным тканям, стимулирует лейкоцитарный фагоцитоз бактерий и снижает выработку провоспалительных цитокинов.лейкоцитами. Кроме того, в исследованиях на животных моделях оксид углерода уменьшал тяжесть экспериментально индуцированного бактериального сепсиса , панкреатита, ишемии / реперфузии печени, колита, остеоартрита, повреждения легких, отторжения трансплантации легких и невропатической боли, способствуя заживлению кожных ран. Эти действия аналогичны действиям специализированных медиаторов, способствующих рассасыванию, которые смягчают, обращают вспять и восстанавливают повреждение тканей из-за различных воспалительных реакций. Действительно, окись углерода может действовать аддитивно с одним из этих медиаторов ( ResolvinD1) для ограничения воспалительных реакций. Исследования предполагают, что оксид углерода является физиологическим фактором ограничения воспаления, и предполагают, что его доставка с помощью ингаляционных препаратов или препаратов, образующих оксид углерода, может быть терапевтически полезна для контроля патологических воспалительных реакций. [44] [45] [46] [47]
СО действует как эндогенная сигнальная молекула, модулирует функции сердечно-сосудистой системы, ингибирует агрегацию и адгезию тромбоцитов, подавляет, реверсирует и восстанавливает повреждения, вызванные воспалительными реакциями. Он может играть роль потенциального терапевтического агента. [44] [48]
Микробиология [ править ]
Окись углерода является питательным веществом для метаногенных архей, которые восстанавливают ее до метана с помощью водорода. [49] Это тема развивающейся области биоорганической химии . Таким образом, экстремофильные микроорганизмы могут утилизировать окись углерода в таких местах, как термальные источники вулканов. [50]
Некоторые микробы могут преобразовывать окись углерода в двуокись углерода для получения энергии. [51]
У бактерий монооксид углерода образуется в результате восстановления диоксида углерода ферментом дегидрогеназа монооксида углерода , содержащим Fe - Ni - S белком. [52]
CooA - это белок-сенсор окиси углерода. [53] Объем его биологической роли до сих пор неизвестен; он может быть частью сигнального пути у бактерий и архей. Встречаемость у млекопитающих не установлена.
Происшествие [ править ]
Окись углерода встречается в различных природных и искусственных средах. Типичные концентрации в миллионных долях следующие:
| ppmv: объемные части на миллион (примечание: объемная доля равна мольной доле только для идеального газа, см. объем (термодинамика) ) | |
| Концентрация | Источник |
|---|---|
| 0,1 частей на миллион по объему | Уровень естественной атмосферы ( MOPITT ) [56] |
| 0,5–5 частей на миллион по объему | Средний уровень в домах [57] |
| 5–15 частей на миллион по объему | Рядом с правильно отрегулированными газовыми плитами в домах, выбросы выхлопных газов современных автомобилей [58] [ необходима цитата ] |
| 17 частей на миллион по объему | Атмосфера Венеры |
| 100–200 частей на миллион по объему | Выхлопные газы автомобилей в центральной части Мехико в 1975 году [59] |
| 700 частей на миллион по объему | Атмосфера Марса |
| <1000 частей на миллион по объему | Выхлопные газы автомобилей после прохождения через каталитический нейтрализатор [60] |
| 5000 частей на миллион по объему | Выхлоп от домашнего дровяного огня [61] |
| 30 000–100 000 частей на миллион | Неразбавленный теплый выхлоп автомобиля без каталитического нейтрализатора [60] |
Атмосферное присутствие [ править ]
Окись углерода (CO) присутствует в атмосфере Земли в небольших количествах (около 80 частей на миллиард) . Около половины оксида углерода в атмосфере Земли образуется в результате сжигания ископаемого топлива и биомассы (например, лесных пожаров и лесных пожаров ). [5] Большая часть остального приходится на химические реакции с органическими соединениями, выделяемыми в результате деятельности человека и растений. Небольшие количества также выбрасываются из океана и в результате геологической деятельности, потому что окись углерода растворяется в расплавленной вулканической породе при высоком давлении в мантии Земли . [62]Поскольку природные источники окиси углерода меняются из года в год, трудно точно измерить естественные выбросы газа.
Окись углерода косвенно влияет на радиационное воздействие , повышая концентрацию прямых парниковых газов , включая метан и тропосферный озон . СО может вступать в химическую реакцию с другими компонентами атмосферы ( в первую очередь гидроксильных радикала , ОН . ) , Что в противном случае было бы уничтожить метан. [63] В результате естественных процессов в атмосфере он окисляется до двуокиси углерода и озона. Окись углерода недолговечна в атмосфере (со средней продолжительностью жизни от одного до двух месяцев) и пространственно различается по концентрации. [64]
В атмосфере Венеры окись углерода возникает в результате фотодиссоциации углекислого газа электромагнитным излучением с длинами волн короче 169 нм .
Из-за длительного срока службы в средней тропосфере окись углерода также используется в качестве индикатора выбросов загрязняющих шлейфов. [65]
Городское загрязнение [ править ]
Окись углерода является временным загрязнителем атмосферы в некоторых городских районах, главным образом из-за выхлопных газов двигателей внутреннего сгорания (включая автомобили, переносные и резервные генераторы, газонокосилки, моечные машины и т. Д.), Но также в результате неполного сгорания различных других видов топлива ( включая древесину, уголь, древесный уголь, масло, парафин, пропан, природный газ и мусор).
Крупные случаи загрязнения CO можно наблюдать из космоса над городами. [66]
Роль в образовании озона на приземном уровне [ править ]
Окись углерода, наряду с альдегидами , входит в серию циклов химических реакций, образующих фотохимический смог . Он реагирует с гидроксильным радикалом ( • OH) с образованием промежуточного радикала • HOCO, который быстро передает свой радикальный водород в O 2 с образованием пероксирадикала (HO 2 • ) и диоксида углерода (CO 2 ). [67] Пероксирадикал впоследствии реагирует с оксидом азота (NO) с образованием диоксида азота (NO 2 ) и гидроксильного радикала. NO 2 дает O ( 3P) посредством фотолиза, тем самым образуя O 3 после реакции с O 2 . Поскольку при образовании NO 2 образуется гидроксильный радикал , баланс последовательности химических реакций, начинающихся с оксида углерода и ведущих к образованию озона, составляет:
- CO + 2O 2 + hν → CO 2 + O 3
(где hν относится к фотону света, поглощаемому молекулой NO 2 в последовательности)
Хотя создание NO 2 является критическим этапом, ведущим к образованию озона низкого уровня , оно также увеличивает этот озон другим, в некоторой степени взаимоисключающим образом, путем уменьшения количества NO, которое доступно для реакции с озоном. [68]
Загрязнение помещений [ править ]
В закрытых помещениях концентрация окиси углерода может легко возрасти до смертельного уровня. В среднем 170 человек в Соединенных Штатах ежегодно умирают от окиси углерода, производимой неавтомобильными потребительскими товарами. [69] По данным Министерства здравоохранения Флориды , «каждый год более 500 американцев умирают от случайного воздействия угарного газа, и тысячам больше в США требуется неотложная медицинская помощь в случае несмертельного отравления угарным газом». [70] Эти продукты включают неисправные приборы для сжигания топлива, такие как печи, плиты, водонагреватели, а также газ и керосинкомнатные обогреватели; оборудование с приводом от двигателя, такое как переносные генераторы; камины; и древесный уголь, который сжигают в домах и других закрытых помещениях. Американская ассоциация центров по борьбе с отравлениями (AAPCC) сообщила о 15 769 случаях отравления угарным газом, в результате которых в 2007 году погибло 39 человек. [71] В 2005 году CPSC сообщил о 94 случаях смерти от отравления угарным газом, связанного с генератором. [69] Известно, что 47 из этих смертей произошли во время отключения электроэнергии из-за суровой погоды, включая ураган Катрина . [69] Третьи умирают от окиси углерода, производимого непотребительскими товарами, такими как автомобили, оставленные работающими в пристроенных гаражах. В Центры по контролю и профилактике заболеванийПо оценкам, несколько тысяч человек ежегодно обращаются в отделения неотложной помощи больниц для лечения отравления угарным газом. [72]
Биологические источники [ править ]
Окись углерода вырабатывается при катаболизме гема и, таким образом, присутствует в крови. Нормальные уровни циркулирующего в крови составляют от 0% до 3% насыщения [73], т.е. отношение количества карбоксигемоглобина к общему циркулирующему гемоглобину [74], и выше у курильщиков. Известно, что некоторые виды морских глубоководных млекопитающих поддерживают уровень карбоксигемоглобина в пределах 5-10%. [22] Уровень окиси углерода нельзя определить с помощью медицинского осмотра. Для лабораторных исследований требуется образец крови (артериальной или венозной) и лабораторный анализ на СО-оксиметре. Кроме того, существует неинвазивный метод определения карбоксигемоглобина (SpCO) от Pulse CO-Oximetry, который прошел валидацию по сравнению с инвазивными методами. [75]
Белок-сенсор угарного газа CooA был охарактеризован у бактерий.
Астрономия [ править ]
За пределами Земли окись углерода является второй по распространенности двухатомной молекулой в межзвездной среде после молекулярного водорода . Из-за своей асимметрии эта полярная молекула дает гораздо более яркие спектральные линии, чем молекула водорода, что значительно упрощает обнаружение CO. Межзвездный CO был впервые обнаружен с помощью радиотелескопов в 1970 году. В настоящее время он является наиболее часто используемым индикатором молекулярного газа в межзвездной среде галактик, поскольку молекулярный водород можно обнаружить только с помощью ультрафиолетового света, что требует использования космических телескопов . Наблюдения за угарным газом предоставляют большую часть информации о молекулярных облаках, в которых больше всегообразуются звезды . [76]
Бета Живописца , вторая по яркости звезда в созвездии Пиктора , показывает избыток инфракрасного излучения по сравнению с нормальными звездами ее типа, которое вызвано большим количеством пыли и газа ( в том числе окиси углерода) [77] [78] вблизи звезды .
Твердая окись углерода входит в состав комет . [79] Комета Галлея на 15% состоит из окиси углерода. [80] Также была идентифицирована спектроскопия на поверхности спутника Нептуна Тритона . [81] При комнатной температуре и атмосферном давлении окись углерода на самом деле является только метастабильной (см. Реакцию Будуара ), и то же самое верно при низких температурах, где CO и CO
2твердые, но тем не менее могут существовать в кометах миллиарды лет. В атмосфере Плутона очень мало CO , которая, похоже, образовалась из комет. Это может быть потому, что внутри Плутона есть (или была) жидкая вода. Окись углерода может реагировать с водой с образованием двуокиси углерода и водорода:
- CO + H 2 O → H
2+ CO
2
Это называется реакцией конверсии водяного газа, когда она происходит в газовой фазе, но она также может происходить (очень медленно) в водном растворе. Если парциальное давление водорода достаточно высокое (например, в подземном море), образуется муравьиная кислота :
- CO + H 2 O → HCOOH
Эти реакции могут происходить через несколько миллионов лет даже при таких температурах, как на Плутоне. [82]
Горное дело [ править ]
Горняки называют угарный газ «белой сыростью» или «тихим убийцей». Его можно найти в замкнутых пространствах с плохой вентиляцией как в открытых, так и в подземных выработках. Наиболее распространенными источниками окиси углерода при добыче полезных ископаемых являются двигатель внутреннего сгорания и взрывчатые вещества, однако на угольных шахтах окись углерода также может быть обнаружена из-за низкотемпературного окисления угля. [83]
Производство [ править ]
Для производства окиси углерода разработано множество методов. [84]
Промышленное производство [ править ]
Основным промышленным источником CO является генераторный газ , смесь, содержащая в основном монооксид углерода и азот, образующаяся в результате сгорания углерода в воздухе при высокой температуре, когда имеется избыток углерода. В печи воздух проходит через слой кокса . Первоначально произведенный CO 2 уравновешивается с оставшимся горячим углеродом с образованием CO. Реакция CO 2 с углеродом с образованием CO описывается как реакция Будуара . [85] При температуре выше 800 ° C преобладающим продуктом является CO:
- CO 2 + C → 2 CO (ΔH = 170 кДж / моль)
Другой источник - « водяной газ », смесь водорода и окиси углерода, полученная в результате эндотермической реакции пара и углерода:
- H 2 O + C → H 2 + CO (ΔH = +131 кДж / моль)
Другие аналогичные « синтез-газы » можно получить из природного газа и других видов топлива.
Окись углерода также может быть произведена путем высокотемпературного электролиза двуокиси углерода с использованием твердооксидных электролизеров : [86] Один метод, разработанный в DTU Energy, использует катализатор на основе оксида церия и не имеет проблем с загрязнением катализатора [87] [ 88]
- 2 CO 2 → 2 CO + O 2
Оксид углерода также является побочным продуктом сокращения металлических оксидных руд с углеродом, показанных в упрощенной форме следующим образом :
- МО + Ц → М + СО
Окись углерода также образуется при прямом окислении углерода в ограниченном количестве кислорода или воздуха.
- 2 C (т) + O 2 → 2 CO (г)
Поскольку CO представляет собой газ, процесс восстановления может осуществляться путем нагревания с использованием положительной (благоприятной) энтропии реакции. На диаграмме Ellingham показано , что образование СО отдается предпочтение по сравнению СО 2 при высоких температурах.
Лабораторная подготовка [ править ]
Окись углерода удобно получать в лаборатории с помощью дегидратации из муравьиной кислоты или щавелевой кислоты , например , с концентрированной серной кислотой . [89] [90] [91] Другой метод состоит в нагревании однородной смеси порошкообразного цинка металла и карбонат кальция , который выпускает СО и оставляет оксид цинка и оксид кальция :
- Zn + CaCO 3 → ZnO + CaO + CO
Нитрат серебра и йодоформ также дают оксид углерода:
- CHI 3 + 3AgNO 3 + H 2 O → 3HNO 3 + CO + 3AgI
Наконец, соли оксалатов металлов выделяют CO при нагревании, оставляя карбонат в качестве побочного продукта:
- Na
2C
2О
4→ Na
2CO
3+ CO
Координационная химия [ править ]
Большинство металлов образуют координационные комплексы, содержащие ковалентно присоединенный монооксид углерода. Только металлы в более низких степенях окисления могут образовывать комплекс с лигандами монооксида углерода . Это связано с тем, что должна быть достаточная электронная плотность для облегчения обратного донорства с d xz -орбитали металла на молекулярную орбиталь π * из CO. Неподеленная пара на атоме углерода в CO также отдает электронную плотность d x² − y² на металле, чтобы сформировать сигма-связь . Это донорство электронов также проявляется цис-эффектом или лабилизацией лигандов CO в цис-положении. Карбонил никеля, например, образуется в результате прямого сочетания оксида углерода и металлического никеля :
- Ni + 4 CO → Ni (CO) 4 (1 бар, 55 ° C)
По этой причине никель в любых трубках или деталях не должен вступать в продолжительный контакт с оксидом углерода. Карбонил никеля легко разлагается обратно на Ni и CO при контакте с горячими поверхностями, и этот метод используется для промышленной очистки никеля в процессе Монда . [92]
В карбониле никеля и других карбонилах электронная пара на углероде взаимодействует с металлом; монооксид углерода отдает металлу электронную пару. В этих ситуациях окись углерода называется карбонильным лигандом . Одним из наиболее важных карбонилов металлов является пентакарбонил железа , Fe (CO) 5 :
Многие комплексы металл-CO получают декарбонилированием органических растворителей, а не CO. Например, трихлорид иридия и трифенилфосфин реагируют в кипящем 2-метоксиэтаноле или ДМФ с образованием IrCl (CO) (PPh 3 ) 2 .
Карбонилы металлов в координационной химии обычно изучаются с помощью инфракрасной спектроскопии .
Органическая химия и химия основных групп [ править ]
В присутствии сильных кислот и воды окись углерода реагирует с алкенами с образованием карбоновых кислот в процессе, известном как реакция Коха – Хафа. [89] В реакции Гаттермана-Кох , арены преобразуются в бензальдегида производные в присутствии AlCl 3 и HCl . [90] Литийорганические соединения (например, бутиллитий ) реагируют с монооксидом углерода, но эти реакции имеют мало научного применения.
Хотя CO реагирует с карбокатионами и карбанионами , он относительно инертен по отношению к органическим соединениям без вмешательства металлических катализаторов. [93]
С реагентами основной группы CO претерпевает несколько заслуживающих внимания реакций. Хлорирование CO - это промышленный способ получения важного соединения фосгена . С бораном CO образует аддукт H 3 BCO , который изоэлектронен с катионом ацетилия [H 3 CCO] + . CO реагирует с натрием с образованием продуктов, образующихся в результате сочетания CC, таких как ацетилендиолат натрия 2 Na.+
· C
2О2-
2. Он реагирует с расплавленным калием с образованием смеси металлоорганического соединения, ацетилендиолата калия 2 К.+
· C
2О2-
2, бензолгексолат калия 6 K+
C
6О6-
6, [94] и родизонат калия 2 K+
· C
6О2-
6. [95]
Соединения циклогексангексона или трихиноила (C 6 O 6 ) и циклопентанепентона или лейконовой кислоты (C 5 O 5 ), которые до сих пор были получены только в следовых количествах, можно рассматривать как полимеры монооксида углерода.
При давлении более 5 гигапаскалей окись углерода превращается в твердый полимер углерода и кислорода . Это метастабильно при атмосферном давлении, но является мощным взрывчатым веществом. [96] [97]
Использует [ редактировать ]
Химическая промышленность [ править ]
Окись углерода - это промышленный газ, который находит множество применений при производстве сыпучих химических веществ. [98] Большие количества альдегидов образуются в результате реакции гидроформилирования алкенов , монооксида углерода и H 2 . Гидроформилирование сочетается с процессом производства высших олефинов Shell с образованием предшественников детергентов .
Фосген , используемый для получения изоцианатов, поликарбонатов и полиуретанов, получают путем пропускания очищенного монооксида углерода и газообразного хлора через слой пористого активированного угля , который служит катализатором . Мировое производство этого соединения оценивалось в 2,74 миллиона тонн в 1989 году. [99]
- CO + Cl 2 → COCl 2
Метанол получают путем гидрирования окиси углерода. В родственной реакции гидрирование монооксида углерода сочетается с образованием связи CC, как в процессе Фишера-Тропша, где монооксид углерода гидрируется до жидкого углеводородного топлива. Эта технология позволяет преобразовывать уголь или биомассу в дизельное топливо.
В процессе Cativa окись углерода и метанол реагируют в присутствии гомогенного иридиевого катализатора и йодистоводородной кислоты с образованием уксусной кислоты . Этот процесс отвечает за большую часть промышленного производства уксусной кислоты .
В промышленных масштабах чистый монооксид углерода используется для очистки никеля в процессе Монда .
Окись углерода также может использоваться в реакции конверсии водяного газа для получения водорода .
Окраска мяса [ править ]
Окись углерода используется в упаковочных системах с модифицированной атмосферой в США, в основном для свежих мясных продуктов, таких как говядина, свинина и рыба, чтобы они выглядели свежими. Окись углерода соединяется с миоглобином с образованием карбоксимиоглобина, ярко-вишнево-красного пигмента. Карбоксимиоглобин более стабилен, чем кислородсодержащая форма миоглобина, оксимиоглобин, который может окисляться до коричневого пигмента метмиоглобина . Этот стабильный красный цвет может сохраняться намного дольше, чем у мяса в обычной упаковке. [100] Типичные уровни окиси углерода, используемые на объектах, использующих этот процесс, составляют от 0,4% до 0,5%.
Впервые технология получила статус « общепризнанной безопасной » (GRAS) Управлением по контролю за продуктами и лекарствами США (FDA) в 2002 году для использования в качестве системы вторичной упаковки и не требует маркировки. В 2004 году FDA одобрило CO в качестве метода первичной упаковки, заявив, что CO не маскирует запах порчи. [101] Несмотря на это решение, процесс остается спорным из-за опасений, что он скрывает порчу. [102] В 2007 году в Палату представителей Соединенных Штатов был внесен законопроект [103] о маркировке упаковки с модифицированным оксидом углерода как цветовой добавки, но этот закон был принят подкомитетом. Процесс запрещен во многих других странах, включая Японию, Сингапур., и Европейский Союз . [104] [105] [106]
Медицина [ править ]
В биологии оксид углерода естественным образом образуется под действием гемоксигеназы 1 и 2 на гем в результате распада гемоглобина . В результате этого процесса у нормальных людей образуется определенное количество карбоксигемоглобина, даже если они не дышат угарным газом.
После первого сообщения о том, что окись углерода является нормальным нейромедиатором в 1993 году [18] [19], а также одним из трех газов, которые естественным образом модулируют воспалительные реакции в организме (два других - оксид азота и сероводород ), окись углерода имеет получил большое клиническое внимание как биологический регулятор. Во многих тканях, все три газа , как известна, действует как противовоспалительные средства , вазодилататоры и вдохновители неоваскулярного роста. [20] Однако проблемы являются сложными, так как рост неоваскулярных сосудов не всегда полезен, поскольку он играет роль в росте опухоли, а также в повреждении от влажного дегенерация желтого пятна , заболевание, при котором курение (основной источник окиси углерода в крови, в несколько раз превышающая естественную выработку) увеличивает риск от 4 до 6 раз.
Существует теория, что в некоторых синапсах нервных клеток , когда закладываются долгосрочные воспоминания , принимающая клетка вырабатывает окись углерода, которая обратно передается в передающую клетку, давая ей указание на более легкую передачу в будущем. Было показано, что некоторые такие нервные клетки содержат гуанилатциклазу , фермент, который активируется оксидом углерода. [19]
Исследования с участием окиси углерода были проведены во многих лабораториях по всему миру на предмет его противовоспалительных и цитопротекторных свойств. Эти свойства могут быть использованы для предотвращения развития ряда патологических состояний, включая ишемическое реперфузионное повреждение, отторжение трансплантата, атеросклероз, тяжелый сепсис, тяжелую малярию или аутоиммунитет. Клинические испытания с участием людей проводились, однако результаты еще не опубликованы. [21]
Металлургия [ править ]
Окись углерода является сильным восстановителем и с древних времен использовалась в пирометаллургии для восстановления металлов из руд . Окись углерода удаляет кислород из оксидов металлов, восстанавливая их до чистого металла при высоких температурах, образуя при этом диоксид углерода . Окись углерода обычно не подается в реактор в газовой фазе как есть, а скорее образуется при высокой температуре в присутствии кислородсодержащей руды или углеродсодержащего агента, такого как кокс, и при высокой температуре. Доменная печь процесс представляет собой типичный пример процесса восстановления металла из руды с монооксидом углерода.
Лазеры [ править ]
Окись углерода также использовалась в качестве лазерной среды в мощных инфракрасных лазерах . [107]
Ниша использует [ править ]
Окись углерода была предложена для использования в качестве топлива на Марсе. Двигатели с оксидом углерода / кислородом были предложены для раннего использования в наземных транспортных средствах, поскольку и оксид углерода, и кислород можно было напрямую получить из атмосферы диоксида углерода Марса путем электролиза диоксида циркония , без использования каких-либо ресурсов марсианской воды для получения водорода, который был бы необходим для получения водорода. метан или любое водородное топливо. [108] Аналогичным образом, доменный газ, собранный в верхней части доменной печи, по-прежнему содержит от 10% до 30% окиси углерода и используется в качестве топлива в печах Каупера и печах Сименс-Мартин на мартеновском производстве стали..
См. Также [ править ]
- Окись углерода (страница данных) - страница химических данных
- Окись углерода дыхания
- Детектор угарного газа - устройство, измеряющее угарный газ (CO).
- Критерии загрязнителей воздуха
- Список высокотоксичных газов - статья со списком в Википедии
- Общество подводной и гипербарической медицины - организация в США, занимающаяся исследованиями и обучением в области гипербарической физиологии и медицины. - гипербарическое лечение отравления угарным газом
- Фонд Рубикон - Некоммерческая организация по содействию исследованиям и доступу к информации о подводных погружениях, исследованиях статей об отравлении угарным газом.
Ссылки [ править ]
- ^ a b «Окись углерода» . Немедленно опасная для жизни или здоровья концентрация (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Ричард, Поханиш (2012). Справочник Ситтига по токсичным и опасным химическим веществам и канцерогенным веществам (2-е изд.). Эльзевир. п. 572. ISBN. 978-1-4377-7869-4. Проверено 5 сентября 2015 года .
- ^ Карманный справочник NIOSH по химическим опасностям. «# 0105» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ GOV, NOAA Управление реагирования и восстановления, США. «ОКИСЬ УГЛЕРОДА - CAMEO Chemicals - NOAA» . cameochemicals.noaa.gov .
- ^ a b Сайнфелд, Джон; Пандис, Спирос (2006). Химия и физика атмосферы: от загрязнения воздуха до изменения климата . Джон Вили и сыновья. ISBN 978-0-471-72018-8.
- ^ Пенни, Дэвид Г. (2000) Токсичность окиси углерода , CRC Press, стр. 5, ISBN 0-8493-2065-8 .
- ^ Cruickshank, W. (1801) "Некоторые наблюдения над различными углеводородами и комбинациями углерода с кислородом и т.д. в ответ на некоторые из последних возражений доктора Пристли против новой системы химии", Journal of Natural Philosophy, Chemistry and the Arts [он же журнал Николсона ], 1-я серия, 5 : 1–9.
- ^ Cruickshank, W. (1801) "Некоторые дополнительные наблюдения об углеводородах и газообразном оксиде углерода", Journal of Natural Philosophy, Chemistry and the Arts , 1-я серия, 5 : 201–211.
- ^ Уоринг, Розмари Н .; Steventon, Glyn B .; Митчелл, Стив С. (2007). Молекулы смерти . Imperial College Press. п. 38. ISBN 978-1-86094-814-5.
- ^ Кухня, Мартин (2006). История современной Германии, 1800–2000 гг . Вили-Блэквелл. п. 323. ISBN 978-1-4051-0041-0.
- ^ Томпсон, Майк. Окись углерода - молекула месяца , Винчестерский колледж, Великобритания.
- ^ Эйрес, Роберт U .; Эйрес, Эдвард Х. (2009). Преодоление энергетического разрыва: переход от зависимости от ископаемого топлива к будущему с чистой энергией . Издательство Wharton School Publishing. п. 36. ISBN 978-0-13-701544-3.
- ^ Кинетические исследования окисления пропана на смешанных оксидных катализаторах на основе Mo и V (PDF) . 2011 г.
- ^ Amakawa, Кадзухико; Коленько, Юрий В .; Вилла, Альберто; Шустер, Манфред Э /; Чепеи, Ленард-Иштван; Вайнберг, Гизела; Врабец, Сабина; Науманн д'Алнонкур, Рауль; Гиргсдис, Франк; Прати, Лаура; Шлёгль, Роберт; Траншке, Аннетт (26 апреля 2013 г.). «Многофункциональность кристаллических оксидных катализаторов MoV (TeNb) M1 в селективном окислении пропана и бензилового спирта» . Катализ ACS . 3 (6): 1103–1113. DOI : 10.1021 / cs400010q .
- ^ Науманн д'Алнонкур, Рауль; Чепеи, Ленард-Иштван; Хэвекер, Майкл; Гиргсдис, Франк; Schuster, Manfred E .; Шлёгль, Роберт; Траншке, Аннетт (март 2014 г.). «Реакционная сеть в окислении пропана над фазово-чистыми оксидными катализаторами MoVTeNb M1» (PDF) . Журнал катализа . 311 : 369–385. DOI : 10.1016 / j.jcat.2013.12.008 . hdl : 11858 / 00-001M-0000-0014-F434-5 . Архивировано из оригинального (PDF) 15 февраля 2016 года . Проверено 14 апреля 2018 .
- ^ Хэвекер, Майкл; Врабец, Сабина; Крёнерт, Ютта; Чепеи, Ленард-Иштван; Науманн д'Алнонкур, Рауль; Коленько, Юрий В .; Гиргсдис, Франк; Шлёгль, Роберт; Траншке, Аннетт (январь 2012 г.). «Химия поверхности фазово-чистого оксида M1 MoVTeNb при работе с селективным окислением пропана до акриловой кислоты» (PDF) . Журнал катализа . 285 (1): 48–60. DOI : 10.1016 / j.jcat.2011.09.012 . hdl : 11858 / 00-001M-0000-0012-1BEB-F . Архивировано из оригинального (PDF) 30 октября 2016 года . Проверено 14 апреля 2018 .
- ^ Weinstock, B .; Ники, Х. (1972). «Баланс угарного газа в природе». Наука . 176 (4032): 290–2. Bibcode : 1972Sci ... 176..290W . DOI : 10.1126 / science.176.4032.290 . PMID 5019781 . S2CID 25223868 .
- ^ а б Верма, А; Hirsch, D .; Glatt, C .; Ronnett, G .; Снайдер, С. (1993). «Окись углерода: предполагаемый нейронный мессенджер». Наука . 259 (5093): 381–4. Bibcode : 1993Sci ... 259..381V . DOI : 10.1126 / science.7678352 . PMID 7678352 .
- ^ a b c Колата, Джина (26 января 1993 г.). «Угарный газ используется клетками мозга в качестве нейротрансмиттера» . Нью-Йорк Таймс . Проверено 2 мая 2010 года .
- ^ a b Li, L; Сюй, А; Мур, ПК (2009). «Действия и взаимодействия оксида азота, оксида углерода и сероводорода в сердечно-сосудистой системе и при воспалении - сказка о трех газах!». Фармакология и терапия . 123 (3): 386–400. DOI : 10.1016 / j.pharmthera.2009.05.005 . PMID 19486912 .
- ^ a b Джонсон, Кэролайн Ю. (16 октября 2009 г.). «Ядовитый газ может принести пользу для здоровья» . The Boston Globe . Проверено 16 октября 2009 года .
- ^ a b Tift, M; Ponganis, P; Крокер, Д. (2014). «Повышенный карбоксигемоглобин у морского млекопитающего, северного морского слона» . Журнал экспериментальной биологии . 217 (10): 1752–1757. DOI : 10,1242 / jeb.100677 . PMC 4020943 . PMID 24829326 .
- ^ Тифт, М; Понганис, П. (2019). «Временные рамки адаптации к гипоксии - морские слоны выделяются среди дайверов» . Границы физиологии . 10 : 677. DOI : 10,3389 / fphys.2019.00677 . PMC 6558045 . PMID 31214049 .
- ^ Гиллиам, штат Орегон; Джонсон, CM; Горди, В. (1950). «Микроволновая спектроскопия в диапазоне от двух до трех миллиметров». Физический обзор . 78 (2): 140–144. Bibcode : 1950PhRv ... 78..140G . DOI : 10.1103 / PhysRev.78.140 .
- ^ Хейнс, Уильям М. (2010). Справочник по химии и физике (91 изд.). Бока-Ратон, Флорида, США: CRC Press . п. 9–33. ISBN 978-1-43982077-3.
- ^ Хейнс, Уильям М. (2010). Справочник по химии и физике (91 изд.). Бока-Ратон, Флорида, США: CRC Press . п. 9–39. ISBN 978-1-43982077-3.
- ^ Общие энергии связи (D) и длины связи (r) . wiredchemist.com
- Перейти ↑ Vidal, CR (28 июня 1997 г.). «Сильновозбужденные триплетные состояния окиси углерода» . Архивировано из оригинала на 2006-08-28 . Проверено 16 августа 2012 года .
- ^ Скузерия, Густаво Э .; Миллер, Майкл Д .; Дженсен, Фрэнк; Герцен, Ян (1991). «Дипольный момент окиси углерода». J. Chem. Phys . 94 (10): 6660. Bibcode : 1991JChPh..94.6660S . DOI : 10.1063 / 1.460293 .
- ^ Мартини, Райан Дж .; Bultema, Jarred J .; Vander Wal, Mark N .; Burkhart, Brandon J .; Vander Griend, Douglas A .; Декок, Роджер Л. (01.08.2011). «Порядок связи и химические свойства BF, CO и N2». Журнал химического образования . 88 (8): 1094–1097. Bibcode : 2011JChEd..88.1094M . DOI : 10.1021 / ed100758t . ISSN 0021-9584 . S2CID 11905354 .
- ^ 1925-, Ульрих, Анри (2009). Кумулены в щелочных реакциях . Wiley InterScience (Интернет-сервис). Чичестер, Великобритания: Wiley. п. 45. ISBN 9780470747957. OCLC 476311784 .CS1 maint: числовые имена: список авторов ( ссылка )
- ^ Лупинетти, Энтони Дж .; Фау, Стефан; Френкинг, Гернот; Штраус, Стивен Х. (1997). «Теоретический анализ связи между CO и положительно заряженными атомами». J. Phys. Chem. . 101 (49): 9551–9559. Bibcode : 1997JPCA..101.9551L . DOI : 10.1021 / jp972657l .
- ^ Бланко, Фернандо; Алькорта, Ибон; Солиманнеджад, Мохаммад; Эльгеро, Хосе (2009). «Теоретическое исследование комплексов 1: 1 между оксидом углерода и гипогалогеновой кислотой». J. Phys. Chem. . 113 (13): 3237–3244. Bibcode : 2009JPCA..113.3237B . DOI : 10.1021 / jp810462h . ЛВП : 10261/66300 . PMID 19275137 .
- ^ Мертс, Вт; Де Леу, FH; Диманус, А. (1 июня 1977 г.). «Электрические и магнитные свойства окиси углерода методом молекулярно-лучевой электрорезонансной спектроскопии». Химическая физика . 22 (2): 319–324. Bibcode : 1977CP ..... 22..319M . DOI : 10.1016 / 0301-0104 (77) 87016-X .
- ^ Стефан, Торстен; Яношек, Рудольф (2000). «Насколько важны двойные связи S = O и P = O для описания молекул кислоты H 2 SO 3 , H 2 SO 4 и H 3 PO 3 соответственно?». Журнал молекулярного моделирования . 6 (2): 282–288. DOI : 10.1007 / PL00010730 . S2CID 96291857 .
- ^ Omaye ST (2002). «Метаболическая модуляция токсичности окиси углерода». Токсикология . 180 (2): 139–150. DOI : 10.1016 / S0300-483X (02) 00387-6 . PMID 12324190 .
- ^ Tikuisis, P; Кейн, DM; Маклеллан, TM; Buick, F; Фэйрберн, С.М. (1992). «Скорость образования карбоксигемоглобина у людей, подвергающихся действию монооксида углерода». Журнал прикладной физиологии . 72 (4): 1311–9. DOI : 10.1152 / jappl.1992.72.4.1311 . PMID 1592720 .
- ^ «Руководящие принципы OSHA CO» . OSHA. Архивировано из оригинального 26 января 2010 года . Проверено 27 мая 2009 года .
- ^ a b Блюменталь, Иван (1 июня 2001 г.). «Отравление угарным газом» . JR Soc Med . 94 (6): 270–272. DOI : 10.1177 / 014107680109400604 . PMC 1281520 . PMID 11387414 .
- ^ Ганонг, Уильям Ф (2005). «37» . Обзор медицинской физиологии (22-е изд.). Макгроу-Хилл. п. 684. ISBN 978-0-07-144040-0. Проверено 27 мая 2009 года .
- ^ Prockop LD, Чичкова RI (2007). «Отравление угарным газом: обновленный обзор». J Neurol Sci . 262 (1-2): 122-130. DOI : 10.1016 / j.jns.2007.06.037 . PMID 17720201 . S2CID 23892477 .
- ^ Tucker Blackburn, Сьюзен (2007). Физиология матери, плода и новорожденного: клиническая перспектива . Elsevier Health Sciences. п. 325. ISBN 978-1-4160-2944-1.
- ^ а б Ву, Л; Ван, Р. (декабрь 2005 г.). «Окись углерода: эндогенное производство, физиологические функции и фармакологические применения». Pharmacol Rev . 57 (4): 585–630. DOI : 10,1124 / pr.57.4.3 . PMID 16382109 . S2CID 17538129 .
- ^ a b Уоллес Дж. Л., Ианаро А., Фланниган К. Л., Чирино Дж. (2015). «Газообразные медиаторы в разрешении воспаления». Семинары по иммунологии . 27 (3): 227–33. DOI : 10.1016 / j.smim.2015.05.004 . PMID 26095908 .
- Перейти ↑ Uehara EU, Shida Bde S, de Brito CA (2015). «Роль оксида азота в иммунных ответах против вирусов: помимо микробицидной активности». Исследование воспаления . 64 (11): 845–52. DOI : 10.1007 / s00011-015-0857-2 . PMID 26208702 . S2CID 14587150 .
- ^ Nakahira K, Choi AM (2015). «Окись углерода в лечении сепсиса» . Американский журнал физиологии. Клеточная и молекулярная физиология легких . 309 (12): L1387–93. DOI : 10,1152 / ajplung.00311.2015 . PMC 4683310 . PMID 26498251 .
- ^ Shinohara М, Serhan CN (2016). «Новые эндогенные молекулы, способствующие разрешению: незаменимые производные жирных кислот и газообразные медиаторы в разрешении воспаления» . Журнал атеросклероза и тромбоза . 23 (6): 655–64. DOI : 10,5551 / jat.33928 . PMC 7399282 . PMID 27052783 .
- ^ Olas, Беата (25 апреля 2014). «Окись углерода не всегда является ядовитым газом для человеческого организма: физиологические и фармакологические особенности СО». Химико-биологические взаимодействия . 222 (5 октября 2014 г.): 37–43. DOI : 10.1016 / j.cbi.2014.08.005 . PMID 25168849 .
- ^ Thauer, РК (1998). «Биохимия метаногенеза: дань уважения Марджори Стивенсон. Лекция 1998 года, посвященная премии Марджори Стефенсон» (бесплатно) . Микробиология . 144 (9): 2377–2406. DOI : 10.1099 / 00221287-144-9-2377 . PMID 9782487 .
- Перейти ↑ Hogan, C. Michael (2010). «Экстремофил» у Э. Моноссона и К. Кливленда (ред.). Энциклопедия Земли . Национальный совет по науке и окружающей среде, Вашингтон, округ Колумбия
- ^ «Марсианская жизнь должна быть редкостью, поскольку свободный источник энергии остается неиспользованным» . Новый ученый . 13 мая 2017 года.
- ^ Jaouen Г., изд. (2006). Биоорганометаллические вещества: биомолекулы, маркировка, медицина . Вайнхайм: Wiley-VCH. ISBN 978-3-527-30990-0.
- ^ Робертс, GP; Юн, H .; Керби, Р.Л. (2004). «Механизмы зондирования CO» . Обзоры микробиологии и молекулярной биологии . 68 (3): 453–473. DOI : 10.1128 / MMBR.68.3.453-473.2004 . PMC 515253 . PMID 15353565 .
- ^ Глобальные карты. Окись углерода . earthobservatory.nasa.gov
- ^ Источник цифр: углекислый газ, Лаборатория исследования системы Земли NOAA , (обновлено 2010.06). Метан, таблица 6.1 ТДО МГЭИК (обновлена до 1998 г.). Общее количество НАСА составило 17 частей на миллион по объему более 100%, а содержание CO 2 увеличилось на 15 частей на миллион по объему. Для нормализации содержание N 2 должно быть уменьшено примерно на 25 частей на миллион по объему, а O 2 - примерно на 7 частей на миллион по объему.
- ^ Комитет по медицинскому и биологическому воздействию загрязнителей окружающей среды (1977). Окись углерода . Вашингтон, округ Колумбия: Национальная академия наук. п. 29. ISBN 978-0-309-02631-4.
- ^ Грин В. "Введение в качество воздуха в помещении: окись углерода (CO)" . Агентство по охране окружающей среды США . Проверено 16 декабря 2008 .
- ^ Gosink, Том (1983-01-28). "Что означают уровни окиси углерода?" . Научный форум Аляски . Геофизический институт Университета Аляски в Фэрбенксе. Архивировано из оригинала на 2008-12-25 . Проверено 1 декабря 2007 .
- ^ Певец, Зигфрид Фред (1975). Изменяющаяся глобальная среда . Springer. п. 90. ISBN 978-9027704023.
- ^ a b «Отравление угарным газом: Транспортные средства (AEN-208)» . abe.iastate.edu . Проверено 11 февраля 2018 .
- ^ Gosink T (28 января 1983). "Что означают уровни окиси углерода?" . Научный форум Аляски . Геофизический институт Университета Аляски в Фэрбенксе. Архивировано из оригинала 25 декабря 2008 года . Проверено 16 декабря 2008 года .
- ^ Сигель, Астрид; Сигель, Роланд КО (2009). Связи металл-углерод в ферментах и кофакторах . Королевское химическое общество. п. 243. ISBN. 978-1-84755-915-9.
- ^ Уайт, Джеймс Кэррик; и другие. (1989). Связи с глобальным изменением климата: кислотные дожди, качество воздуха и стратосферный озон . Springer. п. 106. ISBN 978-0-444-01515-0.
- ↑ Драммонд, Джеймс (2 февраля 2018 г.). «МОПИТТ, загрязнение атмосферы и я: личная история» . Канадское метеорологическое и океанографическое общество . Проверено 1 августа 2018 года .
- ^ Pommier, M .; Закон, KS; Clerbaux, C .; Turquety, S .; Hurtmans, D .; Hadji-Lazaro, J .; Coheur, P.-F .; Schlager, H .; Анселлет, G .; Paris, J.-D .; Nédélec, P .; Дискин, GS; Подольское, младший; Холлоуэй, JS; Бернат П. (2010). «Проверка содержания окиси углерода IASI над Арктикой во время весенних и летних кампаний POLARCAT» . Химия и физика атмосферы . 10 (21): 10655–10678. Bibcode : 2010ACP .... 1010655P . DOI : 10,5194 / ACP-10-10655-2010 .
- ^ Pommier, M .; МакЛинден, Калифорния; Дитер, М. (2013). «Относительные изменения выбросов CO над мегаполисами на основе наблюдений из космоса» . Письма о геофизических исследованиях . 40 (14): 3766. Bibcode : 2013GeoRL..40.3766P . DOI : 10.1002 / grl.50704 .
- ^ Ривз, Клэр E .; Penkett, Stuart A .; Богитт, Стефан; Закон, Кэти С .; Эванс, Мэтью Дж .; Бэнди, Брайан Дж .; Монахи, Пол С .; Эдвардс, Гэвин Д .; Филлипс, Гэвин; Барджат, Ханна; Кент, Джосс; Дьюи, Кен; Шмитген, Сандра; Клей, Дитер (2002). «Возможность фотохимического образования озона в тропосфере над Северной Атлантикой, по данным наблюдений с самолетов во время ACSOE» . Журнал геофизических исследований . 107 (D23): 4707. Bibcode : 2002JGRD..107.4707R . DOI : 10.1029 / 2002JD002415 .
- ^ Озон и другие фотохимические окислители . Национальные академии. 1977. с. 23. ISBN 978-0-309-02531-7.
- ^ a b c Комиссия по безопасности потребительских товаров США , Вопросы и ответы по оксиду углерода Архивировано 9 января 2010 г. в Wayback Machine , доступ осуществлен 4 декабря 2009 г.
- ^ «Отслеживание угарного газа» . Отслеживание экологического состояния здоровья населения - Департамент здравоохранения Флориды. Архивировано из оригинала на 2011-09-27.
- ^ "Годовые отчеты AAPCC 2007" . Американская ассоциация центров по борьбе с отравлениями.
- ^ Центры по контролю и профилактике заболеваний, Национальная сеть отслеживания общественного здоровья в области окружающей среды, Отравление угарным газом , доступ 2009-12-04.
- ^ «Окись углерода (кровь) - Энциклопедия здоровья - Медицинский центр Университета Рочестера» . urmc.rochester.edu .
- ^ Engel, Rolf R .; Родки, Ф. Ли; Крилл, Карл Э. (1 апреля 1971 г.). «Уровни карбоксигемоглобина как показатель гемолиза» . Педиатрия . 47 (4): 723–730. PMID 5104458 - через pediatrics.aappublications.org.
- ^ Roth D .; Herkner H .; Schreiber W .; Hubmann N .; Gamper G .; Лаггнер А.Н.; Гавел С. (2011). «Точность неинвазивной многоволновой импульсной оксиметрии по сравнению с карбоксигемоглобином из анализа газов крови у неотобранных пациентов отделения неотложной помощи» (PDF) . Летопись неотложной медицины . 58 (1): 74–9. DOI : 10.1016 / j.annemergmed.2010.12.024 . PMID 21459480 .
- ^ Комб, Франсуаза (1991). «Распределение CO в Млечном Пути». Ежегодный обзор астрономии и астрофизики . 29 : 195–237. Bibcode : 1991ARA & A..29..195C . DOI : 10.1146 / annurev.aa.29.090191.001211 .
- ^ Хан, Амина. «Столкнулись ли две планеты вокруг ближайшей звезды? Токсичный газ содержит подсказки» . Лос-Анджелес Таймс . Проверено 9 марта 2014 года .
- ^ Дент, WRF; Wyatt, MC; Roberge, A .; Augereau, J.C .; Casassus, S.; Corder, S .; Гривз, JS; де Грегорио-Монсальво, I; Хейлз, А .; Джексон, AP; Хьюз, А. Мередит; Лагранж, А.-М; Matthews, B .; Вильнер, Д. (6 марта 2014 г.). "Молекулярные газовые сгустки от разрушения ледяных тел в диске обломков β Pictoris" . Наука . 343 (6178): 1490–1492. arXiv : 1404,1380 . Bibcode : 2014Sci ... 343.1490D . DOI : 10.1126 / science.1248726 . PMID 24603151 . S2CID 206553853 . Проверено 9 марта 2014 года . CS1 maint: использует параметр авторов ( ссылка )
- ^ Гринберг, Дж. Мэйо (1998). «Создание ядра кометы». Астрономия и астрофизика . 330 : 375. Bibcode : 1998A & A ... 330..375G .
- ^ Йоманс, Дональд К. (2005). "Кометы (Справочный центр World Book Online 125580)" . НАСА. Архивировано из оригинального 29 апреля 2005 года . Проверено 20 ноября 2007 года .
- ^ Lellouch, E .; de Bergh, C .; Sicardy, B .; Ferron, S .; Käufl, H.-U. (2010). «Обнаружение CO в атмосфере Тритона и характер взаимодействия поверхности и атмосферы». Астрономия и астрофизика . 512 : L8. arXiv : 1003,2866 . Бибкод : 2010A & A ... 512L ... 8L . DOI : 10.1051 / 0004-6361 / 201014339 . ISSN 0004-6361 . S2CID 58889896 .
- ^ Кристофер Glein и Хантер Уэйт (11 мая 2018). «Изначальный N2 дает космохимическое объяснение существования Sputnik Planitia, Плутон». Икар . 313 : 79–92. arXiv : 1805.09285 . Bibcode : 2018Icar..313 ... 79G . DOI : 10.1016 / j.icarus.2018.05.007 . S2CID 102343522 .
- ^ «MSHA - Программа профилактики профессиональных заболеваний и травм - Вопросы здоровья - Окись углерода» . arlweb.msha.gov . Архивировано из оригинала на 2017-12-31 . Проверено 31 декабря 2017 .
- ^ Holleman, AF; Виберг, Э. "Неорганическая химия" Academic Press: Сан-Диего, 200. ISBN 0-12-352651-5 .
- ^ Хигман, C; ван дер Бургт, М. (2003). Газификация . Издательство Gulf Professional Publishing. п. 12 . ISBN 978-0-7506-7707-3.
- ^ Чжэн, Юнь; Ван, Цзяньчэнь; Ю, Бо; Чжан, Вэньцян; Чен, Цзин; Цяо, Цзиньли; Чжан, Цзюцзюнь (2017). «Обзор высокотемпературного совместного электролиза H2O и CO для производства экологически безопасных видов топлива с использованием твердооксидных электролизных ячеек (SOEC): передовые материалы и технологии». Chem. Soc. Ред . 46 (5): 1427–1463. DOI : 10.1039 / C6CS00403B . PMID 28165079 .
- ^ «Новый путь к углеродно-нейтральному топливу из углекислого газа, обнаруженный командой Stanford-DTU - DTU» . dtu.dk .
- ^ Skafte, Theis L .; Гуань, Цзысюань; Machala, Michael L .; Gopal, Chirranjeevi B .; Монти, Маттео; Мартинес, Лев; Стамат, Евгений; Санна, Симона; Гарридо Торрес, Хосе А .; Крамлин, Итан Дж .; Гарсия-Мельчор, Макс; Байдич, Михал; Чуэ, Уильям С .; Грейвс, Кристофер (8 октября 2019 г.). «Селективный высокотемпературный электролиз CO 2 с использованием промежуточных продуктов окисленного углерода» . Энергия природы . 4 (10): 846–855. DOI : 10.1038 / s41560-019-0457-4 . S2CID 202640892 - через www.nature.com.
- ^ a b Koch, H .; Хааф, В. (1973). «1-Адамантанкарбоновая кислота» . Органический синтез .; Сборник , 5 , с. 20
- ^ а б Коулман, GH; Крейг, Дэвид (1943). « п- толуальдегид» . Органический синтез .; Сборник , 2 , стр. 583
- ^ Брауэр, Георг (1963). Справочник по препаративной неорганической химии Vol. 1, 2-е изд . Нью-Йорк: Academic Press. п. 646. ISBN. 978-0121266011.
- ^ Монд L, Лангер K, Quincke F (1890). «Действие окиси углерода на никель» . Журнал химического общества . 57 : 749–753. DOI : 10.1039 / CT8905700749 .
- ^ Chatani, N .; Мураи, С. «Окись углерода» в Энциклопедии реагентов для органического синтеза (Эд: Л. Пакетт) 2004, J. Wiley & Sons, Нью-Йорк. DOI : 10.1002 / 047084289X
- ^ Büchner, W .; Вайс, Э. (1964). "Zur Kenntnis der sogenannten" Alkalicarbonyle "IV [1] Über die Reaktion von geschmolzenem Kalium mit Kohlenmonoxid". Helvetica Chimica Acta . 47 (6): 1415–1423. DOI : 10.1002 / hlca.19640470604 .
- ^ Фаунс, Джордж (1869). Учебное пособие по элементарной химии . ХК Леа. п. 678 .
- ^ Кац, Аллен I .; Шиферл, Дэвид; Миллс, Роберт Л. (1984). «Новые фазы и химические реакции в твердом оксиде углерода под давлением». Журнал физической химии . 88 (15): 3176–3179. DOI : 10.1021 / j150659a007 .
- ^ Эванс, WJ; Липп, MJ; Yoo, C.-S .; Cynn, H .; Herberg, JL; Максвелл, RS; Николь, MF (2006). «Под давлением полимеризации окиси углерода: диспропорционирование и синтез энергетического лактонного полимера» . Химия материалов . 18 (10): 2520–2531. DOI : 10.1021 / cm0524446 .
- ^ Elschenbroich, C .; Зальцер, А. (2006). Металлоорганические соединения: краткое введение (2-е изд.). Вайнхайм: Wiley-VCH. ISBN 978-3-527-28165-7.
- ↑ Вольфганг Шнайдер; Вернер Диллер. «Фосген». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a19_411 .
- ^ Сорхейм, S; Ниссена, H; Несбаккен, Т. (1999). «Срок хранения говядины и свинины, упакованных в атмосфере с низким содержанием окиси углерода и высоким содержанием углекислого газа». Журнал мясной науки . 52 (2): 157–164. DOI : 10.1016 / S0309-1740 (98) 00163-6 . PMID 22062367 .
- ^ Eilert EJ (2005). «Новые упаковочные технологии 21 века». Журнал мясной науки . 71 (1): 122–127. DOI : 10.1016 / j.meatsci.2005.04.003 . PMID 22064057 .
- ^ Хаффман, Рэндалл Д. «Упаковка с низким содержанием кислорода с CO: исследование политики в области пищевых продуктов, которое требует экспертной оценки» . FoodSafetyMagazine.com . Проверено 18 апреля 2007 года .
- ^ «Закон о безопасном обращении, маркировке и защите потребителей мяса, птицы и морепродуктов, обработанных угарным газом (введен в производство)» . Библиотека Конгресса . 2007-07-19.
- ^ «Доказательство в розовом? Мясо, обработанное, чтобы придать ему свежий вид» . ABC News. 14 ноября 2007 . Проверено 5 мая 2009 года .
- ^ Окись углерода в упаковке мяса: мифы и факты . Американский институт мяса. 2008. Архивировано из оригинала на 2011-07-14 . Проверено 5 мая 2009 года .
- ^ «CO в упакованном мясе» . Кампания «Убивает угарный газ». Архивировано из оригинального 26 сентября 2010 года . Проверено 5 мая 2009 года .
- ^ Ионин, А .; Киняевский, И .; Климачев, Ю .; Котков, А .; Козлов, А. (2012). «Новая лазерная система на угарном газе с синхронизацией мод обеспечивает высокую точность». Отдел новостей SPIE . DOI : 10.1117 / 2.1201112.004016 . S2CID 112510554 .
- Перейти ↑ Landis (2001). "Марсианский ракетный аппарат с использованием ракетного топлива in situ". Журнал космических аппаратов и ракет . 38 (5): 730–735. Bibcode : 2001JSpRo..38..730L . DOI : 10.2514 / 2.3739 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме окиси углерода . |
- Глобальная карта распределения окиси углерода
- Объяснение конструкции
- Ассоциация по безопасности угарного газа
- Международная карта химической безопасности 0023
- CDC Карманный справочник NIOSH по химической опасности: окись углерода - Национальный институт профессиональной безопасности и здоровья (NIOSH), Центры США по контролю и профилактике заболеваний (CDC)
- Угарный газ - Тема безопасности и здоровья NIOSH - CDC
- Отравление угарным газом - часто задаваемые вопросы —CDC
- Лист данных внешнего паспорта безопасности материалов
- Размещение детектора угарного газа
- Процесс очистки окиси углерода
- Микромасштабные газохимические эксперименты с оксидом углерода
- «Мгновенное понимание: не обвиняйте посланника» . Химическая биология (11: Новости исследований). 18 октября 2007 года Архивировано из оригинала 28 октября 2007 года . Проверено 27 октября 2019 года . Изложение физиологии окиси углерода от Королевского химического общества .

