 | |
 | |
| Имена | |
|---|---|
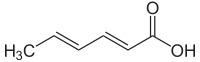
| Название ИЮПАК (2 E , 4 E ) -гекса-2,4-диеновая кислота | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.003.427 |
| Номер E | E200 (консерванты) |
PubChem CID | |
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| С 6 Н 8 О 2 | |
| Молярная масса | 112,128 г · моль -1 |
| Плотность | 1,204 г / см 3 |
| Температура плавления | 135 ° С (275 ° F, 408 К) |
| Точка кипения | 228 ° С (442 ° F, 501 К) |
| 1,6 г / л при 20 ° C | |
| Кислотность (p K a ) | 4,76 при 25 ° C |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Сорбиновая кислота или 2,4-гексадиеновая кислота - это природное органическое соединение, используемое в качестве консерванта для пищевых продуктов . [1] Он имеет химическую формулу CH 3 (CH) 4 CO 2 H. Это бесцветное твердое вещество, которое слабо растворяется в воде и легко сублимируется . Впервые он был выделен из незрелых ягод рябины обыкновенной ( рябины ), отсюда и название.
Производство [ править ]
Традиционный путь получения сорбиновой кислоты включает конденсацию малоновой кислоты и транс-бутеналя . [2] Его также можно получить из изомерных гексадиеновых кислот, которые доступны в результате катализируемой никелем реакции аллилхлорида , ацетилена и монооксида углерода . Однако коммерчески используемый путь основан на кротоновом альдегиде и кетене . [3] Ежегодно производится около 30 000 тонн. [4]
История [ править ]
Сорбиновая кислота была выделена в 1859 году путем перегонкой из рябиновой нефти по AW фон Гофману . В результате образуется парасорбиновая кислота , лактон сорбиновой кислоты, который он превращает в сорбиновую кислоту путем гидролиза. Его противомикробное действие было обнаружено в конце 1930-х и 1940-х годах, а коммерческое использование препарата появилось в конце 1940-х и 1950-х годах. Начиная с 1980-х годов сорбиновая кислота и ее соли использовались в качестве ингибиторов Clostridium botulinum в мясных продуктах, чтобы заменить нитриты , которые могут производить канцерогенные нитрозамины . [5]
Свойства и использование [ править ]
При p K a 4,76 он примерно такой же кислый, как уксусная кислота.
Сорбиновая кислота и ее соли, такие как сорбат натрия , сорбат калия и сорбат кальция , являются антимикробные агенты , часто используемые в качестве консервантов в продуктах питания и напитков , чтобы предотвратить рост плесени , дрожжей и грибов . В общем, соли предпочтительнее кислотной формы, поскольку они более растворимы в воде, но активной формой является кислота. Оптимальный pH для противомикробной активности ниже pH 6,5. Сорбаты обычно используются в концентрациях от 0,025% до 0,10%. Однако добавление солей сорбата к пище немного повысит pH продукта, поэтому, возможно, потребуется отрегулировать pH для обеспечения безопасности. Он содержится в таких продуктах, как сыр и хлеб.
Эти цифры E являются:
- E200 Сорбиновая кислота
- E201 Сорбат натрия
- E202 Сорбат калия
- E203 Сорбат кальция
Некоторые плесневые грибки (в частности, некоторые штаммы Trichoderma и Penicillium ) и дрожжи способны детоксифицировать сорбаты декарбоксилированием с образованием транс- 1,3-пентадиена . Пентадиен проявляется как типичный запах керосина или нефти . Другие реакции детоксикации включают восстановление до 4- гексенола и 4-гексеновой кислоты. [6]
Сорбиновая кислота также может использоваться в качестве добавки к холодной резине и в качестве промежуточного продукта при производстве некоторых пластификаторов и смазок . [7]
Безопасность [ править ]
Этот раздел требует дополнительных ссылок для проверки . ( Январь 2018 г. ) ( Узнайте, как и когда удалить этот шаблон сообщения ) |
LD 50содержание сорбиновой кислоты составляет от 7,4 до 10 г / кг. Таким образом, сорбиновая кислота и сорбаты обладают очень низкой токсичностью для млекопитающих - отсюда их широкое применение для консервирования продуктов питания и напитков. Сорбиновая кислота естественным образом содержится в лесных ягодах, относительно нестабильна и быстро разлагается в почве, поэтому считается экологически чистой. В организме он обычно метаболизируется тем же путем окисления, что и капроновая кислота, насыщенная 5 углеродными жирными кислотами. Существует общее мнение о том, что сорбиновая кислота и сорбаты по своей природе не обладают канцерогенной активностью. Однако было показано, что они могут превращаться в потенциальные мутагены либо за счет окисления, либо за счет химической реакции с нитритами при pH 2-4,2 - последние условия имитируют среду желудка.В живых клетках дрожжей сорбиновая кислота усиливает образование свободных радикалов кислорода митохондриальной цепью переноса электронов, что приводит к повреждению митохондриальной ДНК.
См. Также [ править ]
- Сорбитол
- Полисорбат
- Кислоты в вине
- Парасорбиновая кислота
Ссылки [ править ]
- ^ Piper JD, Piper PW (2017). «Бензоатные и сорбатные соли: систематический обзор потенциальных опасностей этих бесценных консервантов и расширяющийся спектр клинического использования бензоата натрия» . Комплексные обзоры в области пищевой науки и безопасности пищевых продуктов . 16 (5): 868–880. DOI : 10.1111 / 1541-4337.12284 .
- ^ CFH Аллен, Дж. Ваналлан (1944). "Сорбиновая кислота". Орг. Synth . 24 : 92. DOI : 10,15227 / orgsyn.024.0092 .CS1 maint: использует параметр авторов ( ссылка )
- ^ Словарь промышленных химикатов Эшфорда , третье издание, 2011 г., стр. 8482
- ^ Эрих Люк, Мартин Ягер и Нико Рачек «Сорбиновая кислота» в Энциклопедии промышленной химии Ульманна , Wiley-VCH, Weinheim, 2000. doi : 10.1002 / 14356007.a24_507
- ^ А.С. Найду, изд. (2000). Натуральные пищевые противомикробные системы . п. 637. ISBN. 0-8493-2047-X.
- ^ Киндерлерер JL, Хаттон П. (1990). «Грибковые метаболиты сорбиновой кислоты». Пищевая добавка Contam . 7 (5): 657–69. DOI : 10.1080 / 02652039009373931 . PMID 2253810 .
- ^ Bingham E, Cohrssen B (2012). Токсикология Пэтти . Джон Вили и сыновья. п. 547.
Внешние ссылки [ править ]
- Sorbic inchem.org
